ҚАЗАҚСТАН РЕСПУБЛИКАСЫ БІЛІМ ЖӘНЕ ҒЫЛЫМ МИНИСТРЛІГІ
ҚАРАҒАНДЫ МАҢЫЗДЫ БІЛІМ БЕРУ КОЛЛЕДЖІ «БОЛАШАК»
Жалпы білім беретін пәндер кафедрасы
«Химия» пәні бойынша
1-курс студенттері үшін
ЖҰМЫС ДӘПТЕРІ
Құрастырған: Жарқымбекова А.Т.,
Қарағанды 2018
Мазмұны:
Алғысөз
I тарау. 1.1Атом құрылысының заманауи теориясы, атомдағы электрондар күйі, квант саны________________________________________________________________________4
1.2Атом құрылысы тұрғысынан периодтық заң және химиялық элементтердің периодтық жүйесі.______________________________________________________________________5
1.3 Химиялық элементтенрдің электр терістігі, радиоактивтілік, валенттілік және тотығу жәрежесі. Химиялық элементтердің электртерістілігі.____________________________6
I тарау бойынша тест тапсырмалары___________________________________________7-8
ІІ тарау. 2.1Химиялық байланыс және зат құрылысы.Химиялық байланыс_____________9
2.2.Үлестірмелі тапсырмалар__________________________________________________10
IІ тарау бойынша тест тапсырмалары___________________________________________11
ІІІ тарау. 3.1 Элементтепдің олардың жоғары оксидтері,гидроксидтері, сутекті қосылыстарының қасиеттерінің өзгеруінің периодтылығы_________________________12.
3.2. Химиялық реакциялар және олардың жүру заңдылықтары Химиялық реакциялардың жіктелуі. 3.3Химиялық реакциялар, жылу эффектісі 3.4.Химиялық реакциалардың жылдамдығы 3.5.Химиялық тепе-теңдік._________________________________________13
ІІІ тарау бойынша қорытынды тест сұрақтары_________________________________14-16
ІV тарау. 4.1.Металдармен бейметалдардың жалпы сипаттамасы. Сілтілік металл.
4.2Металдардың жалпы қасиеттері. І-ІІІ топтағы негізгі топшадағы металдар
4.3Металдарды алу әдістері 4.4Металдардың химиялық қасиеттері.4.5. Электролиз. Металдардың коррозиясы._________________________________________________ 17-19
1V тарау бойынша тест тапсырмалары_______________________________________20-22
V тарау. 5.1. Күкірт. Күкірт қышқылы________________________________________
5.2. Tақырып бойынша қорытындылау_________________________________________20
YI тарау. 6.1.Азот топшасы. 6.2. Азот қышқылы және оның тұздары________________21
YII тарау.7.1. Фосфор және оның қосылыстары________________________________22-24
7.2. Реакцияның өкімінің шығымы теорилықпен салыстырғандағы массалық және көлемдік үлестерін анықтау бойынша есептеулер______________________________25-27
YIII тарау. 8.1. Көміртегі топшасы. 8.2. Көмір қышқылы және оның тұздары
8.3. Кремний және оның қосылыстары.________________________________________29
8.4. Қоспасы бар заттың белгілі массасы немесе көлемі бойынша реакция өнімінің масасын немесе көлемін есептеу____________________________________________30-34
8.5. Өндірістік және пәнаралық мазмұны бар тапсырмалар Бейметалдар____________35
X тарау 10.1. Алюминий және оның қосылыстары_______________________________36
10.2. Тарау бойынша қорытындылау__________________________________________37
XI тарау. 11.1. Темір. Металлургия. 11.2. Өнеркәсіпте металдар алудың әдістері______38
XII тарау. 12.1. Органикалық заттар. Көмірсутектер._____________________________ 40
12.2. ХІІ тарау бойынша қорытындылау________________________________________41
XIII тарау. 13.1.Оттекті органикалық қосылыстар Спирттер.Альдегидтер мен
кетондар. Көмірсулар. _____________________________________________________42
13.2. Карбон қышқылдары және биологиялық маңызды органикалық заттар___________________________________________________ _______________43-49
13.4. XIII тарау бойынша қосымша тапсырмалар.________________________________31
13.5. «Органикалық заттар» тақырыбын қорытыныдлауға арналған сұрақтар_________32
Химиядан сабағында қолданылатын жұмыс дәптері
Алғысөз
Бұл көмекші құралдың мақсаты - химияны оқу барысында студенттердің бағдарламалық материалды меңгеру деңгейін анықтауда оқытушыларға көмек болу.
Мұнда бейорганикалық, органикалық химия курсының барлық тақырыптары бойынша бірнеше жұмыстар берілген, бұл оқытушыларға студенттердің жекелеген мәселелер бойынша білімін тексеруге мүмкіндік береді. Барлық жұмыстар төрт нұсқада берілген, олар мазмұны мен сипаттамасы бойынша ұқсас болып келеді. Тапсырмалар өзінің дидактикалық мақсаты бойынша ерекшеленеді: олардың біреуі студенттерден тек материалды қарапайым қайталауды талап етсе, екіншілері салыстырып, анализ жасауға машықтандырады, үшіншілері шығармашылық деңгейде ойлап, жаңа жағдаяттарда оны қолдана білу деңгейін талап етеді.
Мұндай тапсырмалар жалпылама жұмыста барлық студенттерді бірдей жұмылдыруға да, олардың жеке жұмысын ұйымдастыруға да мүмкіндік береді. Әр тақырып қорытындалады, бұл барлық тақырып бойынша студенттердің білімін тексеруде ыңғайлы болып табылады.
Тарауды қайталау, қорытындылау кезінде қолданып, тақырыпқа байланысты сөздік қорларын молайтып, өткен тақырыптың мазмұнын толық ашу үшін сәйкестендіру кестесін толтырғызып, сабақты бекітемін. Әр тарауды өткен соң, химиялық диктант, өздік жұмыс, тақырыптық есеп, бақылау жұмыстары, тестік тапсырмалар өткізу арқылы тақырыпты қаншалықты меңгергенін тексеріп, тақырыпты толық меңгере алмаған студенттермен қосымша сабақтар жүргіземін. Тест түрлері студенттер білімін бекітуге қайталауға, жүйелеуге мүмкіндік береді. Сонымен қоса оқытушы мен студенттердің уақытын үнемдеуге оқу жұмысын ұйымдастыруға жағдай жасайды. Тестік тапсырмаларды студенттердің білім деңгейіне байланысты құрастырып, нәтижесін кілтімен тексертіп өздеріне бағалатамын. Егер жауап-75%-дан жоғары болса-«жақсы»,-50%-ға дейін «қанағаттанарлық»,-50%-дан төмен-білім деңгейі «төмен» көрсеткішпен бағаланады. Баға-бейне бір белгі және сонымен қатар өлшем сияқты, ол оқытудың нәтижелілік дәрежесін анықтауға мүмкіндік береді.
Химия пәні табиғаттың құпиясын түсінуге көмектеседі. Осы себептен теориялық білімді практикада ұштастыру қажет. Қазіргі уақытта химия кабинеттерінің материалдық техникалық базасы төмен, құрал жабдықтар, лабораториялық құралдар, реактивтер жетпеген жағдайға келіп отырмыз. Осы себептен практикалық жұмыстарды өткізу барысында және практикалық сабақтар қызықты, ұйымдастырушылықпен, нәтижелі өту үшін және химия пәніне студенттердің қызығушылығын арттыру, жекелеген жұмыс жасау үшін осы жұмыс дәптерді ұсынып отырмын.
Ұсынылып отырған дидактикалық құралдың мазмұны негізгі оқулыққа сәйкес құрастырылған.
Сіздерге химиядан практикалық жұмыстарға арналған жұмыс дәптерін ұсынып отырмын. Барлық тапсырмаларды орындаған кезінде оқулықты, интерактивті тақтаны, электронды оқулықтарды пайдаланып, өзара жұмыс жасап химиядан білімдерінді жетілдіруге болады.
I тарау. 1.1Атом құрылысының заманауи теориясы, атомдағы электрондар күйі, квант саны Атом құрылысы. Изотоп. (§53-§55)
І-деңгей.
1. Изотоп дегеніміз не?2. Кестені толтырыңдар:
| Оттек изотоптары |
|
|
|
| Протондардың саны |
|
|
|
| Нейтрондар саны |
|
|
|
| Электрондар саны |
|
|
|
| Ядро заряды |
|
|
|
| Атомдық массалары |
|
|
|
3. Изотоп қандай мағына білдіреді?
4. Химиялық элемент дегеніміз не?
5. Д.И.Менделеевтің периодтық заңы қалай тұжырымдалады?
ІІ-деңгей
1. Белгісіз 15 электроны бар. Олардың энергиялық деңгейлерге орналастырыңдар.
2. Магнийдің массалық сандары 24, 25 және 26 болатын изотоптары бар. Табиғаттағы магнийде олардың проценттік мөлшері 78,60%, 10,11%, 11,29% сәйкес келеді. Магнийдің салыстырмалы атомдық массасын есептеңдер:
3. Кестеде көрсетілген элементар бөлшектердің саны бойынша элементтерді анықтаңдар:
| Элементар бөлшектер | Элемент | |||
| Протондар саны | Нейтрондар саны | Электрондар саны | ||
| 14 24 70 |
|
|
| |
4. Литий, азот, натрий және хлор атомдары электрондарының энергиялық деңгейлерде орналасуын жазып көрсетіңдер.
ІІІ- деңгей
1. Кестеге химиялық элемент таңбаларын және оларға сай электрондық конфигурацияларын жазыңдар.
| Элемент | Электрондық конфигурациясы | Электрондық-графиктік формуласы |
|
|
|
|
2. Сәйкестендіру тесті:
1. атомдағы электрондар саны а) топ нөмірі(негізгі топша үлкен)
2. атом ядросындағы протондар саны ә) ядро заряды
3. атом ядросындағы нейтрондар саны б) реттік нөмері
4. атомның сыртқы электронды в) период нөмері
қабатындағы электрондар саны
5. атомдағы электрондық қабаттар саны г) Ar-Z
3. Электрондық құрылысы төмендегідей элементтер металдар ма, әлде бейметалдар ма? а) 2,1; ә) 2,8,6; б) 2,8,2 Аттарын атаңдар.
1.2Атом құрылысы тұрғысынан периодтық заң және химиялық элементтердің периодтық жүйесі.
І-деңгей.
1. Сілтілік металдарға сәйкес келетін элементтердің формуласын жазып, атаңдар.
2. Периодттық заңды кім және қашан ашты?
3. Мына элементтердің ішінен металдарды теріп жазып, оларды атаңдар:
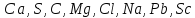
4. Период дегеніміз не?. Атом құрылысын кім және қашан ашты?
ІІ-деңгей.
1. Д.И.Менделеевтің периодтық заңы қалай тұжырымдалады?
2. Атом құрылысы қандай? Реттік номер нені білдіреді?
3. Кестені толтырыңдар.
| Элемент аты | Таңбасы | Реттік номері | Ядроны құраушылар саны | ||
| +р | n0 | e- | |||
|
|
| 6 |
|
|
|
|
|
| 13 |
|
|
|
| оттегі |
|
|
|
|
|
| мыс |
|
|
|
|
|
|
| Sb |
|
|
|
|
|
| Mo |
|
|
|
|
4. Мына өзгерістерді жүзеге асырыңдар.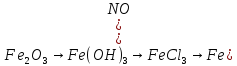
I тарау бойынша тест тапсырмалары
1. Периодтық жүйедегі элементтің алатын орны қалай анықталады:
а) сыртқы электрон қабатындағы электрондар санымен;
ә) ядродағы нейтрондар санымен;
б) атомдық массасымен;
в) атом ядросының зарядымен.+
2. Атомдағы энергиялық деңгейлер саны қалай анықталады:
а) элементтің реттік нөмірімен;
ә) топтың нөмірімен;
б) қатардың нөмірімен;
в) периодтың нөмірімен.+
3. Периодтағы элементтер қасиеттері өзгеруінің негізгі себебі неде:
а) жаңа электрондық қабаттың пайда болуында;
ә) сыртқы қабатта электрондардың жиналуында;
б) атомдық массасының өсуінде;
в) атомдағы электрондар санының өсуінде.+
4. Негізгі топшадағы элементтер қасиеттерінің өзгеру себебі неде?
а) атомдық массаларының өсуінде;
ә) жаңа электрон қабатының пайда болуында;+
б) атомдағы электрондар санының көбеюінде.
в) атом ядросындағы нейтрондар санының көбеюінде.
5. Бейметалдардың таңбасын көрсетіңдер.... (Д.И.Менделеев кестесін пайдаланыңдар):
а) Na;ә)Mg; б)H;+ в)S.+
6. Металдардың таңбасын көрсетіңдер..(Д.И.Менделеев кестесін қараңдар)
а) Na;+ ә)Mg;+ б)O; в)Si.
7. Мына берілген элементтер қатарының қайсысы жалпы формуласы RO болатын оксидтер түзеді:
а) Mg,,Ca,Be+ ә)Na,K,Li .б)B,Al,Ga в)N,P,As
8. Төменде берілген элементтер қатарының қайсысы жалпы формуласы
R2O болатын оксидтер түзеді:
а) Mg, Ca,Be ә) Na, K, Li+ б) B, Al, Ca в) N, P,As
9. Біріншісінен соңғысына қарай бейметалдық қасиеттері артатын элементтер қатары:
а) Na,Mg,Si,Al ә) Mg, Ca,Sr, Ba б)K,H,Na,Li в)I,Br,Cl,At+
10. Біріншісінен соңғысына қарай металдық қасиеттері артатын элементтер қатары:
а) Na, Mg, Al ә) Na, K, Ca б)Na,K,Pb+ в)P,S,Cl
11. Қай элементтің атом мөлшері ең кіші:
а) Na+ ә) K б) Mg в) S
12. Қай элементтің атом мөлшері ең кіші
а) Mg ә) K б) Ca в) H+
13. Көміртектің ең үлкен валенттігі
а) 1 – ге; ә) 2 – ге; б) 3 – ке; в) 4 – ке тең+
14. Күкірттің ең үлкен валенттігі:
а) 2 – ге; ә) 3 – ке; б) 4 – ке; в) 6 – ға+.
15. Қай элементтердің атомдарына электрондарды қосып алғаннан беріпа жіберу оңай:
а) Д.И.Менделеев кестесінде ІІ топтың негізгі топшасында орналасқандарға;+
ә) VІІ топтың негізгі топшасында орналасқандарға;
б) 2 – периодтың ортасында орналасқандарға;
в) 2 – периодтың басында орналасқандарға.
16. Төмендегі элементтер атомдары электрондарды қосып алуға да, беріп жіберуге де қабілетті:
а) І топтың негізгі топшасындағы;
ә) 1V топтың негізгі топшасындағы;+
б) 2 – периодтың басындағы;
в) 2 – периодтың ортасындағы
17. Фтор атомындағы электрондардың энергиялық деңгейлерде орналасуы:
а) 2,8,4 ә) 2,6 б) 2,7+ в) 2,8,5
18. Қай элемент газ күйінде сутекті қосылыс түзеді:
а) №22 ә) №6+ б) №23 в) №24
19. Қай топтағы элементтер ұшқыш сутекті қосылыстар түзеді:
а) I; ә) ІІ; б) V; в)VII+
20. Натрий атомындағы электрондардың формуласы:
а) 1s22s22p3 ә) 1s22s22p4 б) 1s22s22p63s1 + в) 1s22s22p2
21. Күкірт атомының электрондық формуласы:
а) 2,1 ә) 2,8,1 б) 2,4 в) 2,8,6+
22. Элементтердің электрондық формуласы 1s22s22p3. Оның реттік нөмірін анықтаңдар:
а) №2 ә) №3 б) №5 в) №7+
1.3 Химиялық элементтенрдің электр терістігі, радиоактивтілік, валенттілік және тотығу жәрежесі. Химиялық элементтердің электртерістілігі.
| «Әркімнің өзі шығар биігі бар»деңгейлік тапсырмалар №3. Берілген химиялық реакциялардағы элементтердің тотығу дәрежелерін анықтап, электрондық баланс әдісімен реакцияның коэффициенттерін тауып қойыңдар: 2MnO2 + 2H2SO4 → 2MnSO4 + O2↑+ 2H2O 3C + 4HNO3 → 3CO2↑ + 4NO↑ + 2H2O 2AgNO3 → 2Ag + 2NO2↑ + O2↑ |
| Ойлан тап! (Химиялық терминдермен жұмыс) Тотығу – Тотықсыздану – Тотықтырғыш – Тотықсыздандырғыш – Баланс – |
| «Кім алғыр» №1 Мына қосылыстарды қай элементтің тотығу дәрежесі нольге тең және басқалары қандай тотығу дәрежесін көрсетеді ? H2S, N2, HJ,H2, NaF, Cl2, CaF2 №2 K2Cr2O7 қосылысындағы хромның тотығу дәрежесін есептеп шығар. |
| Тапсырма: а) Алюминийдің оттекпен; б) Темірдің хлормен; в) Литийдің күкіртпен тотығу-тотықсыздану реакцияларының теңдеулерін жазыңдар |
ІІ тарау. 2.1Химиялық байланыс және зат құрылысы.Химиялық байланыс(§61-§63)
І-деңгей.
1. Химиялық байланыс дегеніміз не? Ковалентті полюссіз байланыс дегеніміз не?
2. « 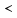 » немесе «
» немесе « 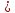 » белгілерінің көмегімен қай элементтің электртерістіктің шамасы үлкен екенін көрсетіңдер.
» белгілерінің көмегімен қай элементтің электртерістіктің шамасы үлкен екенін көрсетіңдер.
а) көміртегі мен күкірт ә) фтор мен хлор
күкірт пен хлор оттегі мен хлор
б) оттегі мен азот в) натрий мен калий
азот пен фтор натрий мен кремний
3. Кристалдық торлардың қандай түрлері бар?
4. Ковалентті полюсті байланыс және иондық байланыс дегеніміз не? Мысал келтіріңдер.
ІІ-деңгей
1. Мынадай қосылыстар түзілгенде электрондар қай элементке қарай ығысатынын көрсетіңдер:
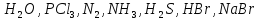
2. Мына заттардағы химиялық байланыс типтерін анықтаңдар: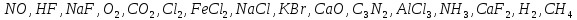
3. Берілген заттардың әрқайсысынң кристалдық тор типтерін анықтаңдар.
| Заттың аталуы | Заттың формуласы | Химиялық байланыстың типі | Кристалдық тор типі |
| 1. су(қатты күйі) 2. калий хлориді 3. йод 4. көміртек (алмаз) 5. мыс 6. көмірқышқыл газы 7. натирй сульфиді |
|
|
|
4. Кестені толтырыңдар
| Кристалдық тордың құрылысы | Өздеріне тән физикалық қасиеттері |
| 1. Иондық кристалдық тор 2. Молекулалық кристалдық тор. |
|
ІІІ- деңгей
1. ІІ топтағы металл қалыпты жағдайда сумен әркеттескенде 11,2 л сутек бөлінеді. Осы металды атаңдар.
2. Элементтің жоғары оксидінің формуласы - 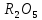 . Ал оның газ күйіндегі қосылысында сутектің мөлшері 17,65%. Осы элементті табыңдар.
. Ал оның газ күйіндегі қосылысында сутектің мөлшері 17,65%. Осы элементті табыңдар.
3. 23,4 г натрий хлориді күкірт қышқылымен әрекеттескенде хлорсутектің қандай көлемін алуға болады?
2.2.Үлестірмелі тапсырмалар
| № 2 тапсырма. Ой қозғау: «Жедел жауап»
№ 1 тапсырма. Ой қозғау: «Жедел жауап»
|
| № 1 тапсырма А) Ковалентті байланыс дегеніміз не? Ә) Химиялық байланыс түрлері мен бейорганикалық қосылыстардың кластарына ажыратыңдар: HF, H2, Br2O7, SiO2, F2, HNO3 |
| № 2 тапсырма А) Ковалентті полюссіз байланыс дегеніміз не? Ә) Химиялық байланыс түрлері мен бейорганикалық қосылыстардың кластарына ажыратыңдар: H2SO4, O2, CI2O7, SO2, B2O7, CI2 |
| № 1 тапсырма
|
| № 2 тапсырма
өзгереді? Жауабыңа түсінік бер. |
1. Қай элемент атомдары электрондарын беріп оң зарядталған иондарға айналады:
а) C;ә) Li;б) Ba; в) P
2. Қай элемент атомдары электрондарды қабылдап алып, теріс зарядталған иондарға айналады
а) Ca;ә)Na;б)F; в)Br
3. Электртерістіліктері бойынша айырмашылықтары үлкен атомдар арасында қандай байланыс түзіледі
а) иондықә) металдықб) коваленттік полюстів) коваленттік полюссіз
4. Электртерістіліктері бірдей атомдар арасында қандай байланыс түзіледі
а) иондықә) металдықб) коваленттік полюстів) коваленттік полюссіз
5. Берілген заттардың қайсыларында иондық байланыс бар
а) SO3ә) KClб) BaCl2в) NH3
6. Мына қосылыстардың қайсысында коваленттік полюсті байланыс бар
а) P2O5ә) CsFб) BaF2в)H2S
7. Мына заттардың қайсысының кристалды торы иондық
а) KFә) CsClб) HIв)Cl2
8. Мына заттардың қайсысының кристалды торы молекулалық
а) HFә)H2б)LiFв)BaCl2
9. Мына заттардың қайсысының балқу температурасы үлкен
а) LiFә) HIб) I2в)HCl
10. Мына заттардың қайсысының балқу температурасы үлкен
а) KFә) HBrб) Br2в) H2O
11. Қай қосылыста көміртектің тотығу дәрежесі +4
а) Na2CO3ә) CH4б) CO2в) SiC
12. Қай қосылыста көміртектің тотығу дәрежесі -4
а) CO2ә) CClб) CH4в) H2CO3
13. Қай процесс тотығуға жатады:
а) S-2S+4ә) Mg0 Mg+2б) S+6 S+4в) S+4 S0
14. Қай процесс тотықсыздануға жатады:
а) N0 N-3ә) N-1 N0б) N-3 N+2в) N+5 N
15. Химиялық реакция теңдеуіндегі тотықсыздандырғыш формуласының коэффициенті қандай: Al + CuCl2 AlCl3 + Cu
а) 1; ә) 2; б) 3; в) 6.
16. Химиялық реакция теңдеуіндегі тотықтырғыштың алдындағы коэффициент қандай:
NO + O2 NO2
а) 6; ә) 3; б) 2; в)
ІІІ тарау. 3.1 Элементтепдің олардың жоғары оксидтері,гидроксидтері, сутекті қосылыстарының қасиеттерінің өзгеруінің периодтылығы.Оксидтердің жіктелуі, аталуы мен қасиеттері(§44-§47)
І-деңгей.
1. Оксидтер дегеніміз не?
2. Төмендегі оксидтерді атаңдар.
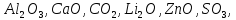
3. Мына негіздердің формуласын жазыңдар.
калий гидроксиді, кальций (ІІ) гидроксиді, мыс (ІІ) гидроксиді, темір (ІІІ) гидроксиді.
4. Қышқылдар дегеніміз не? Олар қалай жіктеледі?
5. Мына қышқылдардың формуласын жазыңдар:
азот қышқылы, күкірт қышқылы, хлорсутек қышқылы, күкірт сутек қышқылы, фосфор қышқылы
ІІ-деңгей.
1. Төмендегі қосылыстардың ішінен қышқылдарды теріп жазып, атаңдар. 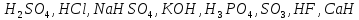
2. Мын теңдеулерді аяқтаңдар:
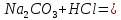
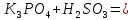
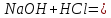
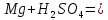
3. Мына тұздарды: мыс (ІІ) сульфаты, кальций (ІІ) хлориді алмасу реакциясының көмегімен алуға болатын реация теңдеулерін жазыңдар.
4. Мөлшері 0,1 моль барий хлориді қанша моль күкірт қышқылымен әрекеттесе алатынын есептеңдер.
ІІІ- деңгей
1. Массасы 12,6 г натрий сульфиті тұз қышқылымен әрекеттескенде неше моль натрий хлориді түзіледі?
2. Құрамында 9,8 г күкірт қышқылы бар ерітіндіні барий гидроксидінің артық мөлшерімен бейтараптағанда түзілетін тұздың массасын есептеңдер.
3. Массалық үлесі: 2,4 % H; 39,1% S; 58.5% O-тен тұратын заттың молекулалық формуласын табыңдар.
3.2. Химиялық реакциялар және олардың жүру заңдылықтарыХимиялық реакциялардың жіктелуі
| Сұрақ-жауап арқылы үй тапсырмасын тексеру
|
| Сұрақ-жауап арқылы үй тапсырмасын тексеру
|
| Сұрақ-жауап арқылы үй тапсырмасын тексеру
|
| Сұрақ-жауап арқылы үй тапсырмасын тексеру
|
3.3Химиялық реакциялар, жылу эффектісі
| Қосымша тапсырмалар: 1. Қандай реакция экзотермиялық деп аталады? 2. Қандай реакция эндотермиялық деп аталады? 3. Жылу эффектісі деген не? 4. Термохимиялық теңдеудің ерекшелігі неде? |
| Деңгейлік тапсырмалар: 2-тапсырма. S + O2 → SO2 + 296 кДж термохимиялық теңдеуі бойынша 1 кг күкірт жанғанда, қанша энергия бөлінеді? |
| 3-тапсырма: Егер реакцияның термохимиялық теңдеуі мынадай болса: 2Cu + O2 → 2CuO + 311кДж 6 моль мыс оттекпен әрекеттескенде қанша энергия бөлінеді? |
| 4-тапсырма: Массасы 1,2 г магнийді оттекте жаққанда, 30,1 кДж жылу бөлінді. Термохимиялық теңдеуін жазып, жылу эффектісін есептеңдер. |
3.4.Химиялық реакциалардың жылдамдығы. 3.5.Химиялық тепе-теңдік
| №2. Әрбір қайтымды реакциялар үшін тепе-теңдік константасының теңдеуін жазыңдар: а) 2H2(г) + O2(г) ↔ 2H2O(г); б) 2SO2(г) + O2(г) ↔ 2SO3(г); в) С(к) + СO2(г) ↔ 2СO(г); г) CaСO3(к) ↔ CaO(к) + СO2(г) |
| 1. Гомогенді және гетерогенді реакциялар дегеніміз не? Олардың айырмашылықтары қандай? 2. Гомогенді және гетерогенді реакциялардың жылдамдықтары дегеніміз не? 3. Гомогенді және гетерогенді реакцияларға әсер етуші қандай факторлар бар? 4. Химиялық кинетиканың негізгі заңы қалай аталады және қалай өрнектеледі? Гетерогенді реакция үшін кинетикалық теңдеудің қандай ерекшелігі бар? 5. Вант-Гофф ережесі қалай тұжырымдалады? Математикалық өрнегі қалай жазылады? 6. Катализ процесі дегеніміз не? Гомогенді және гетерогенді катализ теориялары қандай? 1. А + В → С гомогенді реакциясында А затының концентрациясы 10 сек өткеннен соң 0,020 моль/л-ден 0,015 моль/л-ге өзгерді. Химиялық реакцияның орташа жылдамдығын есептеңдер. (Жауабы: 0,0005 моль/л · с) 2. Химиялық реакция жылдамдығын 1500С-тан 2000С-қа арттырғанда реакция жылдамдығы неше есе артады? γ = 3. (Жауабы: 243 есе артады) |
ІІ тақырып. Химиялық реакция жүруінің негізгі заңдылықтары
Жұмыс 2. Химиялық реакцияның жылдамдығы. Химиялық тепе-теңдік.
І нұсқа
Химиялық реакцияның жылдамдығы әсер етуші заттардың табиғатына байланысты екеніне нақты мысалдармен сипатта.
Реакцияның тепе-теңдігі қай жаққа ығысады?
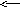
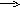 СО(r)+H2O(r) СО2(r) + H2(r)+Q
СО(r)+H2O(r) СО2(r) + H2(r)+Q
А) температураны жоғарылатқанда;
Б) көміртегі (ІІ)оксидін концентрациясын жоғарылатқанда. Негізгі жауабын бер
ІІ нұсқа
Химиялық реакцияның жылдамдығы әсер етуші заттың концентрациясына байланысты екеніне нақты мысалдармен сипатта.
А) температураның төмендеткенде;Б) Қысымды жоғарылатқанда
Реакцияның тепе-теңдігі қай жаққа ығысады?

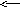
2H2(r) +O2 (r) 2H2O(r) +Q
Негізгі жауабын бер
ІІІ нұсқа
Химиялық реакцияның жылдамдығы температураға тәуелді екеніне нақты мысалдармен сипатта.
А) температураның төмендеткенде;Б) Қысымды төмендеткенде
Реакцияның тепе-теңдігі қай жаққа ығысады?

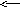
N2(r) +3H2 (r) 2NH3(r) +Q
Негізгі жауабын бер
ІІІ нұсқа
Химиялық реакцияның жылдамдығы катализаторларға тәуелді екеніне нақты мысалдармен сипатта.
А) температураның жоғарылатқанда;
Б) Бромсутектің концентрациясын жоғарылатқанда;
Реакцияның тепе-теңдігі қай жаққа ығысады?

2HBr(r) H2(r)+Br2(r)-Q Негізгі жауабын бер
111. тарау бойынша қорытынды тест сұрақтары
1.Химиялық элемент, бұл
А.жайзат В.молекула С.күрделі зат Д.ядрозаряды бірдей атом түрі Е.бос күйінде кездеседі
2.»Гидрогениум, оксигениум,карбонеум» латынша аталуына сәйкес келетін элементтердің таңбалары А).H, O, S В).O,H, Hg С).H, O, C Д).Hg, O, Si Е).Hg, O, C
3.Күрделі зат құрамындағы элементтердің массалық қатынасы 6,5:6болатын қосылыс
А.CrO В.Cr2O3 С.CrO3 Д.CrCI3 Е. CrCI2
4.Салыстырмалы молекулалық массасы 62-гетең қосылыс
А).күкірт қышқылы В).азот қышқылы С).тұз қышқылы Д.) көмір қышқылы Е).кремний қышқылы
5.Зат мөлшері 0,5моль болатын азот қышқылындағы молекулалар саны
А.6,02*1023 В.3,01*1023n С.6,02*1023 Д.3,01*1022 Е.30,1*1023
6.Молярлық (мольдік) масса, оның өлшем бірлігі
А.1 моль заттың массасы, моль В.1 моль заттың массасы, г/моль С.заттың Авогадро тұрақтысы әртүрлі, өлшем бірліксіз Д.газдарға тән емес, моль Е.газдарға тән, л/моль
7.Молярлық (мольдік) көлем, оның өлшем бірлігі
А.1 моль заттың массасы, мольВ.1моль заттың массасы, г/мольС.заттың Авогадро тұрақтысы әртүрлі, өлшем бірліксізД.газдарға тән емес, мольЕ.кез-келген 1 моль газдың алатын көлемі, л/моль
8.Авогадро тұрақтысы дегеніміз
А.кез-келген заттың 1 молінде 6,02*1023 молекула немесе атом болады
В. кез-келген заттың 1 молінде 6,02*1023 тек атом боладыС. кез-келген заттың 1 молінде 6,02*1023 тек молекула болады
Д. А.кез-келген заттың 1 молінде 6,02*1022 молекула немесе атом бар
Е. кез-келген заттың 1 молінде 6,02*1022 тек атом бар
9.Хром атомындағы протон, электрон, нейтрон саны
А.24,24,28В.24,28,24С.52,24,24Д.24,52,24Е.28,28,24
10.Массасы 49 г күкірт қышқылының зат мөлшері (мольмен)
А.1В.2С.0,5Д.0,1Е.0,2
11. Мөлшері 0,2 моль болатын азот қышқылындағы молекулалар саны
А.1,2*1023В.3,01*1023С.6,02*1023Д.2,4*1023Е.1,5*1023
12.Авогадро саны 1,505*1023 болатын көмір қышқылының массасы мен зат мөлшері
А.15,5г ; 0,25мольВ.62,1г; 1моль\ С.31г;0,5мольД.31г;0,25 мольЕ.62г;0,25моль
13.Массасы 71 г хлордың (қ.ж) алатын көлемі және зат мөлшері
А.22,4 және 0,5В.11,2 және1С.44,8 және2Д.44,8 және1Е.22,4 және1
14.Калий оксидіндегі калийдің массалық үлесі
А.82,64В.82,98С.81,21Д.80,91Е.79,33
15. Массасы 64 г мыспен (қыздырғанда) әрекеттесетін оттектің (қ.ж.) көлемі (литрмен)
А22,4В. 5,6С. 11,2Д.11,8Е.20,5
16.Зат массасының сақталу заңын ашқан ғалым
А. М.В.ЛомоносовВ. Д.И.МенделеевС. Ж.ПрустД. А.АвогадроЕ. А.Лавуазье
17.Заттың құрам тұрақтылық заңын ашқан ғалым
А. М.В.ЛомоносовВ. Д.И.МенделеевС. Ж.ПрустД. А.АвогадроЕ. А.Лавуазье
18.2Н2+О2 -- 2Н2О теңдеуіндегі әрекеттесуші реагенттердің (газдардың) көлемдік қатынастары
А. 2:1В1:2.С1:1Д.2:2.Е2:3.
19.Көлемдері бірдей, яғни 11,2 литр сутек пен хлор әрекеттескенде түзілетін хлорсутектің көлемі
А. 11,2В. 5,6С. 22,4Д. 24,2Е. 26,2
20. 11,2 литр сутек пен хлор әрекеттескенде түзілетін хлорсутектің көлемі (литрмен)
А.10,5 .В.22,4С.21,8Д.20,6Е.11,2
21. Мөлшері 0,2 моль темір мен 0,3 моль хлор әрекеттескенде түзілетін темір (ІІІ)хлоридінің массасы
А. 30,5В. 30,1С. 31,8Д. 32,5Е. 30,8
22.Массасы 42 г темір мен 12,8 г оттек әрекеттескенде түзілетін темір қағының (Fe3O4)
массасы
А. 40,1В. 46,4С.42,3Д.44,5Е.41,6
23.К2Сr2O7 қосылысындағы хромның тотығу дәрежесі
А.-6В.+12С.+1Д.+6Е.-2
24.CuCI2+Fe ---FeCI2+Cu
А.FeВ.CuС.CuCI2 Д.FeCI2 Е.CI
ІV тарау. 4.1.Металдармен бейметалдардың жалпы сипаттамасы
Сілтілік металл – натрий. Гаологендер(§65-§68)
І-деңгей.
1. Кестені толтырыңдар:
| Заттардың техникалық аталуы | Формуласы | Қолданылуы |
| 1. Күйдіргіш натр 2. Кальцийленген сода 3. Ас содасы 4.Глаубер тұзы |
|
|
2. Периодтық жүйедегі орнына сәйкес электрондық формуласын жазыңдар: хлор, натрий, фтор, бром
3. Хлордың физикалық қасиеттерін жазыңдар.
4. Хлорды кім ашты, қайда қолданады?
5. Галогендердің формуласын жазыңдар.
ІІ-деңгей.
1. Хлордың берілген заттармен реакция теңдеулерін жазыңдар:
а)натриймен, ә) кальциймен, б) алюминиймен, в) сутекпен
2. Хлорды алуға болатын реакция теңдеулерін жазып, оларды электрондық баланс әдісімен теңестіріңдер.
3. 30 г хлордың қалыпты жағдайдағы көлемін есептеңдер.
4. Реакция теңдеулерін аяқтаңдар:
а) 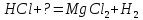
b) Cl2 + ? = HCl + HClO
c) Fe + Cl2 =
ІІІ-деңгей.
1. 40,5 г мыс хлоридін алу үшін қанша г хлор қажет?
2. 3 л сутек пен 2 л хлор газы (қ.ж) әрекеттескенде қанша л хлорсутек түзіледі?
3. Темір (ІІ) сульфидін алу үшін 28 г темір мен 22,4 г күкірт қосылды. Қай зат артық қалады және артық заттың массасы қандай? Түзілген темір (ІІ) сулфидінің неше грамы түзілетінін есептеңдер.
V тақырып. Металдардың жалпы қасиеттері. І-ІІІ топтағы негізгі топшадағы металдар. 1. Металдарды алу әдістері
І нұсқа
Мыс (І) оксиді менмыс (ІІ) оксидінен мысты көмірмен тотықсыздандырудың реакция теңдеулерін жазыңдар. Элементтердің тотығу дәрежесін белгілеңдер және тотықтырғыш пен тотықсыздандырғышты көрсетіңдер
Алюминді-термиялық әдіспен, 5% қоспасы бар, 90 г. марганец (ІV) оксидін тотықсыздандырған кезде қанша масса марганец алуға болады?
ІІ нұсқа
Алюминдітеримиялық әдіспен хром (ІІІ) оксидінен хромды алу реакция теңдеулерін жазыңдар. Элементтердің тотығу дәрежесін белгілеңдер және тотықтырғыш пен тотықсыздандырғышты көрсетіңдер.
Егер шығымның массалық үлесі 90% болса, 960 г. темір (ІІІ) оксидін көмір (ІІ) оксидімен тотықсыздандыру кезінде қанша масса темір алуға болады?
ІІІ нұсқа
Көміртегі (ІІ) оксидімен тотықсыздану реакция теңдеулерін жазыңдар: А) қорғасынды оның жоғарғы оксидінен; Б) мысты оның мыс (ІІ) оксидінен Элементтердің тотығу дәрежесін белгілеңдер және тотықтырғыш пен тотықсыздандырғышты көрсетіңдер
Алюминдітеримиялық әдіспен 52 г. хромды алу үшін, 10% қоспасы бар, хром (ІІІ) оксидінің қанша массасы қажет?
ІVнұсқа
Молибденді оның жоғарғы оксидінен сутегімен тотықсыздандыру жолымен алудың реакция теңдеулерін құраңдар. Элементтердің тотығу дәрежесін белгілеңдер және тотықтырғыш пен тотықсыздандырғышты көрсетіңдер.
Егер мыстың шығымының массалық үлесі 85% құрайтын болса, 160 г. мыс (ІІ) оксидін көмірментотықсыздандыру кезінде қанша масса мыс алуға болады?
Металдардың химиялық қасиеттері.
І нұсқа
Әрекеттесу реакция теңдеулерін құраңдар: А) натрийдің күкіртпен; Б) темірдің күкірт қышқылының ерітіндісімен; В) алюминийдің броммен. (А) реакция теңдеуінен элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар.
Қандай заттар арасында химиялық реакциялар жүреді: А) мыс және темір (ІІ) сульфатының ерітіндісімен; Б) мырыш пен сынап (ІІ) нитратымен; В) магний мен қорғасын (ІІ) нитратының ерітіндісімен? Сәйкес реакция теңдеулерін молекулалық және қысқаша иондық түрде жазыңдар
ІІ нұсқа
Әрекеттесу реакция теңдеулерін құраңдар: А) мыстың оттегімен; Б) темірдің хлормен; В) барийдің сумен. (А) реакция теңдеуінен элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар.
Қандай заттар арасында химиялық реакциялар жүреді: А) мыс және күміс сульфатының ерітіндісімен; Б) темір мен сынап (ІІ) нитратымен; В) қорғасын мен хром (ІІ) хлоридінің ерітіндісімен? Сәйкес реакция теңдеулерін молекулалық және қысқаша иондық түрде жазыңдар
ІІІ нұсқа
Әрекеттесу реакция теңдеулерін құраңдар: А) алюминидің иодпен; Б) мыстың күкіртпен; В) натрийдің сумен. (А) реакция теңдеуінен элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар.
Қандай заттар арасында химиялық реакциялар жүреді: А) темірдің мыс (ІІ) хлоридінің ерітіндісімен; Б) күміс және кальций бромидінің ерітіндісі; В) алюминий және қорғасын (ІІ) нитратының ерітіндісімен? Сәйкес реакция теңдеулерін молекулалық және қысқаша иондық түрде жазыңдар
ІVнұсқа
Әрекеттесу реакция теңдеулерін құраңдар: А) магнийдің тұз қышқылымен ; Б) мырыштың оттегімен; В) кальцийдің хлормен. (А) реакция теңдеуінен элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар.
Қандай заттар арасында химиялық реакциялар жүреді: А) магний және сынап (ІІ) нитратының ерітіндісімен; Б) мыс және хлор(ІІ) хлоридінің ерітіндісі; В) мырыш пен темір (ІІ) сульфа тының ерітіндісімен? Сәйкес реакция теңдеулерін молекулалық және қысқаша иондық түрде жазыңдар
. Электролиз. Металдардың коррозиясы.
І нұсқа
Электролиз кезінде жүретін реакция теңдеулері мен схемасын құраңдар: А) калий хлоридінің балқымасы;
Б) мырыш бромидінің ерітіндісі.
Коррозия дегеніміз не? Металдардың жемірілуін баяулататын қандай факторлар қолданылады?
ІІ нұсқа
1. Электролиз кезінде жүретін реакция теңдеулері мен схемасын құраңдар:
А) натрий иодидінің ерітіндісі;
Б) мыс хлоридінің ерітіндісі.
2. Қандай жемірілудің түрлерін білесіңдер?
ІІІ нұсқа
Электролиз кезінде жүретін реакция теңдеулері мен схемасын құраңдар:
А) калий бромидінің ерітіндісі;
Б) кальций хлоридінің ерітіндісі.
Жемірілуді тездетуге қандай факторлар әсер етеді?
Электролит қатысында қарым-қатынастағы қай металл бұрын бүлінеді: мыс және мырыш; алюминий және темір? Неге?
ІVнұсқа
1. Электролиз кезінде жүретін реакция теңдеулері мен схемасын құраңдар:
А) натрий хлоридінің балқымасы;
Б) темір (ІІ) бромидінің ерітіндісі.
2. Металдың жемірілуіне қарсы күрестің әдістерін тізіңдер
3. Неге мырышпен қапталған бакта сызылған жерлердегі мырыш бүлінеді, ал темір тоттанбайды?
Сілтілік және сілтілік жер металдар
І нұсқа
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Са→ CаO→СaCO3→Сa (HCO3)2
Сілтілік металдар бейметалдармен әрекеттескен кезде тотығу және тотықсыздану қасиетін көрсете ме? Жауапты дәлелдейтін екі реакция теңдеуін жазыңдар
20 г. калий гидроксидіне 25 г. азот қышқылы бар ерітіндіні әсер етті. Қанша масса тұз түзілді?
ІІ нұсқа
Әрекеттесетін реакция теңдеулерін жазыңдар: А) натрийдің күкіртпен; Б) кальцийдің хлормен; В) литийдің сумен
Неге әк суы ауада лайланады, ал калий гидроксидінің тұзы – жоқ? Барий гидроксидінің ерітіндісі ауада көп тұрса лайланады ма? Жауабын сәйкес келетін реакция теңдеулерімен дәлелдеңдер
8% қоспасы бар,1 кг. әктасты күйдірген кезде қанша масса кальций оксидін алуға болады?
ІІІ нұсқа
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Na→NaОН→NaHCO3→Na2SO4
Судың кермектілігі деген не және сендерге олардың қандай түрлері белгілі? Оны жойдыратын екі реакция теңдеулерін жазыңдар
11,5 г. натрийге 78 г. су әсер етті.Түзілген натрий гидроксидінің массасын есептеңдер
ІVнұсқа
Көрсетілген заттардың қайсысында натрий гидроксиді әсер етеді: тұз қышқылы, магний оксиді, кальций гидроксиді; көміртегі (ІV) оксиді, күкірт қышқылы? Орындалатын реакция теңдеулерін жазыңдар
Мәрмәр мен су сенде бар болса, онда әк суын қалай дайындайды? Реакция теңдеулерін жазыңдар
6,9 г. натрий сумен әрекеттескен кезде (қ.ж.) 3 л. сутегі алынды. Газ шығынының көлемдік үлесін есептеңдер
1V тарау бойынша тест тапсырмалары
Сілтілік металдарға жататын элементтер:а) Naә)Alб)Caв)Li
Ең белсенді элемент:а) Kә)Naб)Liв)Cs
Қалыпты жағдайда сумен әрекеттеседіа) Alә)Cuб)Naв)Li
Натрийді:а) керосинніңә) судыңб) құмныңв) вазелиннің астында сақтайды.
Қыздырғанда ыдырамайтын заттар:а) Cu(OH)2ә) NaOHб) Fe(OH)в) Cr(OH)
Натрий гидроксидімен әрекеттесетін заттар:а) H2Oә) CuCl2б) O2в)HCl
Сызбанұсқа бойынша реакция теңдеулерін жазып, А затының формуласын табыңдар: Na A NaOHа) NaClә) Na2Oб) Na2SO4в) NaF
Берілген айналуларға сәйкес келетін реакция теңдеулерін жазып, х затын табыңдар: H2 x NaBr а)Naә)NaClб)Br2в)HBr
Қай галоген ең белсенді тотықтырғыш болып саналады:а) Fә)Brб)Iв)Cl
Қай тотығу дәрежесі барлық галогендерге сәйкес келеді:а) +7ә) -1б) +5в) 1
NaBr қосылысындағы химиялық байланыс _________________ , химиялық байланысы________________ , кристалдық торы_____________________
Хлор молекуласының формуласы___________________ , химиялық байланысы _______________, кристалдық торы_____________________
Табиғатта хлор:а)жай заттыңә) тұздыңб) қышқылдыңв) оксидтердің құрамында кездеседі.
14. Хлор табиғатта кең таралған қаттардың құрамында кездеседіа) NaClә) HClб) KClв)Cl2
15. Хлор әрекеттесуі мүмкін:а) N2ә) O2б) HNO3в) H2O
16. Хлор әрекеттесуі мүмкін:а) O2ә)H2б) H2SO4в)HCl
17. Лабораторияда хлорсутекті алу:
а) NaCl (қатты) + H2SO4ә) H2O + Cl2б) NaCl(ер-ді) + H2SO4(сұйық) в) NaCl(қатты) + H2SO4(конц)
18. Реакция жүруі мүмкін:а) NaCl + Br2 ә) MABr + I2б) NaI + Cl2в) NaF + Cl2
19. 8л хлор (қ .ж) және 10 л сутектен тұратын қоспа жарылды. Алынған хлорсутектің көлемі:а) 5,6 лә) 8 лб) 11,2 лв) 16 л
20. 5,85 натрий хлоридін концентрлі күкірт қышқылымен әрекеттестіргенде түзілген (қ.ж) хлорсутектің көлемі:а) 2,24лә) 4,48лб) 22,4лв) 44,
V тарау. Күкірт. Күкірт қышқылы
І нұсқа
Әрекеттесетін реакция теңдеуін жазыңдар:
А) күкірттің оттегімен
Б) күкірттің литиймен (элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар)
В) күкірт қышқылының ерітіндісі магниймен
Г ) күкірт қышқылының ерітіндісі кальций оксидімен
Д) күкірт қышқылының ерітіндісі барий гидроксидімен (молекулалық және иондық формада)
2. Оттегі мен азонның молекулалық құрылысы мен қасиетін салыстырыңдар. Аллотропияның бар екенін түсіндіріңдер.
3. Пробирканың біреуінде натрий сульфатының ерітіндісі бар, ал екіншісінде күкірт қышқылының ерітіндісі бар. Қандай тәжірибелік жолмен оларды табуға болады. Сәйкес келетін реакция теңдеуін жазыңдар.
ІІ нұсқа
Әрекеттесетін реакция теңдеуін жазыңдар:
А) күкірттің алюминиймен Б) күкірттің көміртегімен (элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар)
В) күкірт қышқылының ерітіндісі мырышпен
Г ) күкірт қышқылының ерітіндісі магний оксидімен
Д) күкірт қышқылының ерітіндісі мысгидроксидімен (молекулалық және иондық формада)
Табиғатта күкірт қандай түрінде кездеседі? Оны қолданудың негізі облысын сипаттаңдар
Пробирканың біреуінде күкірт қышқылы бар, ал екіншісінде тұз қышқылы. Қандай тәжірибелік жолмен оларды табуға болады. Сәйкес келетін реакция теңдеуін жазыңдар.
ІІІ нұсқа
Әрекеттесетін реакция теңдеуін жазыңдар:
А) күкірттің сутегімен
Б) күкірттің мырышпен(элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар)
В) күкірт қышқылының ерітіндісі темірмен
Г ) күкірт қышқылының ерітіндісі мыс (ІІ) оксидімен
Д) күкірт қышқылының ерітіндісі натрий гидроксидімен (молекулалық және иондық формада)
Оттегі мен күкірт-химиялық элементтерін, түзетін жай заттардың атауларын жазыңдар. Бұл құбылысты түсіндір.
Пробирканың біреуінде калий сульфаты бар, ал екіншісінде тұз қышқылы. Қандай тәжірибелік жолмен оларды табуға болады. Сәйкес келетін реакция теңдеуін жазыңдар.
ІVнұсқа
Әрекеттесетін реакция теңдеуін жазыңдар:
А) күкірттің натриймен
Б) күкірттің фтормен (элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар)
В) күкірт қышқылының ерітіндісі алюминиймен
Г ) күкірт қышқылының ерітіндісі темір (ІІІ) оксидімен
Д) күкірт қышқылының ерітіндісі кальций гидроксидімен (молекулалық және иондық формада)
Күкірт қышқылының өнеркәсіпте және ауылшаруашылығында қолданылуының негізгі облысын сипаттаңдар.
Пробирканың біреуінде натрий хлоридінің ерітіндісі, ал екіншісінде натрий сульфаты бар. Қандай тәжірибелік жолмен оларды табуға болады. Сәйкес келетін реакция теңдеуін жазыңдар.
ІІ тақырып бойынша қорытындылау
І нұсқа
Төменде келтірілген заттардың қайсысына күкірт қышқылы әсер етеді?: калий гидроксиді; алюминий, күкірт (ІV) оксиді; темір (ІІ) оксиді; барий нитраты; мыс, мырыш гидроксиді? Орындалатын рекция теңдеулерін жазыңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
S→SO2→SO3→H2SO4→SO2
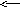

2SO2(r)+O2 (r)2SO3(r)+O2
А) температураны жоғарылатқанда;Б) қысымды төмендеткенде;
Реакцияның тепе-теңдігі қай жаққа ығысады? Негізгі жауабын бер
Күкіртқышқылды зауытта пиритті жаққанда реакцияның жылдамдығының артуы қандай әдіспен қолжетімді болады?
ІІ нұсқа
Төменде келтірілген заттардың қайсысына күкірт қышқылы әсер етеді?: Сынап, темір (ІІІ) гидроксиді; барий хлориді; литий гидроксиді ; магний оксиді; мырыш, көміртегі (ІV) оксиді? Орындалатын рекция теңдеулерін жазыңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
H2S→S→ FeS→ SO2
↓
Na2S
Химиялық реакцияның жылдамдығы неге тәуелді?
А) температураға;
Б) Әсер етуші заттардың концентрациясына
Мысал келтіріңдер
Күкіртқышқылды зауытта қандай үрдіс жылу алмасу принципінің қолданылуына негізделген. Осы принциптің қолдануына не жеткізеді?
ІІІ нұсқа
Төменде келтірілген заттардың қайсысына күкірт қышқылы әсер етеді?: натрий гидроксиді ; алтын, мыс (ІІ) оксиді; магний , барий хлориді; күміс, алюминий гидроксиді? Орындалатын рекция теңдеулерін жазыңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
S→ZnS→ SO2→ SO3→H2 SO4
Химиялық реакцияның жылдамдығы неге тәуелді?
А) катализатордан;
Б) әсер етуші заттардың табиғатына;
Мысал келтіріңдер
Неге көмірқышқылды зауытта күкірт (ІV) оксидін тазартуға көп мән береді?
ІVнұсқа
1. Төменде келтірілген заттардың қайсысына күкірт қышқылының ерітіндісі әсер етеді?: мыс, кальций гидроксиді ; мырыш оксиді; темір, кремний (ІV) оксиді; барий нитраты; мыс (ІІ) гидроксиді? Орындалатын рекция теңдеулерін жазыңдар
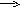
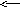 2. SO2(r) + H2O (c) H2 SO3(с) + Q
2. SO2(r) + H2O (c) H2 SO3(с) + Q
А) температураны жоғарылатқаннан;
Б) күкірт (ІV) оксидінің концентрациясын жоғарылатқанда;
Реакцияның тепе-теңдігі қай жаққа ығысады? Негізгі жауабын бер
3. Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
H2S←S→ SO2→ SO3
Al2S3
Негі күкірт қышқылыды зауытта күкірт (ІV) оксидін сумен емес, концентрлі күкірт қышқылымен сіңдіреді?
YI тарау. ІІІ тақырып. Азот топшасы.
Жұмыс 1. Азот. Аммиак. Аммоний тұздары
І нұсқа
Реакция теңдеулерін жазыңдар:
А) азоттың литиймен әрекеттесуі ( элементтердің тотығу дәрежесін белгілеңдер және тотығу мен тотықсыздануды көрсетіңдер);
Б) аллюминий тұзынан аммиакты алу;
В) аммоний хлоридінің ерітіндісі мен күміс нитратының ерітіндісімен әрекеттесуін (молекулалық және иондық түрде)
2. Сутегі, хлор және азот арқылы аммоний хлорын қалай алады? Реакция теңдеуін жазыңдар.
3. Азот молекуласының молекулалық , электрондық және құрылымдық формуласын бейнелеңдер. Азоттың физикалық қасиетін көрсетіңдер
ІІ нұсқа
1. Реакция теңдеулерін жазыңдар:
А) азоттың сутегімен әрекеттесуі ( элементтердің тотығу дәрежесін белгілеңдер және тотығу мен тотықсыздануды көрсетіңдер) ;
Б) аммиактың күкірт қышқылымен әрекеттесуі;
В) аммоний сульфатының ерітіндісі мен барий нитратының ерітіндісімен әрекеттесуін (молекулалық және иондық түрде)
Үш номерленген пробиркаларға күкірт қышқылы, натрний сульфаты және аммоний хлоридінің ерітінділері бар. Қандай тәжірибелік жолмен оларды табуға болады? Сәйкес келетін реакция теңдеулерін жазыңдар
Аммоний ионының түзілу схемасын бейнелеңдер. Азот пен сутегі арасындағы химиялық байланыстың түрін, тотығу дәрежесін және аммиактағы мен аммоний ионындағы азоттың валенттілігін көрсетіңдер
ІІІ нұсқа
1. Реакция теңдеулерін жазыңдар:
А) азоттың магниймен әрекеттесуі ( элементтердің тотығу дәрежесін белгілеңдер және тотығу мен тотықсыздануды көрсетіңдер) ;
Б) аммиактың оттегінде жануын;
В) аммоний карбонатының ерітіндісі мен азот қышқылының ерітіндісімен әрекеттесуін (молекулалық және иондық түрде)
2. Азот, сутегі, күкірт (ІV) оксиді және су арқылы аммоний сульфатын қалай алуға болады? Реакция теңдеуін жазыңдар
3. Азот молекуласының түзілуінің схемасын бейнелеңдер. Азот атомдары арасындағы химиялық байланыстың түрін және тотығу дәрежесін көрсетіңдер
ІVнұсқа
1. Реакция теңдеулерін жазыңдар:
А) азоттың оттегімен әрекеттесуі ( элементтердің тотығу дәрежесін белгілеңдер және тотығу мен тотықсыздануды көрсетіңдер) ;
Б) аммиактың хлорсутекпен әрекеттесуін;
В) аммоний сульфатының ерітіндісі мен барий гидроксидінің ерітіндісімен әрекеттесуін (молекулалық және иондық түрде)
2. Үш номерленген пробиркаларда кристалдық заттар бар: аммоний хлориді; аммоний сульфаты; натрий хлориді. Қандай тәжірибелік жолмен оларды табуға болады? Сәйкес келетін реакция теңдеулерін жазыңдар.
3. Аммиактың молекулалық, эхлектрондық және құрылымдық формулаларын бейнелеңдер. Аммиактың физикалық қасиетін көрсетіңдер.
Азот қышқылы және оның тұздары
І нұсқа
Азот қышқылының ерітіндісімен:
А) кальций оксиді; Б) натрий гидроксиді; В) калий карбонаты арасындағы молекулалық және иондық реакция теңдеулерін жазыңдар.
2. Концентрлі азот қышқылы мен мыстың әрекеттесуінің реакция теңдеуін құраңдар. Элементтердің тотығу дәрежесін көрсетіңдержәне электрондық баланс әдісімен коэффиценттерін қойыңдар.
3. Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
N2→ NO→NO2→НNO3
ІІ нұсқа
Азот қышқылының ерітіндісімен:
А) кальций гидроксиді; Б) мыс (ІІ)оксиді; В) барий карбонаты арасындағы молекулалық және иондық реакция теңдеулерін жазыңдар.
2. Қорғасын нитратын қыздырған кезде айырылу реакция теңдеулерін жазыңдар. Элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар.
3. Үш номерленген пробиркаларда кристалды заттар бар: натрий нитраты; натрий сульфаты және аммоний нитраты. Қандай тәжірибелік жолмен оларды табуға болады? Сәйкес келетін реакция теңдеулерін жазыңдар.
ІІІ нұсқа
1. Азот қышқылының ерітіндісімен:
А) калий гидроксиді; Б) натрий оксиді; В) натрий карбонаты арасындағы молекулалық және иондық реакция теңдеулерін жазыңдар.
2. концентрлі азот қышқылы мен сынаптың әрекеттесу реакция теңдеулерін жазыңдар. Элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар.
3. Келесі өзгерісті орындайтын реакция теңдеулерін жазыңдар:
KNO3→HNO3→Cu(NO3)2→NO2
ІVнұсқа
1.Азот қышқылының ерітіндісімен:
А) барий гидроксиді; Б) магний оксиді; В) кальций карбонаты арасындағы молекулалық және иондық реакция теңдеулерін жазыңдар.
2. Күміс нитратының қыздыру кезіндегі айырылу реакция теңдеулерін жазыңдар. Элементтердің тотығу дәрежесін көрсетіңдер және электрондық баланс әдісімен коэффиценттерін қойыңдар.
3. Үш номерленген пробиркаларда азот, күкірт және тұз қышқылдары бар. Қандай тәжірибелік жолмен оларды табуға болады? Сәйкес келетін реакция теңдеулерін жазыңдар.
YII тарау. Фосфор және оның қосылыстары
І нұсқа
Әрекеттесі реакция теңдеулерін жазыңдар: А) фосфордың оттегімен; Б) фосфиннің (РН3) хлорсутегімен; В) фосфор қышқылының ерітіндісі мен калий гидроксиді (молекулалық және иондық түрде)
Қызыл және ақ фосфор бір элементтің аллотропиялық түр өзгерісі болып табылатынын қалай дәлелдейсіңдер?
Үш номерленген пробиркаларда фосфор және тұз қышқылдары, натрий фосфаты ерітінділері бар. Қандай тәжірибелік жолмен оларды табуға болады? Сәйкес келетін реакция теңдеулерін жазыңдар.
ІІ нұсқа
Әрекеттесі реакция теңдеулерін жазыңдар: А) фосфордың хлормен; Б) фосфордың магниймен; В) натрий фосфатының ерітіндісі мен күміс нитратының ерітіндісі (молекулалық және иондық түрде)
Неге фосфор табиғатта тек қосылыс түрінде кездеседі, ал бір топта орналасқан азот – бос күйінде кездеседі?
Келесі өзгерісті орындайтын реакция теңдеулерін жазыңдар:
+Н2О
Р→Са3Р2→ РН3→ Р2О5
ІІІ нұсқа
Әрекеттесі реакция теңдеулерін жазыңдар: А) фосфордың кальциймен; Б) калий фосфаты мен күкірт қышқылын қыздыру арқылы; В) натрий гидроксидінің ерітіндісі мен фосфор қышқылының ерітіндісі (молекулалық және иондық түрде)
Бірдей жағдайда ақ және қызыл фосфорды жаққан кезде бірдей немесе әртүрлі қосылыс алына ма?
Үш номерленген пробиркаларда фосфор және азотқышқылдары, су бар. Қандай тәжірибелік жолмен оларды табуға болады? Сәйкес келетін реакция теңдеулерін жазыңдар
ІVнұсқа
Әрекеттесі реакция теңдеулерін жазыңдар: А) фосфордың күкіртпен; Б) фосфор (V) оксиді сумен; В) натрий карбонатының ерітіндісі мен фосфор қышқылының ерітіндісі (молекулалық және иондық түрде)
Құрамы бойынша фосфор молекуласы (буда) азо молекуласынан қандай айырмашылығы бар?
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Р→Р2О5→ Н3РО4→ К3РО4
Реакцияның өкімінің шығымы теорилықпен салыстырғандағы массалық және көлемдік үлестерін анықтау бойынша есептеулер
Керекті мөлшерде алынған натрий гидроксидіне 252 г. азот қышқылы бар ерітіндіс әсер етті. Алынған тұздың массасын есептеңдер, егер практикалық шығымы теориямен салыстырғанда 90 % болса
20 г. аммоний хлориді мен кальций гидроксидінің артық мөлшерін қыздырғанда алынған аммиактың (қ.ж.) көлемін есептеңдер, егер аммиактың көлемдік үлесінің шығымы 98% болса
280 г. кальций оксидінен 358 г. кальций гидроксидін алды. Кальций гидроксидінің массалық үлесінің шығымын есептеңдер.
20 г. аммоний хлориді мен 20 г. кальций оксидінің қоспасын қыздырғанда алынған аммиактың массасы қандай? Массалық үлесінің шығымы 98% құрайды
Аммоний нитратын NH4NO2қыздырған кезде азот пен су төзімді. Егер азоттың көлемдік үлесінің шығымы 0,89 болғандығы, 6,4 г. аммоний нитритін айырған кезде алуға болатын азоттың (қ.ж.) көлемін есептеңдер.
Көлемі 56 л.(қ.ж.) азотқа артық мөлшерде алынған сутегімен әсер етті. Аммиактың массалық үлесінің шығымы 50 % құрайды. Алынған аммиактың көлемін және массасын есептеңдер.
107 г. аммоний хлоридін айырған кезде (қ.ж.) 38 л. аммиак алынды. Аммиактың көлемдік үлесінің шығымын есептеңдер.
200 кг. фосфор қышқылын алу үшін фосфордың қанша массасы қажет? Егер қышқылдың массалық үлесінің шығымы 90 % құрайтын болса
33г. аммоний сульфаты мен артық мөлшерде алынған кальций гидроксидінің қоспасын қыздыру арқылы қанша көлем (қ.ж.) аммиак алуға болады? Егер көлемдік үлесінің шығымы 85% құраса
4 л. (қ.ж.) азот (ІV) оксидін алу үшін артық мөлшерде концентрлі азот қышқылымен реакциялауға қанша масса мыс қажет екенін есепте.Егер азот(ІV) оксидінің көлемдік мөлшерінің шығымы 96% құрайтын болса
30 г. аммоний хлоридін артық мөлшерде кальций гидроксидімен қыздырған кезде алынатын аммиактың (қ.ж.) көлемін есептеңдер. Аммиактың көлемдік мөлшерінің шығымы 94% құрайтын болса
40 г. аммоний нитратын айырған алынатын азоттың (І) оксидінің (қ.ж.) көлемін есептеңдер, егер оның көлемдік мөлшерінің шығымы 96% құрайтын болса
20,2 г. калий нитратына концентрлі күкір қышқылын әрекеттестірген кезде алынатын азот қышқылының массасын есептеңдер, егер қышқылыдың шығымының масалық үлесі 0,98 болса
80 г. калий фосфатына концентрлі күкірт қышқылы әрекеттестірген кезде алынатын фосфор қышқылының массасын есептеңдер, егер қышқылыдың шығымының масалық үлесі 0,96 болса
тақырып бойынша қорытындылау
І нұсқа
Молекулалық азот пен ақ фосфорға салыстырмалы сипаттама беріңдер, ұқсастығы мен айырмашылығын көрсетіңдер: А) агрегаттың күйі бойынша; Б) химиялық қасиеті бойынша; В) реакциялық қабілеті мен адам ағзасына әсері бойынша жауабын реакция теңдеуімен дәлелдеңдер.
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Р→Р2 О5→НРО3→Н3РО4→NaРО4→Ag3РО4
37 г. калий гидроксиді аммоний сульфатымен әрекеттесуінен 15 г. аммиак алынды. Аммиактың шығынының массалық үлесін есептеңдер
ІІ нұсқа
Азот пен фосфор элементтеріне салыстырмалы сипаттама беріңдер, ұқсастығы мен айырмашылығын көрсетіңдер: А) атом құрылысында; Б) тотығу дәрежесінде; В) олардан түзілген оксидтердің құрамы мен қасиетін. Жауабын реакция теңдеулерімен дәлелдеңдер
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
N2→NH3→NО→ NО2→H NО3→Ba(NО3) 2
17г. натрий нитратын концентрлі күкірт қышқылымен әрекеттестіру арқылы алынатын азот қышқылының массасын есептеңдер; егер қышқылыдың шығымының масалық үлесі 0,96 болса
ІІІ нұсқа
Азот пен фосфордың ұшқыш сутектік қосылыстарына салыстырмалы сипаттама беріңдер, ұқсастығы мен айырмашылығын көрсетіңдер: молекулалық құрылысынан, физикалық және химиялық қасиетінен. Жауабын реакция теңдеулерімен дәлелдеңдер
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
P→Ca3 P2→ PH3→Р2О5→HРО3→H3РО4
30г. аммоний хлоридін артық мөлшерде кальций гидроксидінен қыздыру арқылы алынатын аммиактың (қ.ж.) көлемін есептеңдер, аммиактың шығымының көлемдік үлесі 0,92 болса
ІVнұсқа
1. Азот пен фосфордың қышқылына салыстырмалы сипаттама беріңдер, ұқсастығы мен айырмашылығын көрсетіңдер: молекулалық құрылысынан, физикалық және химиялық қасиетінен. Жауабын реакция теңдеулерімен дәлелдеңдер
2. Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Pb(NО3) 2→NO2→HN О3→NH4 NО3→ NH3→(NH4) 2SO4
3.62 г. фосфорды оттегінде жаққан кезде 130 г. фосфор (ІV) оксиді алынды, фосфор (ІV) оксидінің шығымының массалық үлесін есептеңдер
YIII тарау Көміртегі топшасы.
Көміртегі. Көміртегі оксиді
І нұсқа
Көміртегі атомының қалыпты және қозған күйдегі электрондық конфигурациясын бейнелеңдер. Неге көміртегі атомы үшін 2s22p2→ 2s12p3схемасы бойынша электронның ауысуы болады?
Реакция теңдеулерін жазыңдар: А) көмірдің мыс (ІІ) оксидімен әрекеттесуін;
Б) көмірдің көміртегі (ІV) оксидімен әрекеттесуін; В) өнеркәсіптік әдіспен әктастан көміртегі (ІV) оксидін алынуын.
5 % азоты бар, 20 л. көміртегі (ІІ) оксидін толық жандыру үшін қанша көлем қажет?
ІІ нұсқа
Табиғатта көміртегі қандай жай зат түрінде кездеседі? Физикалық қасиеттерін салыстырыңдар және кристалдық тордың құрылымына байланысты екенін түсіндіріңдер.
Реакция теңдеулерін жазыңдар: А) көміртегі (ІV) оксидінің әктас суымен әрекеттесуі; Б) көміртегінің сумен әрекеттесуі; В) көмірдің артық мөлшеріндегі оттегінде жануын
8 % карбонатсыз қоспалары бар, 60 г. мрамордың артық мөлшеріндегі азот қышқылымен әрекеттесуі арқылы алынатын көміртегі (ІV) оксидінің (қ.ж.) көлемі қанша?
ІІІ нұсқа
Көміртегі қосылыстарда қандай тотығу дәрежесін көрсетеді? Көміртегі атомының әртүрлә тотығу дәрежесінде болатын үш қосылысының формуласын жазыңдар.
Реакция теңдеулерін жазыңдар: А) көміртегі (ІІ) оксидінің темір (ІІ) оксидімен әрекеттесуін; Б) көмірдің алюминиймен әрекеттесуін; В) көміртегі (ІV) оксиді кальций оксидімен әрекеттесуі.
6% жанбайтын қоспасы бар. 400 г. көмірді жандырған кезде бөлінетін (қ.ж.) көміртегі (ІV) оксидінің көлемі қандай?
ІVнұсқа
Адсорбция мен десорбцияға анықтама беріңдер. Ағаш көмірінің адсорбциялық қасиеті адамдардың қандай практикалық жағдайларда қолданылады?
Реакция теңдеулерін жазыңдар: А) көміртегі (ІІ) оксидінің жануын; Б) көмірдің күкіртпен әрекеттесуін;В)зертханалық әдіспен мрамордан көміртегі (ІV) оксидінің алынуын;
10% карбонатты емес қоспалары бар, 500 г. әктастың термиялық ыдырауы кезінде бөлінетін көміртегі (ІV) оксидінің (қ.ж.)көлемі қандай?
Көмір қышқылы және оның тұздары
І нұсқа
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Ca(HCO3)2→ CaCO3→CO2→Na2 CO3→H2 CO3
Үш номерленген пробиркаларда калий хлориді, калий карбонаты, калий фосфатының ерітінділері бар. Қандай тәжірибелік жолмен оларды табуға болады? Сәйкес келетін реакция теңдеулерін жазыңдар.
Егер көмірқышқыл газын лакмусы бар күлгін түсті судан өткізсе, онда түсі қызыл түске боялады, ал қыздырған кезде бояу қайта күлгін түске боялады. Бұл құбылысты түсіндіріңдер
ІІ нұсқа
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
СО→CO2→КНCO3→К2CO3→CO2
Әк суынан көмірқышқыл газын көп өткізген кезде қандай өзгерістер байқалады? Сәйкес келетін реакция теңдеулерін жазыңдар
Натрий және калий карбонаттарының сулы ерітінділері қандай ортаны көрсетеді? Неге?
ІІІ нұсқа
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Ca(HCO3)2→ CaCO3→CO2→Na2 CO3→H2 CO3
Әктасты күйдірген кезде калий карбонаты ерітіндісінен қосалқы газдарды өткізе отырып, көмірқышқыл газын қосып алады. Қаныққан кейінгі алынған ерітіндіні қыздырады, сонда көмірқышқыл газынан ол босатады. Жүретін реакция теңдеулерін жазыңдар.
Қандай сапалық реакциялар арқылы көмірқышқылының тұзын тұз, күкірт және азот қышқылының тұздарынан айыруға болады?
ІVнұсқа
Келесі өзгерісті орындайтын реакция теңдеулерін жазыңдар:
C→ CO2→ H2 CO3→Na2 CO3→NaNO3
А) барий гидроксиді: Б) күкірт қышқылы; В) калий гидроксиді; Г) калий нитраты ерітінділеріне сода ерітіндісін қосты. Қандай
жағдайда реакция байқалады? Сәйкес келетін реакция теңдеулерін жазыңдар
Ас тұзға кальций карбонатын әсер еткенде сода алуға бола ма? Неге?
IX Жұмыс 3. Кремний және оның қосылыстары.
І нұсқа
Неге кремнийдің бейметалдық қасиеті көміртегіне қарағанда әлсіз екенін кремнийдің атом құрылысы арқылы түсіндіріңдер
Келесі өзгерісті орындайтын реакция теңдеулерін жазыңдар:
SiO2→ Si→ SiO2→Na SiO3
5% қоспасы бар, 160 г. магний силициді Mg2Si тұз қышқылыменәрекеттескен кезде түзілетін SiН4 силанның массасы қанша?
ІІ нұсқа
Калий силикаты мен натрий силикатының сулы ерітінділері реакцияның қандай ортасын көрсетеді? Неге?
Келесі өзгерісті орындайтын реакция теңдеулерін жазыңдар:
NaОН→Na2 SiO3→Н2 SiO3→ SiO2
10% қоспасы бар, 40 г. кремний (ІV) оксидін көмірмен тотықсыздандырған кезде кремнийдің қанша массасы алынады?
ІІІ нұсқа
Кремний қосылыстарда қандай тотығу дәрежесін көрсетеді? Кремний әр түрлі тотығу дәрежесін көрсететін қосылыстардың формулаларын жазыңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
+НCl
Si→Mg2Si→SiН4→ SiO2
10% қоспасы бар, 50 г. кремний (ІV) оксидін натрий гидроксидімен балқытқан кезде түзілген натрий силикатының массасы қанша?
ІVнұсқа
Кремний (ІV) оксиді қандай оксидтер тобына жатады? Неге? Жауабын реакция теңдеулерімен жазыңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Si→ SiO2 →К2 SiO3→ Н2 SiO3
5% қоспасы бар, 60 г. кремний магнийімен әрекеттескен кезде алынған Mg2Si магний силицидінің массасы қанша?
Қоспасы бар заттың белгілі массасы немесе көлемі бойынша реакция өнімінің масасын немесе көлемін есептеу
10% қоспасы бар, 600 г. әктасты термиялық ыдыратқан кезде алынған кальций оксидінің массасы қанша?
20% қоспасы бар, 200 г.әктасты термиялық ыдыратқан кезде алынған көмірқышқыл газының (қ.ж.) көлемін қанша?
5% қоспасы бар, 50 г. азоттан 8 г. аммиак алды. Аммиактың шығымының массалық үлесін есептеңдер
6% қоспасы бар, 400 г.әктасты күйдірген кезде түзілген сөндірілмеген әктің массасы қанша?
8% қоспасы бар, 500 г.әктасты күйдірген кезде түзілген сөндірілмеген әктің массасы мен көміртегі (ІV) оксидінің (қ.ж.) көлемін (м3) есептеңдер
10,8 г. сусыз натрий карбонаты артық мөлшерден азот қышқылымен әрекеттескен кезде 2,24л. (қ.ж.) көміртегі (ІV) оксидін алды. Натрий карбонатындағы қоспаның құрамын есепте
8 % жанбайтын қоспасы бар, 500 г. көмірді жаққан кезде (қ.ж.) көміртегі (ІV) оксидінің қанша көлемі бөлінеді?
187,5 көмір жанған кезде (қ.ж.)336 л. көміртегі (ІV) оксиді түзілді. Көмірдегі көміртектің массалық үлесін есептеңдер
(қ.ж.)5% қоспасы бар, 0,6 кг. әктасты ыдыратқан кезде алынатын көміртегі (ІV) оксидінің зат мөлшерін (моль) және көлемін (л) анықтаңдар
Кальций гидроксидінің ерітіндісімен 2 м3 ауаны (қ.ж.) өткізген кезде 3 г. кальций карбонаты түзілді. Ауадағы көміртегі (ІV) оксидінің көлемдік үлесін есептеңдер
3% қоспасы бар, 80 г. барий карбонатын ыдыратқан кезде түзілген барий карбонатын ыдыратқан кезде түзілген барий оксидінің зат мөлшерін (моль) және массасын есепте
95% кальций карбонаты бар, 60 г. әктасты артық мөлшердегі тұз қышқылымен әрекеттескен кезде алынатын көміртегі (ІV) оксидінің (қ.ж.) көлемі мен зат мөлшері (моль) қанша?
54 г. әктасты күйдірген кезде 22 г. массасын жоғалтты. Әктастағы кальций карбонатының массалық үлесін есептеңдер. (әктаста кальций карбонатынан басқа ыдырамайтын заттар бар)
5% қоспасы бар, 60 г. кремний (ІV) оксидін көмірмен тотықсыздандырған кезде қанша масса кремний түзілді?
тақырып бойынша қорытындылау
І нұсқа
Көміртегі (ІV) оксиді мен кремний (ІV) оксидіне салыстырмалы сипаттама беріңдер. Құрамы, физикалық және химиялық қасиеттері бойынша ұқсастықтары мен айырмашылықты көрсетіңдер. Жауапты қажетті реакция теңдеулерімен дәлелдеңдер
Төменде көрсетілген заттардың қайсысымен көміртегі (ІІ) оксидін көмірқышқыл газының қоспасынан тазартуға болады: фосфор (V) оксиді, әк суы, күкірт қышқылының ерітіндісі, натрий гидроксидінің ерітіндісі? Болатын реакция теңдеуін жазыңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
NaCO3→ Ca CO3→CO2→ Ca(HCO3)2→CO2
6% қоспасы бар,400 г. кальций карбонатын ыдыратқан кезде (қ.ж.) қанша көлем көміртегі (ІV) оксидін алуға болады?
ІІ нұсқа
Кремний және көмірқышқылдарына салыстырмалы сипаттама беріңдер. Құрамы, физикалық және химиялық қасиеттері бойынша ұқсастықтары мен айырмашылықты көрсетіңдер. Жауапты қажетті реакция теңдеулерімен дәлелдеңдер
Ерітіндіде тұздар бар: натрий хлориді, калий сульфаты, кальций нитраты және магний сульфаты. Оған калий карбонатын құйды. Ақ тұнба түсті. Бұл тұнба нені көрсетеді? Жүретін реакция теңдеулерін жазыңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
CO2→ Na2CO3→Na HCO3 →CO2→ CaCO3
3% қоспасы бар, 30 г. кремний (ІV) оксидін магниймен тотықсыздандырған кезде қанша масса кремний түзілді?
ІІІ нұсқа
Кристалды кремний мен графитке салыстырмалы сипаттама беріңдер. Құрамы, физикалық және химиялық қасиеттері бойынша ұқсастықтары мен айырмашылықты көрсетіңдер. Жауапты қажетті реакция теңдеулерімен дәлелдеңдер
Бір пробиркада натрий карбонатының ерітіндісі, екіншісінде – натрий сульфатының ерітіндісі берілген. Әр пробиркаға барий хлоридінің ерітіндісін қосты. Екі жағдайда да ақ түсті, суда ерімейтін тұнба түзілді. Қай пробиркада натрий карбонатының ерітіндісі бар екенін көрсетіңдер? Сәйкес келетін реакция теңдеулерін жазыңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
CO2→ Сa2CO3→Сa (HCO3)2 → CaCO3→CO2
Артық мөлшердегі азот қышқылы 3% қоспасы бар, 20 г. кремний карбонатымен әрекеттескен кезде (қ.ж.) қанша көлем көміртегі (ІV) оксидін алуға болады?
ІVнұсқа
Көміртегі (ІІ) оксиді мен көміртегі (ІV) оксидіне салыстырмалы сипаттама беріңдер. Құрамы, физикалық және химиялық қасиеттері бойынша ұқсастықтары мен айырмашылықты көрсетіңдер. Жауапты қажетті реакция теңдеулерімен дәлелдеңдер
Үш номерленген пробиркаларда калий сульфаты, натрий силикаты және натрий карбонатының ерітінділері бар. Қандай бір зат арқылы әр пробиркадағы қосылысты анықтауға болады? Сәйкес келетін реакция теңдеулерін жазыңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
SiO2 →К2 SiO3→ Н2 SiO3→SiO2 →Si
5% қоспасы бар, 60 г. кремний жанған кезде қанша масса кремний (ІV) оксиді түзілуі керек?
Өндірістік және пәнаралық мазмұны бар тапсырмалар Бейметалдар
Кремнийді өнеркәсіпте доғалы электрлік пештерде кремнеземді кокспен тотықсыздандыру арқылы алады:
t
Si2O+2C= Si+2CO↑
Массасы 80 кг кокс арқылы тотықсыздандыру үшін қанша масса кремзем алуға болады, егер кокстағы көміртегінің массалық үлесі 92% болса. Жауабы: 184 кг.
Ақ фосфорды аппатит және фосфорит құрамында бар, кальций фосфатын кокспен тотықсыздандыру арқылы электрлік пештерде ауа қатысынсыз алады:
2Ca(PO4)2+10C+6SiO2= 6CaSiO3+10CO↑+P4↑
Фосфор буын су астында конденсирлейді. 248 кг. фосфор алу үшін құрамында көміртегінің массалық үлесі 90% болатын қанша масса кокс қажет? Бұл жағдайда өлшенген қ.ж. қанша көлем көміртегі (ІІ) оксиді бөлінеді? Жауабы: 266,7 кг.; 448 м3
Фосфор қышқылы теориялық әдіс арқылы алу мынамен қорытындыланады, алынған табиғи фосфаттардан фосфорды жағады, түзілген фосфор (V) оксидін сумен әрекеттестірген кезде H3PO4 береді, суммарлық реакция теңдеуі:
4P+5O2+6Н2O=4 H3PO4
400 кг. фосфор қышқылын алу үшін қанша масса фосфор қажет, егер фосфор қышқылының шығымының массалық үлесі 80 % болса. Жауабы: 158,2 кг.
Фосфор қышқылын алуының экстракционды әдіс негізінде табиғи фосфатты күкірт қышқылымен өңдеуді жатқызамыз: Ca3(PO4)2+3Н2SO4 = 3CaSO4+2 Н3PO4
Түзілген қышқылды кальций сульфатынан фильтрлейді және буландырумен концентрлейді: құрамында 60 % Ca3(PO4)2 бар, 200 кг фосфариттен қанша массафосфор қышқылын алуға болады? Шығымның массалық үлесі 80%. Жауабы: 60,7 кг.
Күкірт қышқылын көп уақыт бойы тек нитроздық әдіспен алды, оның негізі күкірт (ІV) оксидін азот (ІV) оксидімен су қатысында тотықтыру арқылы алумен қорытындыланады:
SO2+NO2+ Н2O= Н2 SO4+ NO↑
Осы әдіспен алынатын қышқылдың концентрациясы 75-76%, ондағы азот (ІV) оксиді бар болғандықтан оны қолдануды шектейді. Массалық үлесі 74 % (қыс.1,66 кг\л) болатын 100 л. күкірт қышқылы алынса, қанша масса күкірт (ІV) оксидін және суды әсер етті. Жауабы: 80,2 кг.; 22,6 кг.
Жолжелкеннің кептірілмеген жапырағында фосфордың массалық үлесі 0,38%, ал кептірілген жапырағында- 2,51 % құрайды. Жолжелкеннің жапырағын кептірген кезде суды жою нәтижесінде қанша пайыз массасын жоғалтады? Жауабы: 84%, 86%.
Металдар
Натрий гидроксидін әктасты әдіспен сода ерітіндісін Nа2СО3 сөнлірілген әктас Са(ОН)2 қыздыру кезінде алуға болады. 2 % қоспасы бар, қанша масса сода 10кг. натрий гидроксидін алу үшін қажет? Натрий гидроксидін қалай бөледі? Жауабы: 13,52 кг.
Табиғатта сынап HgS киноварь түрінде жиі кездеседі. Сынапты алу үшін киноварьді күйдіреді. Мұнда сынап пен күкірт (ІV) оксиді түзіледі. Сынап буын салқындататын қабылдағышта конденсирлейді. 10% қоспасы бар, 600 кг. киноварьді күйдіру кезінде қанша масса сынап түзіледі. Жауабы: 465,8 кг.
Адам күнделікті тамақпен 3 г. калий қоректенеді. Адамның калиймен тәуліктік қажеттілікті қамтамасыз етуге, құрамында 0,6% осы элемент бар, қанша масса картоп қажет. Жауабы: 500 кг.
Сатылым желісіне түскен ас тұзы құрамында натрий хлориді және қоспалар – су және ерімейтін қоспа бар. Натрийдің массалық үлесі 38%, тұздағы массаның массалық үлесі қандай? Таза натрий хлоридіндегі натрийдің массалық үлесі 39,3% құрайды. Жауабы: 3,31%
Техникалық марганецті алюмотермиялық әдіспен алуға болады:
3Mn3O4+8Al=9 Mn+ Al2 O3+250кДж
Егер реакцияға массасы 458 кг. Mn3O4 түскен болса, қанша масса марганец түзіледі және қанша жылу мөлшері бөлінеді? Жауабы: 330 кг.; 1666,7 кДж
Алтын мен күміс таза күйінде –жұмсақ металдар. Механикалық мықтылығын жоғарылату үшін оларды мыспен балқытады. Алтын немесе күміс бөліктер саны құйманың 1000 бөлігіне келсе, сынама дейді. Массасын есептеңдер: А) алтынның 750 сынамасында массасы 860 г.; Б) күмістің 750 сынамасында массасы 800 г. Жауабы: А) 645 г.; Б) 700 г.
Кальцинирленген сода шыны өндіріснде қолданылады. Натрий оксидінің массалық үлесі 17% бар, 1 т. шыны алу үшін қанша масса кальцинирленген сода қажет. Жауабы: 291 кг.
Натрий гидроксидінің көміртегі (ІV) оксидімен реакциясы практикалық маңыздылығы бар: 2Na2О2+2СО2=2Na2 СО3+ О2↑. Бұл реакция изомерленген орындарда ауаны регенерациялау үшін натрий гидроксидін (К2О4 пен) қолдануға негізделген. 2,5% қоспасы бар (қ.ж.) массасы 320 г. натрий пероксидімен қанша көлем көміртегі (ІV) оксиді реакцияға түседі? Мұнда қанша көлем оттегі бөлінеді? Жауабы: 89,6 л СО2; 44,8 л. О2
Кальций гидроксидінің массалық үлесі 86 % болса, массасы 60 кг.сөндірілген әктас өндіруге кальций карбонатының массалық үлесі 95% болса, қанша масса әктас жұмсалады? Жауабы: 73,4 кг.
Өздік жұмыс
Тапсырма: Қандай заттар өзара реакцияға түседі , егер берілген болса:
Ін.
Калий, күкірт қышқылы, темір (ІІІ) оксиді, фосфор (V) оксиді , натрий гидроксиді, мыс (ІІ) хлориді.
ІІ н.
1.Темір, тұз қышқылы, литий оксиді, күкірт (IV) оксиді, барий гидроксиді, қүміс нитратыТиісті реакция теңдеулерін жазыңдар.Түзілген заттарды және реакция типтерін атандар
І н.
Натрий гидроксидінің массалық үлесі 2% , көлемі 10 мл (тығыздығы 1,021г/см3 ) ерітіндісін бейтараптауға тұз қышқылының массалық үлесі 2% (тығыздығы 1,008г/см3 ) ерітіндісінің қанша көлемі қажет екенін табыңдар. Ж. 9 мл
ІІ н.
2.Көлемі 20 мл массалық үлесі 2 % , тығыздығы 1,02 г/мл натрий гидроксидінің ерітіндісін бейтараптауға күкірт қышқылының массалық үлесі 1 % , тығыздығы 1,01 г/мл ерітіндісінің қандай көлемі қажет болатынын есептендер Ж: 50 мл
І н .
Бір элементітің оксидінің формуласы ЭО2, ондағы оттектің массалық үлесі 53,3% . Элементті табыңдар.
ІІн
Бір элемент оттектің массалық үлесі 30,5% болатын оксид түзеді. Элементтің тотығу дәрежесі +4. Осы элементтің салыстырмалы атомдық массасын анықтап атын атандар
Ін.
Алюминий , оттек және сутек атомдары массалық қатынастары 9 : 16 : 1 болатын қосылыстың қарапайым формуласын табыңдар
ІІн.
4.Табиғи маржанның құрамында кальций , көміртек , оттек массалық қатынастары 10 : 3 : 12 –ге тең болады. . Маржанның формуласын табыңдар.
4.2.«Маңызды бейметалдар» Бақылау жұмысы
І нұсқа ІІ нұсқа
1) Мүмкін болатын реакция теңдеулерін аяқтаңдар. Олардың иондық теңдеулерін
жазыңдар:
А) Na2CO3 + НNО3 = А) СuСІ2 + КОН =
Б) Н2SО4 + КОН = Б) NaСІ + Н2SО4 =
В) КСІ + НNО3= В) НNО3 + Са(ОН)2 =
Г) СuSО4 + NaОН = Г) К2СО3 + НСІ =
2) Берілген айналымдарды жүзеге асыруға болатын реакция теңдеулерін жазыңдар:
А) S→SО2→SО3→Na2SО4→ВаSО4 А) С→СО→СО2→СаСО3→СаСІ2
Б) N2→NН3→NО→NО2→НNО3→NН4NО3 Б) Р→Р2О5→Н3PO4→КН2PO4→ К3PO4
3) Құрамында 20% қоспасы бар 200г ізбес 3) 200г 4%-тік хлорсутек пен 200г 17%
тасын ыдыратқанда алынатын көміртек (ІV) -тік күміс нитраты ерітіндісін оксидінің массасын есептеңдер. СО2-нің бір-біріне құйғанда алынуы мүмкін
практикалық шығымы теориялық тұнбаның массасын есептеңдер.
мүмкіндіктің 80%-ін құрайды.
X тарау. . Алюминий және оның қосылыстары
І нұсқа
Алюминийдің келесі заттармен әрекеттесу реакция теңдеулерін жазыңдар: хлормен сұйытылған күкірт қышқылы; хром (ІІІ) оксидімен; мыс (ІІ) сульфатының ерітіндісімен.
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Al(OH)3→AlCl3→ Al(OH)3→ Al2O3
Қандай сыртқы белгісі арқылы алюминийден жасалған бұйымдарды басқа материалдардан жасалған бұйымдардан айыра алады?
ІІ нұсқа
Химиялық реакция теңдеулерін аяқтаңдар:
Fe2O3+ Al → Al(OH)3 +NaOH→
Al2(SO4)3+BaCl2→ Al+ O2→
Осылардың ішінен тотығу-тотықсыздану реакциясын, сонымен қатар тотықтырғыш пен тотықсыздандырғышты көрсетіңдер
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Al(NO3)3→Al(OH)3 ; Al2O3→Al2(SO4)3; Al→AlCl3
Алюминийдің қолдану облысын жазыңдар және қолдануға негізделген қасиетін көрсетіңдер.
ІІІ нұсқа
Алюминий хлоридін алудың төрт жолының реакция теңдеулерін жазыңдар.
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Al→ Al2O3→Al2(SO4)3→ Al(OH)3
Неге алюминийлі ыдыс қайнаған суда бүлінбейді және атмосфералық жемірілуге ұшырамайды?
ІVнұсқа
Алюминийдің келесі қосылыстармен әрекеттесу реакция теңдеулерін жазыңдар: броммен, күкіртпен, сумен, нарий гидроксидімен.
Схема арқылы толық реакция теңдеулерін жазыңдар:
Al+?=H2+?; ?+KOH=Al(OH)3+?; HCl+?= AlCl3+H2O
Алюминий сымдарын өңдеген кезде балқыған алюминийді домалақ ауызынан өткізеді. Тамшыға бөлмей ағымды қатырады. Неге?
Жұмыс 6. V тақырып бойынша қорытындылау
І нұсқа
Кальций гидроксидінің химиялық қасиетін сипаттайтын реакция теңдеулерін жазыңдар.
Темір (ІІ) хлоридінің ерітіндісінің электролизінің схемасын құраңдар
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
алюминий оксиді→алюминий нитраты→
→алюминий гидроксиді
алюминий
алюминий гидроксиді→алюминий хлориді
Өндірісте алюминийді неге қолданады? Алюминотермиялық деген не және оны қайда қолданады?
140 г. кальций оксидінен 182 г. кальций гидроксидін алды, кальций гидроксидінің шығымының массалық үлесін есептеңдер.
ІІ нұсқа
1.Алюминий оксиді қандай оксидтер тобына жатады? Оның қасиетін сипаттайтын реакция теңдеулерін жазыңдар.
2.Натрий хлоридінің балқымасының электролизінің схемасын құраңдар.
3.Келесі айналым орындалатын реакция теңдеулкрін жазыңдар ;
Кальций →кальций оксиді→кальций гидроксиді→кальций карбонаты→кальций гидрокарбонаты→кальций хлориді.
4.Жеңіл әрі мықты кальций металы авиациялық өндірісте және көлікшығарудың басқа облысында неге қолданылмайды?
5. 5% қоспасы бар, 80г натрий карбонаты әк суымен әрекеттескен кезде қанша масса кальций карбонаты алынады?
III нұсқа
1.Алюминий гидроксидінің химиялық қасиетін сипаттайтын рекция теңдеуін жазыңдар.
2.Калий иодидінің балқымасының электролизінің схемасын құраңдар.
3.Келесі айналым орындалатын реакция теңдеулерін жазыңдар:
Кальций хлориді→кальций карбонаты→кальций гидрокарбонаты→кальций карбонаты→кальций нитраты→кальций карбонаты.
4.20% қоспасы бар, 500г. әктасты күйдірген кезде қанша масса кальций оксидін алуға болады?
ІVнұсқа
Кальций оксиді оксидтерінің қай тобына жатады? Оның қасиетін сипаттайтын реакция теңдеулерін жазыңдар
Мыс (ІІ) бромидінің ерітіндісінің электролизінің схемасын құраңдар.
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
алюминий оксиді→алюминий сульфаты алюминий
алюминий хлориді→алюминий гидроксиді
Алюминий табиғатта қандай қосылыс құрамында кездеседі?
Сөндірілген әкке 3,15 г. таза азот қышқылын әсер етті. Егер шығымының массалық үлесі 0,98 болса, кальций нитратының қанша массасы алынады?
XI тарау. Темір. Металлургия.
Темір және оның қосылыстары
І нұсқа
Темірдің жай заттармен әрекеттесу реакция теңдеулерін жазыңдар: оттегі, хлор, күкірт, бром. Түзілген заттарға атау беріңдер
Темір атомының құрылысының схемасын бейнелеңдер. Қосылыстағы темірдің тотығу дәрежесін көрсетіңдер
Екі ерітіндінің біреуінде Fe2+ионы, екіншісінде – Fe3+ионы бар екенін қалай дәлелдейсіңдер. Жүретін реакция теңдеулерін жазыңдар
32 г. мыс (ІІ) сульфаты бар ерітіндіге 28 г. темір жаңғағын қосты. Мұнда қанша масса мыс бөлінді?
ІІ нұсқа
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Fe(NO3)3→ Fe(OH)3→ Fe2O3→Fe→ FeCl2
+2 тотығу дәрежесіндегі темірдің қосылысы қандай қасиет: тотығу немесе тотықсыздану көрсетеді? Неге?
Темір металын темір (ІІ) гидроксидін қалай алуға болады? Реакция теңдеулерін келтіріңдер
112 г. темір сұйытылған күкірт қышқылында еріген кезде (қ.ж.) қанша көлем сутегі алуға болады, егер сутегінің шығымының көлемдік үлесі 98% болса ?
ІІІ нұсқа
Темірдің басқа ерітінділерімен қосылу реакция теңдеулерін жазыңдар: А) күкірт қышқылы; Б) мыс (ІІ) сульфаты; В) бромсутекті қышқыл; Г) қорғасын нитраты
Темірдің (ІІ) және (ІІІ) оксидтері және оларға сәйкес гидроксидтері қандай сипатқа ие?
Үш номерленген пробиркаларда: натрий, барий және темір(ІІ) хлоридтерінің ерітінділері берілген қандай тәжірибелік жолмен оларды табуға болады? Сәйкес реакция теңдеулерін жазыңдар
80%FeCO3 құрамында бар, 50 г. сидерит минералы тұз қышқылымен әрекеттескен кезде бөлінген көміртегі( ІV) оксидінің көлемін табыңдар
ІV нұсқа
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
Fe→FeSO4→ Fe(OH)2 → Fe(OH)3→F eCl3
Темір (III) тұздарының сулы ерітінділері реакцияның қандай ортасын көрсетеді? Неге?
3.Темір (II) сульфатты арқылы: а)темір (II) хлориді; б)темір (II)нитраты қалай алады? Сәйкес реакция теңдеулерін жазыңдар.
4. 7г темірді 18г хлормен әсер етті. Темір (III) хлоридінің қандай массасы түзілді?
. Өнеркәсіпте металдар алудың әдістері
І нұсқа
Жоспар бойынша шөгеннің өндірілуін жазыңдар: А) шикізат; Б) өндіру үшін аппараттың құралдары; В) өндіру кезінде жүретін негізгі химиялық реакциялар. Шөгеннің қолдану облысын атаңдар
6 г. құрышты сымды оттегінде жандырды. Одан 0,1 г. көміртегі( ІV) оксиді түзілді. Құрышты көміртегінің масалық үлесі қандай?
ІІ нұсқа
Құрыштың оттекті-конверторлы әдісімен жоспар бойынша өндірудің әдістерін жазыңдар: А) шикізат; Б) өндіру үшін аппараттың құралдары; В) өндіру кезінде жүретін негізгі химиялық реакциялар. Құрыштың қолдану облысын атаңдар
0,4% қоспасы бар, 50 т. алюминий оксидін электролиздеген кезде алюминийдің қанша массасын алуға болады?
ІІІ нұсқа
Жоспар бойынша алюминийді өндірудің технологиясын жазыңдар: А) шикізат; Б) өндіру үшін аппараттың құралдары; В) өндіру кезінде жүретін негізгі химиялық реакциялар. Алюминийді қолдану облысын атаңдар
5 г. көміртегімен темірдің құймасының үлгісін күкірт қышқылының ерітіндісінде артық мөлшерінде ерітті. Реакция аяқталған соң бөлінген сутектің көлемі 1,96 л. құрады. Құймадағы темірдің масалық үлесін есептеңдер.
ІV нұсқа
Құрышты өндіруді мартен әдісімен жоспар бойынша әдісті жазыңдар:А) шикізат; Б) өндіру үшін аппараттың құралдары; В) өндіру кезінде жүретін негізгі химиялық реакциялар.
Шөген құрамында темір карбиді Fe2С сияқты көміртегі бар. Көміртегінің шөгендегі массалық үлесі 3,6%. Шөгендегі темір карбидінің масалық үлесін есептеңдер.
XII тарау. Органикалық заттар. Көмірсутектер.
І нұсқа
Қаныққан көмірсутектер деп нені атайды? Олардың кейбіреулерінің молекулалық формулаларын және атауларын көрсетіңдер.
Қаныққан, қанықпаған және ароматты көмірсутектердің генетикалық байланысы немен қорытындылады?
Әрекеттесу реакция теңдеулерін жазыңдар: А) бензолдың сутекпен; Б) этиленнің хлор сутекпен. Осы реакциялар типін көрсетіңдер және алынған затты атаңдар
ІІ нұсқа
Этилен мен промиленнің құрылымдық формуласын жазыңдар. Олардың құрылысында артық не? Оларды көмірсутектердің қай класына жатқызады?
Бензолдың физикалық қасиеті және қолдану облысы қандай?
Реакция теңдеуін құр: А) метанның жануы; Б) этанның термиялық ыдырауы. Тұрмыста адамдар бұл процестің қайсысын кең қолданады? Неге?
ІІІ нұсқа
Этиленнен адамдар көп қолданатын қандай материал алады? Осы материалдың физикалық қасиеті және қолдану облысы қандай?
Табиғи газ құрамына кіретін кейбір көмірсутектердің формуласын жазыңдар. Адамдар табиғи газды қалай қолданады?
Реакция теңдеуін құраңдар: А) бензолдың броммен әрекеттесуін; Б) этиленнің жануын. «а» реакция теңдеуін көрсетіңдер және алынған затты атаңдар
ІV нұсқа
Қаныққан көмірсутектер және олардың галогентудырушыларын қолдану облысы қандай?
Ацетиленнің құрылымдық формуласын жазыңдар: А) оны көмірсутектердің қандай класына жатқызады; Б) оны қалай алуға болады, көрсетіңдер
Реакция теңдеуін құраңдар: А) пропиленнің сутегімен әрекеттесуін; Б) метанның термиялық ыдырауы. Адамдар метанның термиялық ыдырауын қандай мақсатта қолданады?
XIII тарау Спирттер.
І нұсқа
Этил спиртін қолдану облысы қандай?
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
CH3Cl→CH3OH→СО2
9,2г. натрий пропил спиртімен әрекеттескен кезде (қ.ж.) қанша көлем сутегі бөлінеді?
ІІ нұсқа
Біратомды қаныққан спирттердің класының жалпы формуласын жазыңдар. Олардың құрамында қандай функционалды топ бар?
Келесі өзгерісті орындайтын реакция теңдеулерін жазыңдар:
С2Н4→С2Н5ОН→СО2
2,3 г. этил спирті жанған кезде қанша масса су түзілді?
ІІІ нұсқа
Глицериннің физикалық қасиеті және қолдану облысы қандай?
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
С2Н5ОН→С2Н4→С2Н5Cl
4,6 г. этанол хлорсутекпен әрекеттесекен кезде қанша масса хлорэтан түзіледі?
ІV нұсқа
Құрылысы бойынша көпатомды спирттер біратомды спирттерден айырмашылығы қандай?
Келесі өзгерісті орындайтын реакция теңдеулерін жазыңдар:
С2Н6→С3Н7ОН→С3Н7ONa
23г. этанол дегидратацияланған кезде (қ.ж.) қанша көлем этилен алуға болады?
. Карбон қышқылдары және биологиялық маңызды органикалық заттар.
І нұсқа
Сірке қышқылының физикалық қасиеті және қолдану облысы қандай?
Төменде келтірілген схема бойынша химиялық реакция теңдеулерін жазыңдар:
А) Н-СООН+Mg→
Б) CH3-CHO+O2→
«б» реакция теңдеуіне сәйкес процесті көрсетіңдер.
Картоп пен ақ нанда крахмал бар екенін тәжірибелік жолмен қалай дәлелдейсіңдер? Жұмыстың жоспарын құраңдар және байқауды жазыңдар
ІІ нұсқа
Күрделі эфирлердің физикалық қасиеті және қолдану облысы қандай?
Төменде келтірілген схема бойынша химиялық реакция теңдеулерін жазыңдар:
А) CH3-СООН+Са(ОН)2→
t
Б) (C6H10O5)n +nН2O→
«б» реакция теңдеуіне сәйкес процесті көрсетіңдер.
Майлардың сумен гидролизі майлардың сілті ерітінділерімен гидролизі әдісінен түзілген өнімдер сипаттамасы бойынша немен ерекшеленеді?
ІІІ нұсқа
Сабын деген не? Қайда және қалай қолданады?
Төменде келтірілген схема бойынша химиялық реакция теңдеулерін жазыңдар:
А) Н-СООН+ C2H5OH →
t
Б) H-CHO+Ag2 O →
«б» реакция теңдеуіне сәйкес процесті көрсетіңдер.
Ақуыздардың денатурациясы деген не?Оның болуы неде және қандай факторлар ықпал етеді?
ІV нұсқа
Майлардың физикалық қасиеті және қолдану облысы қандай?
Төменде келтірілген схема бойынша химиялық реакция теңдеулерін жазыңдар:
А) C2H5-СООН+К2О →
t
Б) CH3-CОONa(қ)+H2SO4 →
«б» реакция теңдеуіне сәйкес процесті көрсетіңдер.
Неге ақуызды тамақсыз жүруге болмайды? Ақуызды тамақ адам ағзасында не болады?
тақырып бойынша қорытындылау
І нұсқа
Майлар гидролизінің қандай түрлерін білесіңдер? Олардың айырмашылығы неде?
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
С2Н2
СН4
СН3Br→A
А затын атаңдар.
Қандай қанықпаған көмірсутектерді білесіңдер? Қолдану облысын атаңдар
234 г. бензолды гидрлеу кезінде қанша масса циклогексан алынады? Циклогеннің шығынының массалық үлесі 65% құрайды.
ІІ нұсқа
Көмірсутектер спирттер және карбон қышқылдары арасында генетикалық байланыс немен қорытындыланады? Нақты мысалмен жауабын түсіндіріңдер
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
С6Н6В
С2Н2
С2Н6
В затын атаңдар.
Глицеринді заттардың қай класына жатқызады? Оның құрылысы мен қасиеті қандай?
Бромэтан алу үшін 23 г. этанол мен 56,7 г. бромсутегін алды, мұнда қанша масса бромэтан түзілді?
ІІІ нұсқа
Сабынды дайындау үшін қандай тұздар мен қандай қышқылдарды қолданады? Нақты мысал келтіріңдер.
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
+СН2- СООН
С2Н4→С2Н5ОН Х
Н2
Х затын атаңдар.
Бензолды қандай органикалық заттардың класына жатқызады? Оның физикалық қасиеті қандай?
5 л. этиленді толық жағу үшін қанша көлем ауа қажет? Ауадағы оттегінің көлемдік үлесі 21% құрайды.
ІV нұсқа
Адам ағзасында ақуыздар қандай қызмет атқарады?
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
+Н2 Х
СН3→СНО−
СН3-СООН→СН3→СООNa
Хзатын атаңдар.
Қандай карбон қышқылдарын білесіңдер? Олардың қолдану облысы қандай?
23 г. құмырсқа қышқылын метил спиртімен әрекеттесу нәтижесінде 24 г. күрделі эфир алынды. Эфирдің шығымының массалық үлесін есептеңдер.
VІІ тақырып бойынша қосымша тапсырмалар.
I нұсқа
Салыстырмалы молекулалық массасы мынаған тең, қаныққан көмірсутектердің молекулалық формулаларын жазыңдар: А) оттегінің салыстырмалы атомдық массасына тең; Б) көмірқышқыл газының салыстырмалы молекулалық массасына тең; В) магний гидроксидінің салыстырмалы молекулалық массасына тең; Г) СаS салыстырмалы молекулалық массасына тең
Мұнайдың практикалық маңызы қандай?
Қанықпаған көмірсутектерді алуға болатын реакция теңдеуін жазыңдар
Натуралды каучуктың құрамын, физикалық қасиетін және қолданылуын көрсетіңдер.
Метан үшін есептеңдер: А) ондағы элементтердің массалық қүлесін; Б) оның 4 г. (қ.ж.) көлемі
алыстырмалы молекулалық массасы мынаған тең, қаныққан көмірсутектердің молекулалық формулаларын жазыңдар: А) N2 салыстырмалы молекулалық массасына тең; Б) көмірқышқыл газының салыстырмалы молекулалық массасына тең; В) магний гидроксидінің салыстырмалы молекулалық массасына тең; Г) MgCO3 салыстырмалы молекулалық массасына тең
Этанды этилен қоспасынан қалай тазартады? Жауабын химиялық реакция теңдеулері бойынша жазыңдар
Ацетиленнің және оның негізінде алынған материалдың аса маңызды қолдану облысы қандай?
Төменде келтірілген формулаларды қосылыстардың класы бойынша заттарға бөліңдер және оларды атаңдар:
А) СН3- СН3 Б) СН= СН В)СН3- СН= СН2 Г) Н3С- СН2- СН2 Д) СН2=СН2
׀
СН2- СН3
Е) СН3- СН2
׀
СН3
Келесі айналымды орындайтын реакция теңдеулерін жазыңдар:
СН4→С2Н2→С2Н4→С2Н6→СО2
С6Н6
Ацетиленнің кейбір көлемі 39 г. массасы болады. Осындай көлемдегі (қ.ж.) пропиннің массасын есептеңдер.
Келесі заттардағы элементтердің массалық үлесін есептеңдер: А) Этанол; Б) Бутанол; В) Сірке қышқылы.
Төменде келтірілген заттардың формуласынан тек спирттердің формуласын теріп жазыңдар және оларды атаңдар:
А) С6Н6 Б) СН3ОН В)С2Н4 Г) С4Н9ОН Д) СН3-СНО
Спирттердің атомдылығы немен анықталады?
Ақуыз молекуласы қандай элементтер атомынан құралған? Ақуыздар қандай химиялық қасиет көрсетеді?
Ақуыздың біріншілік, екіншілік және үшіншілік құрылымы нені білдіреді? Әрбір құрылымға қандай байланыс сәйкес?
Пробиркалардың біреуінде сабын ерітіндісі, ал екіншісінде жуғыш ұнтақ бар. Қандай тәжірибелік жолмен оларды табуға болады? Жұмыстың жоспарын құраңдар және болатын құбылысты жазыңдар
20 л. (қ.ж.) көлемі бар этиленді гидрлеу кезінде 18 л. этан алынды. Этанның шығымының көлемдік үлесін есептеңдер.
Жауабы: 90%
Бромныі 1,6% массалық үлесі бар бром суының қандай массасы 1,12(қ.ж.) көлемі пропиленді түссіздендіреді?Жауабы: 500 г.
Этиленнің кейбір көлемінде 7 г. массасы болады. Осындай көлемдегі пропиленнің (қ.ж.) массасын есептеңдер. Жауабы: 10,5 г
92 г. таза этил спиртінен (қ.ж.) 42 л. этилен спиртін алды. Оның шығымының көлемдік үлесін есептеңдер.Жауабы: 93,75%
20 л. этен қоспасын этинмен толық гидрлеу үшін қанша көлем сутегі жұмсалады? Қоспадағы этиннің көлемдік үлесі 40% құрайды. Жауабы: 28 л.
39 г. бензолдан қанша масса бромбензол алуға болады? Бромбензолдың шығымы 64 % құрайды.Жауабы: 50,2 г.
(қ.ж.) 25 л. ацетиленнен 16 г. бензол алды. Оның шығымының көлемдік үлесін есептеңдер. Жауабы: 55,2%
8 г. магний сірке қышқылымен әрекеттескен кезде қанша көлем сутегі бөлінеді? Жауабы: 7,5л.
92 г. этил спирті бромсутегінің артық мөлшерімен әрекеттескен кезде қанша масса бромэтан түзіледі? Реакция өнімінің шығымының массалық үлесі 85% құрайды.Жауабы: 185,3 г.
90 г. сірке қышқылы метил спиртімен әрекеттесу нәтижесінде 100 г. күрделі эфир түзілді. Эфир шығымының массалық үлесін есептеңдер. Жауабы: 90%
90 г. сірке қышқылы альдегидін сутегімен тотықсыздандырған кезде 82 г. этил спирті алынды. Спирт шығымының массалық үлесін есептеңдер. Жауабы: 87%
Картопта крахмалдың массалық үлесі 20%160 г. картоптан қанша масса глюкоза алуға болады? Жауабы: 360 г.
Егер шығымның массалық үлесі 75% құраса, 81 г. крахмалдан қанша масса глюкоза алуға болады? Жауабы: 67,5г.
YIII тарау «Органикалық заттар» тақырыбын қорытыныдлауға арналған сұрақтар
5.1. 1-тапсырма. Берілген ұғымдар мен терминдерге түсініктеме беріңдер.
1.Органикалық химия.
2.Изомерия.
3. Изомерлер.
4.Гомологтар.
5.Электрон бұлттарының гибридтенуі.
6.Сигма және р-байланыстар.
7.Көмірсутектер(-ан, -ен, -ин, -диен, - арен).
8.Жалпы формуласы.
9.Радикал.
10.Полимерлену.
11.Орынбасу.
12.Қосып алу.
13.Мұнай өнімдері.
14.крекинг.
15.Отын оның түрлері.
15.Отынды тиімді жағу деген не?
5.2. 2-тапсырма.Заттардың құрылысы. Көмірсутектер.
1. А.М. Бутлеров тұжырымдаған органикалық қосылыстардың құрылыс теориясының негізгі қағидаларын айтып беріңдер.
Көмірсутектердің жіктелуін мысалмен түсіндіріңдер.
Алкандардың қандай гомологтарын білесіңдер?
Қанықраған көмірсутектерге қандай қосылыстар жатады?
Бутадиенді көмірсутектерге мысалдар келтіріп, қолданылатын жерлерін айтып беріңдер.
6.Этилен мен ацетиленнің химиялық қасиеттерінде қандай ұқсастық бар екнін реакция теңдеулерін жазу арқылы дәлелдеңдер.
7.Бензол молекуласында көміртек атомдары өзара қалай жалғасады? Басқа көмірсутектерден айырмашылығы неде?
8. Табиғи газдан қандай заттар алуға болады? Олар негізінен қайда қолданылады?
9. Мұнайдан алынатын қандай заттарды білесіңдер?
10.Қазақстанда көмір қай жерлерде өндіріледі?
5.3. 3- тапсырма.
1.Метанның, этанның, бензолдың буларының сутекпен салыстырғандағы тығыздықтары қанша?
2.Көлемі (қ.ж.) 18л СН4, 3л С2Н2, 5л С3Н8 болатын газдардың қанша зат мөлшері және қандай массасы болатынын есептеңдер.
3.Құрамында 93,75% көміртек, 6,25% сутек бар белгісіз газдың ауамен салыстырғандағы тығыздығы 4,41 болатынын ескере отырып, заттың молекулалық формуласын табыңдар.
4. Көлемі (қ.ж.) 89,6 л метанды толық ыдыратқанда неше грамм күйе алынады?
5. Көлемі 5,6 л этилен (қ.ж.) қанша грамм бромды қосып алады?
6 . Төмендегі айналымдарды жүзеге асыруға болатын реакция теңдеулерін жазыңдар. А, Б заттарының атын атаңдар.
- H2 -H2 2Cl2
этан А Б тетрахлорэтан.
7.Массасы 3,9 г бензолды толық жағу үшін қанша көлем ауа қажет екенін есептеңдер.
8.а) бутаннан; ә) бутеннен бутадеин – 1,3-ті қалай алуға болады? Химиялық реакция теңдеуін жазыңдар.
9. Өзгерістерді іске асыруға болатын реакция теңдеулерін жазыңдар:
пропан→пропен→хлорпропан
↓ ↓
көміртек дихлорпропан
(IV) оксиді
10.Берілген айналымдарға мысалдар келтіріп, реакция теңдеулерін жазыңдар: Қаныққан көмірсутек→қанықпаған көмірсутек→спирт→жай эфир.
6.1. ОТТЕКТІ ОРГАНИКАЛЫҚ ҚОСЫЛЫСТАР
Спирттер. Көп атомды спирттер 5-10 минуттық тексеру жұмысы
| I нұсқа | II нұсқа |
| 1.Этанолдың молекулалық, құрылымдық формуласын жазыңдар 2. Бірінші сұрақтағы аты аталған заттың жітелуін, қолданылуын айтыңдар. 3. Берілген теңдеулерді аяқтаңдар: а) CH4 + O2→ ә) C2H4 + O2→
түзілген өнімдердің аттарын атаңдар | 1.Метанолдың молекулалық және құрылымдық формуласын құрыңдар 2.Бірінші сұрақта аты аталған заттың молярлық массасын табыңдар 3.Берілген теңдеулерді аяқтаңдар: а) C2H6 + O2→ ә) C2H4 + HBr → б) түзілген өнімнің аттарын атаңдар |
6.2. Алған білімді бекіту үшін 5-10 мин-тық тапсырма
I нұсқа. 1.сахарозаның молекуласындағы оттектік массалық үлесін есептеңдер.
2. Көмірсулардың табиғатта таралуын айтып беріңдер.
II нұсқа. 1. Мына айналымдарды іске асыруға болатын реакция теңдеулерін жазыңдар:
Этилен→этил спирті→сірке қышқылы→сіркеэтилэфирі.
2. Крахмалды, целлюлозаны табиғатта неден алады?
III нұсқа. Сахарозаның молекуласындағы көміртектің массалық үлесін есептеңдер:
Көмірсулардың жіктелуін айтып беріңдер.
Глюкоза, сахароза, крахмал, целлюлозаның физикалық қасиеттерін жеке-жеке сипаттаңдар, табиғатта таралуын айтып беріңдер;
Көмірсулар қандай мақсатқа қаолданылады?
6.3. Есептер мен жаттығулар
Сутек бойынша салыстырмалы тығыздығы 15-ке тең көмірсутектің молекулалық формуласын анықтаңдар.
Құрамында көміртектің массалық үлесі 51,89%, сутектің массалық үлесі 9,73%, хлордың массалық үлесі 33,38% болатын, сутек бойынша буының тығыздығы46,25-ке тең көмірсутектің формуласын есептеп шығарыңлар. (C4H9Cl)
Құрамында көміртектің массалық үлесі 85,7%, сутектің массалық үлесі 14,3% болатын сутек бойынша тығыздығы14-ке тең көмірсутектің формуласын табыңдар. (C2H4)
Ауа бойынша тығыздығы 1,93-ке тең, құрамындакөміртектіңмассалық үлесі 85,7%, болатын көмірсутектің молекулалық формуласын есептеп шығарыңлар. (C4H8)
Ауа бойынша тығыздығы 1,86-ға тең, құрамындакөміртектіңмассалық үлесі 88,9%, болатын көмірсутектің молекулалық формуласын есептеп шығарыңлар. (C4H6)
Мына алкандардың: а) н-пентан; ә) 2-метилбутан; б) 2,4-диметилпентан; в) триметилметанның құрылымдық формулаларын жазыңдар.
Мына заттардың: а) метилциклобутан; ә) 1,2-диметилциклобутанның құрылымдық формулаларын жазыңдар.
Изооктанның (2,2,4-триметилпентанның) құрылымдық формуласын жазып, құрамында қанша біріншілік,екіншілік, үшіншілік және төртіншілік көміртек атомлары бар екенін көрсетіңдер.
Мына қосылыстардың: а) 2-метилпропен; ә) 4-метилпентен-2 оларлың құрылымдық формулаларын жазыңдар.
Мына қосылыстардың: а) 3-метилпентин-1; ә)4-метилгексин-2; құрылымдық формулаларын жазыңдар.
Мына қосылыстардың құрылымдық формулаларын жазыңдар: а) 1,3,5-триметилбензол ә) 1-метил-2-пропилбензол б)n-метилэтилбензол в) изопрен (2-метилбутадиен-1,3)
Мына айналымға сәйкес реакциялардың теңдеулерін жазып, реакциялардың жүру жағдайларын көрсетіңдер:
этан→хлорэтан→этил спирті→дивинил(бутадиен-1,3)→ дивинил көксағызы.
Құрамында 25% қоспасы бар 500кг кальций карбидінен ацетиленнің қандай көлемін (қ.ж.) алуға болатының есептеңдер. (131,250м3)
52г ацетиленмен толық әрекеттесуге бромның қандай массасы қажет? (640г)
Көлемі 11,2л (қ.ж.) ацетиленмен толық жағу үшін, ауаның қандай массасы қажет болатынын есептеңдер. Ауа құрамында 20% оттек бар деп есептеңдер. (140л)
Көлемі 11,2л алканнан (қ.ж.) неше моль алкен алуға болатынын табыңдар. (0,5моль)
Зат мөлшері 1,5моль этиленді сумен әрекеттестіргенде, зат шығымы 80% болатын жағдайда этанолдың қандай массасын алынатынын есептеңдер. (55,2г)
Мына сізбанұсқа бойынша, берілген айналымды орындауға мүмкіндік беретін реакция теңдеуін жазыңдар.
метан→хлорметан→бутан→дихлорбутан→циклобутан
Берілген сізбанұсқаны орындауға мүмкіндік беретін реакция теңдеулерін жазыңдар және жүру жағдайларын көрсетіңдер.
CaCO3→ CaO→ CaC2→HC≡CH→H3C-CHO→ H3C-COOH
Мына сізбанұсқа бойынша, берілген айналымды орындауға мүмкіндік беретін реакция теңдеуін жазып, заттарды атаңдар.
C2H4→C2H6→C2H5Cl →C2H5OH→C2H4→(-CH2-CH2-)n
Өзгерістер тізбегіндегі соңғы өнім X5;
CH3-COH X1 X2 X3X4
X5. (C2H6)
Төмендегі айналымды орындауға мүмкіндік беретін химиялық реакция теңдеулерін жазыңдар және жүру жағдайларын көрсетіңдер.
CH4→CH≡CH→C6H6→ C6H5-C2H5→ C6H2-C2H5(NO2)3→CO2+N2+H2O
Берілген айналымды орындауға мүмкіндік беретін реакция теңдеуін жазып, заттарды атаңдар.
CH4→CH3Cl→C2H6→C2H5Cl →C3H8
Массасы 14,5г көмірсутекті жаққанда, 44г көміртек диокиді мен 22,5г су түзілді. Қосылысың сутек бойынша тығыздығы 29-ға тең. Көмірсутектің молекулалық формуласын есептеп шығарыңлар. (C4H10)
Массасы 39г бензол алу үшін қанша грамм циклогексан қажет болатындығын есептеңдер. (42г)
Газ тәрізді көмірсутектің 11,2л-ін (қ.ж.) жаққанда, 33,6л көмірқышқыл газы мен су түзілді. Көмірсутектің молекулалық формуласын есептеп табыңдар.
Метанды лабораторияда алюминий карбидіне сумен әсер етіп алуға болады. Алюминий карбидінің формуласын жазып одан метан алу реакциясынның теңдеуін құрастырыңдар.
Влюц реакциясы арқылы бутанды алу үшін қандай галогеналкандар қажет болатынын айтып, сәйкес реакция теңдеулерін жазыңдар.
Ароматты көмірсутектердің С9-мүшесінің үш изомерінің құрылысдық формулаларын жазып, оларды атаңдар.
Бензолдың бүйір тізбегінде үш байланысы бар туындылары да болалы. Олардың ең қарапайымы фенилацетилен(C6H5-C≡CH). Фенилацетилен бром суын түссіздендіреді. Жүретін реакциялардың теңдеуін жазыңдар. Фенилацетиленді тағ қандай көмірсутектерің туындысы ретінде қарастыруға болатынын түсіндірі
№1 зертханалық тәжірибе
Тақырыбы: «Әртүрлі химиялық байланысы бар зат молекулаларының моделін жасау, кристалдық торлары әртүрлі заттардың қасиеттерін зерттеу»
Мақсаты: Физикалық, химиялық құбылыстарға тән белгілерді түсіндіру, мысалдар келтіріп, құбылыстарды ажырату, химиялық құбылыс, химиялық реакция екенін оның жүру белгілерін меңгерту.
Көрнекілік: әртүрлі кристалды тор үлгілері мәнін түсіндіріңдер.
Реактивтер мен құралдар: Пластмассадан жасалған шарлар және оларды байланыстыруға арналған таяқшалар.
Химия кабинетінде қауіпсіздік техникасы ережесін сақтауды ескерту.
Тәжірибенің орындалуы:
1) 1. 2. 3. 4. 5.
Тапсырма: суреттердегі кристалдық тор үлгілерін атын тауып, әрқайсысына сипаттама бер.
2) Ермексаздан және металдан немесе пластмассадан жасалған шарлар мен таяқшалар берілген.
Оқытушы: тапсырмасы бойынша: а) иондық; ә) атомдық; б) молекулалық кристалдық торы бар заттардың моделдерін жасаңдар.
3)Өздерің моделдерін жасаған заттардың физикалық және химиялық қасиеттеріндегі айырмашылықтардың
Практикалық жұмысты орындау барысы:
| № | Тәжірибенің орындалуы | Жасалған жұмыстар |
| 1 | Иондық кристалдық тор түзетін NаСI ас тұзының моделін құрастыр және суретін сал. |
|
| 2 | Төмендегі молекулалық кристалдық торы бар заттардың модельдерін жасаңдар және суретін салыңдар: І2, Н2О(мұз). |
|
| 3 | Төмендегі атомдық кристалдық торы бар заттардың модельдерін жасаңдар және суретін салыңдар: С(алмаз және графит), S8. |
|
Тапсырма: Өздерің моделін жасаған заттардың физикалық қасиеттеріндегі айырмашылықтардың мәнін түсіндіріңдер.
Қорытынды:_____________________________________________________________
№2 зертханалық тәжірибе
Тақырыбы: «Гидроксидтерді алу (сілті, қышқыл) және олардың қасиеттерін зерттеу. Тұздар гидролизі»
Мақсаты: Студенттерге тұздар гидролизінің жүру механизмін түсіндіре отырып, тұздар ерітіндісінде индикаторлардың түсі өзгеруі жайлы білім беру;
Құралдар: сынауықтар
Реактивтер:NH₄CI, Na₂CO³, К₂СО₃ , фенолфталеин немесе лакмус ерітінділері
Жұмыс барысы
Химия кабинетінде қауіпсіздік техникасы ережесін сақтауды ескерту.
Тәжірибенің орындалуы:
Кестені толтыру
| Не істедік | Не байқадық | Реакция теңдеуі,қорытынды |
| Судың өте аз мөлшерде сутек Н+ және гидроксид ОН - иондарына диссоциацияланатыны белгілі: | Шындығында да күшті қышқыл мен күшті негіз әрекеттескенде түзілетін натрий хлориді, калий нитраты, калий сульфаты сияқты тұздардың сулы ерітіндісі бейтарап ортаны көрсетеді (электронды оқулық, №6 мысал). Кейбір орта тұздардың, мысалы, темір (ІІІ) хлоридінің NH₄CI судағы ерітінділері қышқылдық ортаны, ал натрий карбонатының Na₂CO³, калий карбонатының К₂СО₃ ерітіндісі сілтілік ортаны көрсетеді. Бұған көз жеткізу үшін осы тұздардың ерітінділеріне фенолфталеин немесе лакмус ерітінділерінің 1 - 2 тамшысын қосамыз |
|
№3 зертханалық тәжірибе
Тақырыбы: «Қышқыл, негіз және тұздардың сапалық құрамын тәжірибелермен дәлелдеу»
Мақсаты: Әр түрлі тұздар ерітініділерінің ортасын индикатор көмегімен анықтау
Құралдар мен реактивтер: сынауық, кальций оксиді, су, түрлі индикатор, шыны түтікше, натрий гидроксиді, мыс сульфаты, мырыш хлориді.
Жұмыс барысы
Химия кабинетінде қауіпсіздік техникасы ережесін сақтауды ескерту.
Тәжірибенің орындалуы:
Кестенітолтыру
Не істедік
Не байқадық
Реакция теңдеуі,қорытынды
Тапсырмалар:
Қышқылдардың формулаларын көрсетіңдер:а) H2SO4 ә)MgSO4 б) MgO в) HCI
Тұздардың формулалары:а)NaCI ә)CaSO4 б)MgSO4 в)NaOH
Қышқылдар металдармен және негіздік оксидтермен әрекеттескенде үнемі:а) су ә)сутек немесе басқа газдар б) тұз в) негіз түзіледі
Тұз қышқылымен: а)Ag ә)AI б)Fe в)Zn
Азот қышқылының мыс (ІІ) гидроксидімен химиялық реакция теңдеуіндегі реакция өнімдерінің формулаларымен олардың алдындағы коэффиценті:а) Cu(NO3)2және 2H2O ә) Сu(NO3)2 жәнеH2 б)CuOжәне 2H2O в)CuOжәне H2O
магний хлориді:а) MgO және HCI ә)Mg және HOH б)Mg және O2 в)Mg және HCI аралығындағы орынбасу реакциясының нәтижесінде алынады.
Хлорсутек қышқылының тұзы-кальций хлоридініңформуласындағы хлор атомыныңиндексі:а)1 ә)2 б)3 в)4
Күкірт қышқылының тұзы-литий сульфаты формуласындағы литий атомының индексі:а) 1 ә) 2 б)3 в)4
P→P2O5-+H2O→x айналым тізбегіндегі «х» деп белгіленген заттың формуласы:а)H3PO2ә)H3PO4 б)H3PO3 в)N2
Э→ЭО2→H2ЭО3 айналым тізбегіндегі «Э» элементі:а)CIә)S б)N в)P
Сұйылтылған күкірт қышқылы төмендегі заттармен әрекеттеседі:а) Mg және Cu(OH)2ә)CO2және NaOH б)FeO және H2S в)P және CuCI2
Тұз қышқылы:а) Cu-мен ә) CuO-мен б) Cu(OH)2-мен в) Zn-мен әрекеттеспейді.
№4 зертханалық тәжірибе
Тақырыбы:«Химиялық тепе-теңдіктің ығысуы (аммоний не калий тиоционаты мен темір (ІІІ) хлориді концентрациясының өзгеруі бойынша)»
Мақсаты:Бұл жұмыста калий роданиді (KSCN)мен темір (III) хлоридінің ( FeCl₃) әрекеттесуінің қайтымды реакциясы қарастыру
Құралдар мен реактивтер:сынауық, калий роданиді (KSCN)мен темір (III) хлоридінің ( FeCl₃)
Жұмыс барысы
Химия кабинетінде қауіпсіздік техникасы ережесін сақтауды ескерту.
Тәжірибенің орындалуы:Кестенітолтыру
| Не істедік | Не байқадық | Реакция теңдеуі,қорытынды |
| Экзотермиялық болады. | Қайтымды жүйенің тура реакциясы:FeCl₃ + 3KSCN→ Fe(SCN)₃ + 3KCl; ∆Н˂0 | Тепе-теңдік қай жағына ығысады KSCN, KCL, FeCl₃ -дін қосқанда? Бұл жағдайда әрбір компоненттің концентрациясы қалай өзгереді? Ле-Шателье шартын қолданып, жауапты түсіндір. Берілген реакцияның химиялық тепе-теңдігінің математикалық өрнегін жаз. |
№5 зертханалық тәжірибе
Тақырыбы:«Типтік металдар, бейметалдар мен амфотерлі элементтердің химиялық қасиеттері»
Бейнематериал көру арқылы жасау электронды оқулық
Қолданған әдебиеттер:
1. Н.Нұрахметов, К. Сарманова, К. Жексембина, Н.Заграничная, Ә. “Химия” 9 сынып, Алматы, “Мектеп” баспасы, 2004 ж.
2. Н.Нұрахметов, К.М.Жексембина, К. Сарманова, “Химия” 9 сынып, Әдістемелік нұсқау, Алматы, “Мектеп” баспасы, 2009 ж.
3. Химия мектепте, ғылыми – педагогикалық журнал, №2, 2009 ж, 70 -72 бет.
4. Оқу бағдарламалар, Астана қаласы, 2010 ж.
5.Химия жұмыс дәптері – Н.Нұрахметов
6.Химия мектепте – журнал 2010-2012 жылғы номерлері
7.Химик анықтамалығы – журнал 2012жыл
8.Интернет сайттар

 Получите свидетельство
Получите свидетельство Вход
Вход











 Химиядан методикалық оқу құралы (237.25 KB)
Химиядан методикалық оқу құралы (237.25 KB)
 0
0 1452
1452 23
23 Нравится
0
Нравится
0


