
Амины и Анилин
Колотова Екатерина Александровна
МАОУ НТГО ‘СОШ№3”
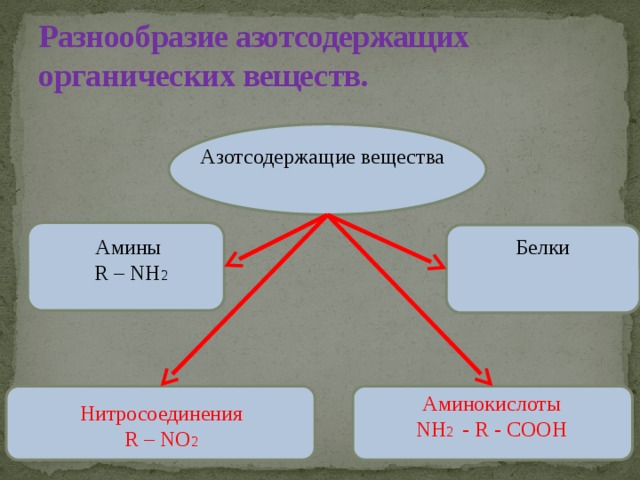
Разнообразие азотсодержащих органических веществ.
Азотсодержащие вещества
Белки
Амины
R – NH 2
Аминокислоты
NH 2 - R - COOH
Нитросоединения
R – NO 2

Амины.
Амины – органические производные аммиака , в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы:
RNH 2 , R 2 NH, R 3 N.
Группа – NH 2 называется аминогруппой.

История изучения аминов.
Первооткрывателями аминов считаются Ш.А. Вюрц и
А. В.Гофман (середина 19 века). Ученые получили первичные, вторичные и третичные амины.
Шарль Адольф Вюрц
(1817 – 1884)
Август Вильгельм Гофман
(1818 – 1892)

История изучения аминов.
Русский химик – органик. Открыл метод получения ароматических аминов восстановлением ароматических нитросоединений (реакция Зинина). Синтезировал анилин, заложил основы анилинокрасочной промышленности.
Николай Николаевич Зинин
( 1812 – 1880)
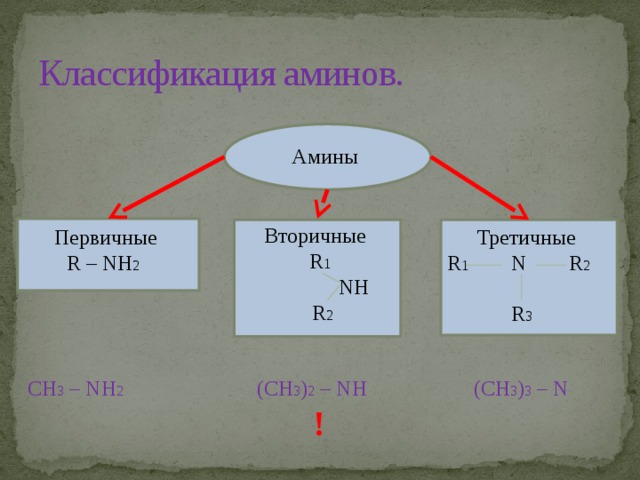
Классификация аминов.
Амины
Вторичные
R 1
NH
R 2
Первичные
Третичные
R – NH 2
R 1 N R 2
R 3
CH 3 – NH 2 (CH 3 ) 2 – NH (CH 3 ) 3 – N
!
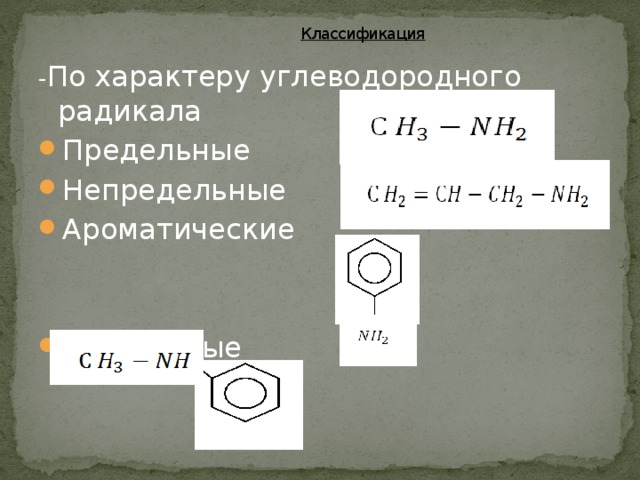
Классификация
- По характеру углеводородного радикала
- Предельные
- Непредельные
- Ароматические
- Смешанные
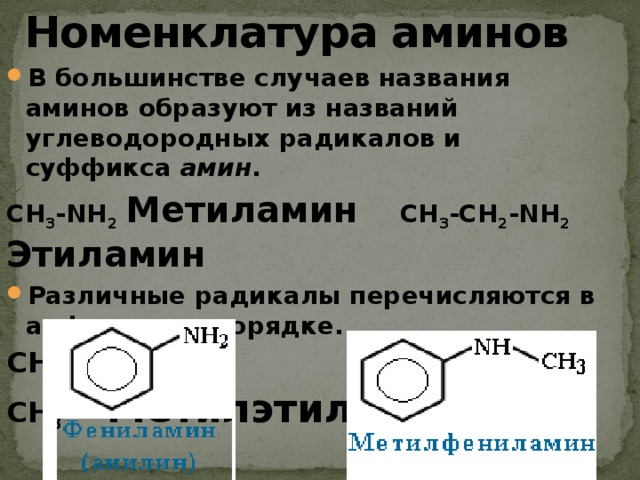
Номенклатура аминов
- В большинстве случаев названия аминов образуют из названий углеводородных радикалов и суффикса амин .
CH 3 -NH 2 Метиламин CH 3 -CH 2 -NH 2 Этиламин
- Различные радикалы перечисляются в алфавитном порядке.
CH 3 -CH 2 -NH-CH 3 Метилэтиламин

Номенклатура аминов
- Первичные амины часто называют как производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на аминогруппы -NH 2 .
- CH 3 -CH 2 -CH 2 -NH 2 пропанамин-1
- H 2 N-CH 2 -CH 2 -CH(NH 2 )-CH 3
бутан ди амин-1,3

Изомерия аминов
- Структурная изомерия
- углеродного скелета, начиная с С 4 H 9 NH 2 :
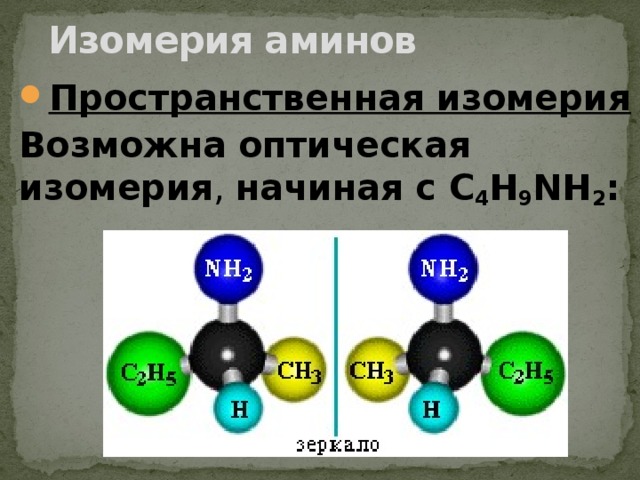
Изомерия аминов
- Пространственная изомерия
Возможна оптическая изомерия , начиная с С 4 H 9 NH 2 :

Физические свойства.
- Хорошо растворимы в воде( простые амины)
- Чем больше атомов углерода , тем хуже растворимость в воде.
- Простейшие(метиламин , этиламин , диметиламин)- газы , имеют запах аммиака.
- Средние амины- жидкости ,имеют «рыбный» запах.
- Высшие амины- начиная с -твёрдые вещества без запаха.

Получение аминов.
1 способ
2 способ
3 способ

Получение аминов.
4 способ
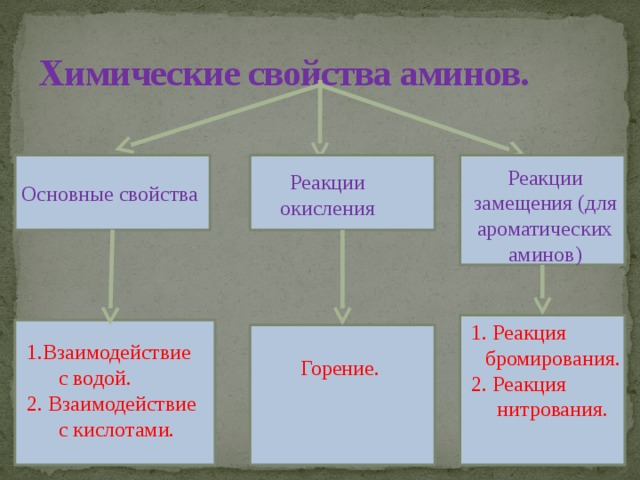
Химические свойства аминов.
Основные свойства
Реакции замещения (для ароматических аминов)
Реакции окисления
1. Реакция
бромирования.
2. Реакция
нитрования.
Горение.
1.Взаимодействие с водой.
2. Взаимодействие с кислотами.
![Химические свойства аминов. Взаимодействие с водой ( изменяют цвет индикаторов, проявляя основные свойства): CH 3 – NH 2 + H 2 O = [CH 3 NH 3 ] + + OH ˉ метиламмония 2. Взаимодействие с минеральными кислотами: CH 3 – NH 2 + HCl = [CH 3 NH 3 ] + Clˉ метиламмония хлорид 3. Реакция горения: 4CH 3 NH 2 + 9O 2 = 4CO 2 + 2N 2 + 10H 2 O Взаимодействие с бромной водой: C 6 H 5 NH 2 + 3Br 2 = C 6 H 2 Br 3 NH 2 ↓ + 3HBr 2,4,6-трибромамнилин (белый осадок)](https://fsd.videouroki.net/html/2018/03/11/v_5aa55dba143d0/img15.jpg)
Химические свойства аминов.
- Взаимодействие с водой ( изменяют цвет индикаторов, проявляя основные свойства):
CH 3 – NH 2 + H 2 O = [CH 3 NH 3 ] + + OH ˉ
метиламмония
2. Взаимодействие с минеральными кислотами:
CH 3 – NH 2 + HCl = [CH 3 NH 3 ] + Clˉ
метиламмония хлорид
3. Реакция горения:
4CH 3 NH 2 + 9O 2 = 4CO 2 + 2N 2 + 10H 2 O
- Взаимодействие с бромной водой:
C 6 H 5 NH 2 + 3Br 2 = C 6 H 2 Br 3 NH 2 ↓ + 3HBr
2,4,6-трибромамнилин
(белый осадок)

- Окисление аминов
- В отличие от аммиака , низшие газообразные амины способны воспламеняться от открытого пламени.
- 4СH 3 NH 2 + 9O 2 = 4CO 2 + 10H 2 O + 2N 2
- Ароматические амины легко окисляются даже кислородом воздуха. Являясь в чистом виде бесцветными веществами, на воздухе они темнеют. Неполное окисление ароматических аминов используется в производстве красителей.

- Амины широко распространены в природе . Их много в белковых пищевых продуктах . Например , триметиламин содержится в сельди. Он играет важную роль в биохимических процессах организма человека.
- Широко используются в органическом синтезе как исходное сырьё для получения красителей , пестицидов и других продуктов.
Применение аминов.
Лекарства
Пластики:
нейлон, полиуретан
Амины
Стабилизаторы
Пестициды
Анилиновые красители

Представитель аминов ароматических – анилин .
Ароматические амины являются более слабыми основаниями, чем аммиак (влияние бензольного кольца).
Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Поэтому анилин взаимодействует лишь с сильными кислотами, а его водный раствор не окрашивает лакмус в синий цвет.
Таким образом, основные свойства изменяются в ряду:
C 6 H 5 NH 2 3 2 2 NH 3 N

История создания
- В 1840 Ю.Ф.Фрицше обнаружил, что при нагревании с щелочью синяя окраска индиго исчезает и образуется вязкая масса коричневого цвета. Очистив это в-во, Фрицше получил быстро желтеющую на воздухе маслянистую жидкость и назвал её анилином.
- Примерно в то же время О.Унфердорбен нагреванием кристаллического индиго получил продукт, который он назвал кристаллином.

- Фридлиб Фердинанд Рунге в продуктах перегонки каменноугольной смолы открыл вещество, названное им кианолом.
- Н.Н.Зинин в 1841 году открыл способ восстановления нитробензола до соответствующего ароматического амина – бензидама.
- 1843 г. – Гофман установил, что бензидам, кианол, кристаллин и анилин – одно и то же соединение. Остановились на анилине.
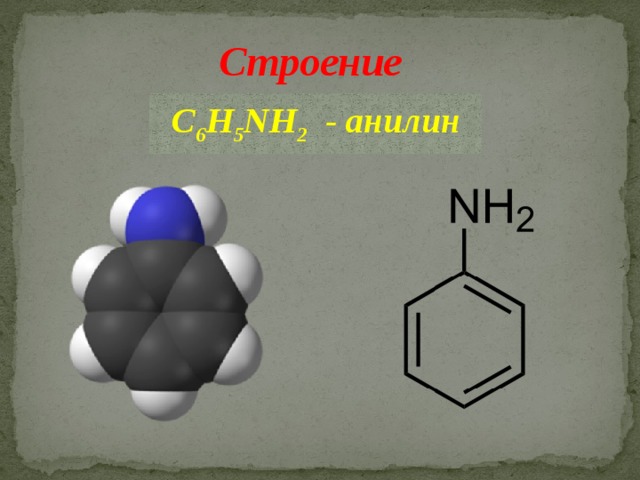
Строение
C 6 H 5 NH 2 - анилин

Физические свойства
- Анилин - бесцветная маслянистая жидкость.
- Немного тяжелее воды, малорастворим в ней.
- Хорошо растворяется в этаноле и бензоле.
- При окислении на воздухе становится светло-коричневого цвета.
- Температура кипения – 174 С.
- Проявляет слабые основные свойства.
- Ядовит.

Получение
В промышленности анилин получают в две стадии. На первой стадии бензол нитруется смесью концентрированной азотной и серной кислот при температуре 50 - 60°C в результате образуется нитробензол. На втором этапе нитробензол гидрируют при температуре 200-300°C в присутствии катализаторов.
C 6 H 5 NO 2 + 3Н 2 → C 6 H 5 NH 2 + 2Н 2 О.

Другим способом получение анилина является восстановление нитро соединений-
Реакция Зинина :
C 6 H 5 NO 2 + 3(NH 4 ) 2 S → C 6 H 5 NH 2 +
6NH 3 + 3S + 2H 2 O

Применение
- В настоящий момент в мире основная часть (85%) производимого анилина используется для производства метилдиизоционатов (MDI), используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуков (9%), гербицидов (2%) и красителей (2%).
- В России он в основном применяется в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты).

2.6. Контрольные вопросы
1. Вещество CH 3 -NH-CH(CH 3 ) 2 относится к ряду …
алифатических аминов
ароматических аминов
амидов
нитросоединений
2. Вещество, формула которого имеет вид C 6 H 5 -N(CH 3 ) 2 , называется …
анилин
диметилфениламин
диметилнитробензол
диметилфенол

2.6. Контрольные вопросы
3. Какую реакцию на индикатор показывают амины жирного ряда?
кислотную
нейтральную
щелочную
не действуют на индикатор
4. Характерной химической реакцией аминов, обусловленной наличием в их молекулах аминогруппы, является …
электрофильное присоединение
радикальное замещение
взаимодействие с кисло-тами с образованием солей
нуклеофильное присоединение

2.6. Контрольные вопросы
5. Какие реакции характерны для анилина?
а) C 6 H 5 NH 2 + Br 2 б) C 6 H 5 NH 2 + NaOH
в) C 6 H 5 NH 2 + HCl г) C 6 H 5 NH 2 + C 6 H 6
г
б, г
б
а, в
6. Определите массу хлорида фениламмония, если к анилину массой 13,95 г добавили хлороводород, выделившийся на первой стадии хлорирования метана объемом 5 л (при н.у.).
21,2 г
18,2 г
19,4 г
17,5 г

Материал, используемый для оформления презентации.
http:// cnit.ssau.ru/organics/chem5/pic/n2322.gif
http:// cnit.ssau.ru/organics/chem5/pic/n2321.gif
http:// www.chemistry.ssu.samara.ru/chem2/pic/viurtc1.jpg
http:// www.krugosvet.ru/images/1001120_1120_201.jpg
http:// rpp.nashaucheba.ru/pars_docs/refs/54/53936/img23.jpg
http:// 900igr.net/datas/khimija/KHimija-aminy/0012-012-Primenenie-aminov.jpg
http:// msize.ru/wp-content/uploads/2012/04/pigmenty2.jpg

Информация для педагога.
Учебный материал рассчитан на учащихся 10 класса общеобразовательной школы. Может использоваться:
- При изучении нового программного материала органической химии;
- При организации дистанционного обучения;
- На уроке обобщении для повторения основных понятий и умозаключений темы «Азотсодержащие соединения»
Цор соответствует УМК О.С.Габриеляна.

 Получите свидетельство
Получите свидетельство Вход
Вход











 Азотсодержащие соединения.АМИНЫ И АНИЛИН (1.66 MB)
Азотсодержащие соединения.АМИНЫ И АНИЛИН (1.66 MB)
 0
0 1480
1480 94
94 Нравится
0
Нравится
0


