Масса молекул. Количество вещества
Цели урока:
обучающая: Познакомится с важнейшими величинами, которые используются в молекулярной физике. Понять физический смысл каждой из этих величин и определить их взаимосвязь.
развивающая: развитие умения применять полученные знания на практике, научится пользоваться таблицей Менделеева для решения задач по молекулярной физике.
воспитывающая: воспитание дисциплины и норм поведения, творческого отношения к изучаемому предмету; стимулировать активность учащихся, повышать мотивацию к изучению физики.
Методы:
словесный — беседа;
наглядный — видеоурок;
контролирующий — решение задач с использованием наглядных примеров
Ход урока:
1. Организационный этап.
Добрый день. Прежде чем мы приступим к уроку, хотелось бы, чтобы каждый из вас настроился на рабочий лад.
2. Актуализация знаний.
Совсем недавно мы приступили к изучению молекулярной физики. На сегодняшнем уроке мы дадим представление о массе молекул, а также введем совершенно новую величину, которая называется количеством вещества.
3. Объяснение нового материала.
Как вы понимаете, масса и размеры молекул крайне малы. Например, в одном стакане воды содержится просто огромное количество молекул.
Поэтому, для удобства вводится такая величина, как относительная молекулярная масса. Эта величина определяется как отношение массы молекулы (или атома) данного вещества к одной двенадцатой массы атома углерода. Таким образом, массы всех химических элементов можно выразить в атомных единицах массы.

В таблице Менделеева собраны данные обо всех известных химических элементах. В частности, из этой таблицы можно узнать относительную молекулярную массу. На примере соляной кислоты мы научимся, как вычислять относительную молекулярную массу любого соединения с помощью таблицы Менделеева.
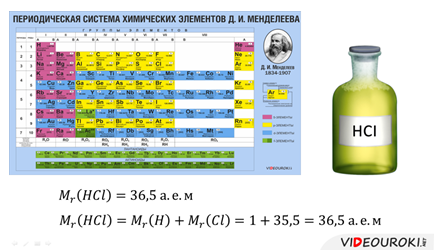
Помимо характеристики массы молекул, необходимо характеризовать и количество молекул, содержащихся в той или иной массе данного вещества. Для этого вводится такая величина, как количество вещества. Единицей измерения этой величины является моль. Один моль — это количество вещества, в котором содержится столько же молекул или атомов, сколько содержится атомов в двенадцати граммах углерода.

В связи с этим, вводится еще одна величина, которая называется молярной массой. Молярная масса — это масса данного вещества, взятого в количестве один моль. Эта величина измеряется в килограммах на моль.

Молярную массу также можно взять из таблицы Менделеева. Только обязательно нужно помнить о том, что в таблице Менделеева молярная масса указана в граммах на моль. Ну и конечно, ни в коем случае нельзя путать относительную молекулярную массу с молярной массой, несмотря на то, что в таблице Менделеева эти величины численно равны.

4. Решение задач.
Ну и конечно, необходимо рассмотреть практическое применение полученных знаний, то есть, решение задач.
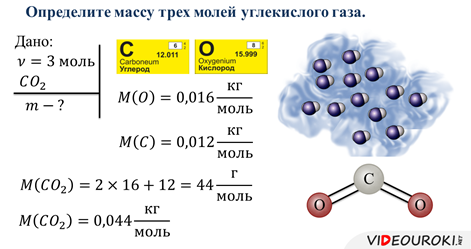
5. Рефлексия
Хотелось бы услышать ваши отзывы о сегодняшнем уроке: что вам понравилось, что не понравилось, чем бы хотелось узнать еще.
6. Домашнее задание.
7. Итоги урока
Получите комплекты видеоуроков + онлайн версии
Похожие записи
 30326
30326 Нравится
0
Нравится
0

 Получите свидетельство
Получите свидетельство Вход
Вход









