Производство серной кислоты контактным способом осуществляется из серосодержащих руд. На геофизической карте эти руды имеют соответствующее обозначение.

Самыми яркими примерами серосодержащих руд являются самородная сера, цинковая обманка, киноварь, свинцовый блеск, лимонит, пирит, или серный колчедан.


Самой распространённой рудой, из которой получают серную кислоту, является пирит, или серный колчедан. Добываемую руду доставляют на завод, где руда измельчается и подаётся на ленточный транспортёр, а затем сверху в печь для обжига пирита.
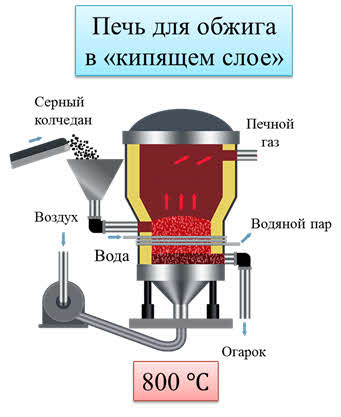
В печи температура достигает восьмисот градусов по цэльсию. Для того, чтобы мелкие частицы оставались в подвешенном состоянии, снизу нагнетается кислородо-воздушная смесь. Находясь в подвешенном состоянии, слой из мелких частиц напоминает кипящую жидкость, поэтому его и называют «кипящий слой». Реакция сгорания пирита является экзотэрмической, в результате образуется оксид серы четыре.

Отвод избыточного тепла осуществляется с помощью воды, циркулирующей по трубам вокруг печи. Забирая лишнее тепло от установки, вода переходит в пар. Образующийся в ходе сгорания руды огарок содержит оксиды железа и отправляется на завод для производства железа, а газообразная смесь, включающая сернистый газ поступает в следующий аппарат.
Сернистый газ после печи называют «печным (обжиговым) газом». Эта смесь содержит сернистый газ, крупные примеси, мелкие примеси и пары воды. Затем сернистый газ нужно очистить, чтобы удалить крупные примеси. Для этого используют аппарат циклон.
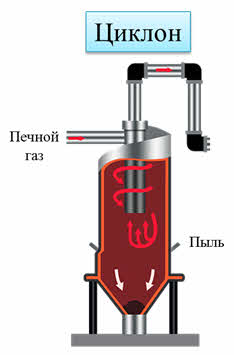
Попадая в него, газовая смесь начинает двигаться по спирали сверху вниз. Крупные частицы примесей отбрасываются к стенке и падают вниз.
Для удаления наиболее мелких пылинок, газовая смесь направляется в другой аппарат – электрофильтр.

В этом аппарате находятся металлические сетки, между которыми протянута мелкая проволока, к которой подведён постоянный электрический ток высокого напряжения. Мелкие пылинки притягиваются к сетке и падают в специальный бункер.
От водяных паров газовую смесь очищают в сушильной башне.
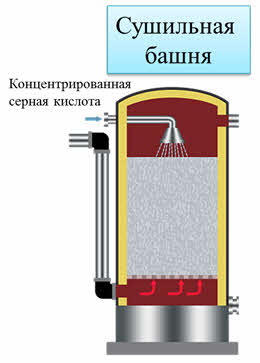
В эту башню газовая смесь поступает снизу. А сверху противотоком протекает концентрированная серная кислота. Для увеличения поверхности соприкосновения газа и жидкости башню заполняют керамическими кольцами.
Следующая фаза – это процесс окисления сернистого газа до серного ангидрида.
Эта реакция является экзотэрмической, обратимой и идёт в присутствии катализатора – оксида ванадия пять.

Осуществляется данный процесс в контактном аппарате. Сернистый газ в процессе очистки охлаждается, поэтому в контактном аппарате его подогревают, пропуская через теплообменник.
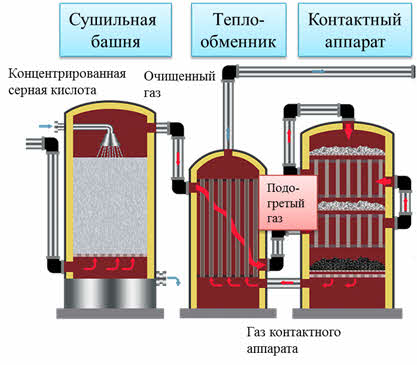
В роли подогревателя выступает газовая смесь, выходящая из контактного аппарата. Её пропускают по трубам теплообменника. А между ними в противоположном направлении пропускают сернистый газ.
Таким образом, достигается одновременно две цели: исходные вещества нагреваются, а продукты реакции охлаждаются до нужных температур. В контактном аппарате находятся полки, в которых слоями располагается катализатор – оксид ванадия пять, спрессованный в форме трубок. Охлаждённый в теплообменнике серный ангидрид направляется в поглотительную башню.
В поглотительной башне идёт процесс образования серной кислоты.
Оксид серы шесть в башне поглощается концентрированной серной кислотой, то есть серный ангидрид вступает в реакцию с водой, содержащейся в этой серной кислоте. Получается безводная серная кислота, в которой дополнительно растворим серный ангидрид, получается так называемый олеум.
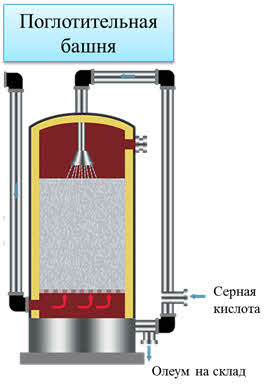
Получение серной кислоты контактным способом – непрерывный процесс. Образующийся таким образом олеум отправляется на склад.
Серная кислота применяется для производства минеральных удобрений, взрывчатых веществ, при травлении металлов, серную кислоту используют для получения минеральных кислот, органических красителей, химических волокон, при очистке нефтепродуктов и масел.

Рассмотрим производство аммиака.
В промышленности синтез аммиака осуществляют из азота и водорода. Высокая эффективность и мощность производства во многом зависит от применения катализаторов на всех стадиях производства.
В процессе производства аммиака используют воду, природный газ, атмосферный воздух. Азот для производства аммиака берут из воздуха, в котором около семидесяти восьми процентов его по объёму, а водород берут из природного газа.
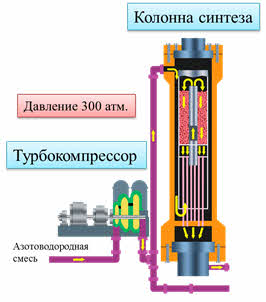
Азото-водородная смесь последовательно очищается от примесей и поступает в четырёхступенчатый компрэссор. Синтез аммиака идёт под давлением триста атмосфер.
Из компрэссора азото-водородная смесь через сепаратор и теплообменник поступает в колонну синтеза, где расположен катализатор.
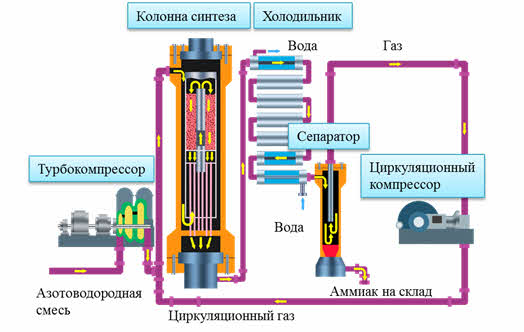
Катализатор – это: оксид железа два, оксид железа три, оксид алюминия, оксид калия, оксид кремния четыре.

Азото-водородная смесь нагревается выходящим из колонны газом и последовательно проходит в слои катализатора, где идёт образование аммиака.
Аммиак используется для получения минеральных удобрений, гербицидов, азотной кислоты, азотсодержащих органических веществ.

Таким образом, производство серной кислоты осуществляется контактным способом из серосодержащих руд. В промышленности аммиак получают синтезом азота и водорода. Серная кислота и аммиак находят широкое применение во многих областях народного хозяйства.

 Получите свидетельство
Получите свидетельство Вход
Вход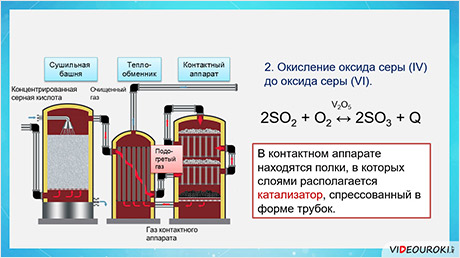




 7542
7542

