Оксиды неметаллов делят на несолеобразующие и солеобразующие. К несолеобразующим относят оксид кремния два, оксид азота один, оксид азота два, оксид углерода два.
Все остальные оксиды являются солеобразующими. Например, оксид фосфора пять, оксид хлора семь, оксид серы шесть, оксид серы четыре. Эти солеобразующие оксиды являются кислотными.
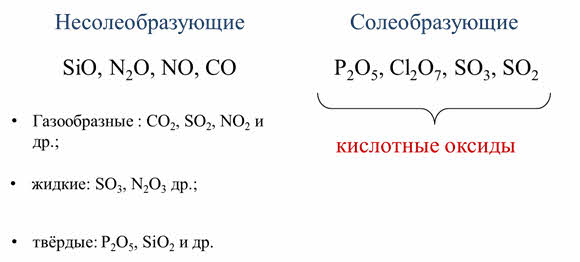
Среди них есть газообразные, как оксид углерода четыре, оксид серы четыре, оксид азота четыре и другие, а также жидкие, как оксид серы шесть, оксид азота три и другие; твёрдые, как оксид фосфора пять, оксид кремния четыре и другие.
Все кислотные оксиды – это ангидриды кислот. Например, оксид углерода четыре – ангидрид угольной кислоты, оксид фосфора пять – ангидрид фосфорной кислоты.
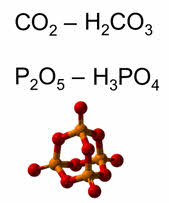
Все кислотные оксиды, кроме оксида кремния четыре, растворяются в воде с образованием гидроксидов, которые по характеру являются кислотами. При растворении оксида фосфора пять в воде образуется фосфорная кислота.
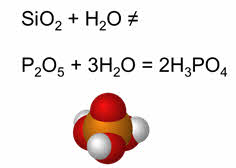
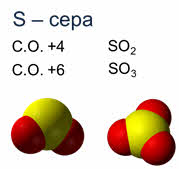
В оксидах неметаллов элемент-неметалл имеет положительные степени окисления, причём этих степеней окисления может быть несколько и тогда неметалл может образовывать несколько оксидов.
Например, сера в степени окисления плюс четыре образует оксид серы четыре, в степени окисления плюс шесть – оксид серы шесть, азот также имеет несколько степеней окисления.
Так, азот в степени окисления плюс один образует оксид азота один, азот в степени окисления плюс два образует оксид азота два, азот в степени окисления плюс три – оксид азота три, в степени окисления плюс четыре – оксид азота четыре, в степени окисления плюс пять – оксид азота пять.

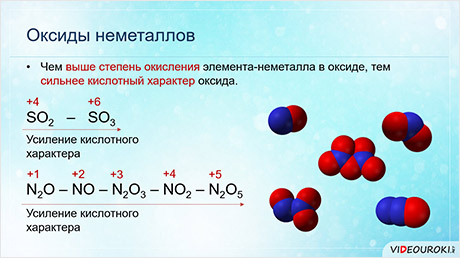
Чем выше степень окисления элемента-неметалла в оксиде, тем сильнее кислотный характер оксида. Так кислотные свойства оксида серы шесть выражены сильнее, чем оксида серы четыре.
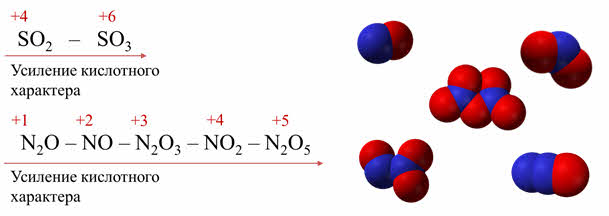
Тоже самое наблюдается в ряду оксидов азота: начиная с оксида азота один до оксида азота пять идёт усиление кислотных свойств оксидов, так как увеличивается степень окисления элемента-неметалла.
Оксиды неметаллов – это соединения с полярной ковалентной связью. Кристаллические решётки у этих оксидов могут быть молекулярные, как у оксида углерода четыре, оксида серы шесть, и атомные, как у оксида кремния четыре.
По периоду слева направо усиливается кислотный характер оксида. Так у оксида серы шесть кислотные свойства выражены сильнее, чем у оксида кремния четыре, так как по периоду также увеличивается высшая степень окисления элементов-неметаллов в соединениях.
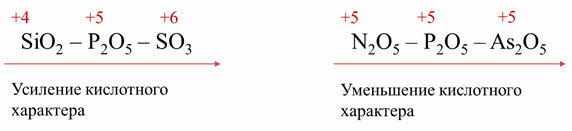
В группах главных подгруппах сверху вниз кислотный характер оксидов ослабевает, поэтому в пятой A группе кислотные свойства оксида азота пять будут выражены сильнее, чем у оксида мышьяка пять. Так как в группе сверху вниз увеличивается радиус иона неметалла, но степень окисления не изменяется.
Таким образом, все солеобразующие оксиды, образованные неметаллами, обладают кислотными свойствами, а сила кислотного оксида зависит от степени окисления неметалла и его радиуса атома.
Оксидам неметаллов соответствуют гидроксиды – кислородсодержащие кислоты. Изменение силы кислоты зависит от степени окисления неметалла, радиуса атома.
Например, оксидам азота три и пять соответствуют кислоты – азотистая и азотная. Азотная кислота является более сильной, чем азотистая и-за того, что в азотной кислоте степень окисления азота плюс пять, а в азотистой плюс три.
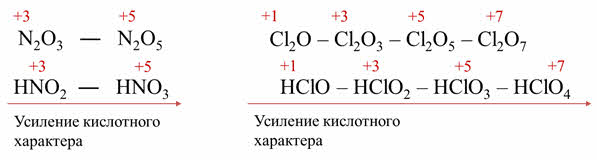
Кислотные свойства оксидов хлора также усиливаются с увеличение степени окисления атома хлора, поэтому и сила кислоты, которой соответствует данный оксид, также будет увеличиваться. Поэтому в ряду от хлорноватистой до хлорной кислоты идёт увеличение силы кислоты.
Таким образом, в периодах слева направо идёт увеличение заряда ядра атома неметалла, поэтому наблюдается усиление кислотных свойств гидроксидов, образованных оксидами неметаллов.

Например, хлорная кислота является более сильной, чем кремниевая, потому что степень окисления хлора в хлорной кислоте плюс семь, а кремния в кремниевой кислоте плюс четыре, а радиус иона неметалла уменьшается от кремниевой до хлорной кислоты.
В группах сверху вниз кислотный характер гидроксидов, образованных оксидами неметаллов, ослабевает. Например, серная кислота является более сильной, чем тэллуровая, так как радиус иона неметалла в этом ряду возрастает, а степень окисления неметалла не изменяется, и остаётся плюс шесть.

Все оксиды и гидроксиды, образованные элементами в максимальной степени окисления всегда окислители. Так, в реакции оксида серы шесть с сероводородом сера в степени окисления плюс шесть понижает свою степень окисления до плюс четырёх, поэтому оксид серы шесть выступает в роли окислителя, в реакции серной кислоты с медью, серная кислота также является окислителем, потому что сера понижает свою степень окисления с плюс шести до плюс четырёх.
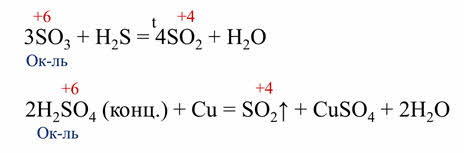
Если же в оксиде или гидроксиде элемент-неметалл проявляет промежуточную степень окисления, то эти соединения могут быть и окислителями, и восстановителями.
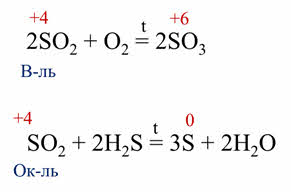
Так, в реакции оксида серы четыре с кислородом образуется оксид серы шесть. Оксид серы четыре в данной реакции является восстановителем, так как сера повышает свою степень окисления с плюс четырёх до плюс шести. В реакции оксида серы четыре с сероводородом, образуется сера и вода. В этой реакции оксид серы четыре является окислителем, так как сера понижает свою степень окисления с плюс четырёх до нуля.
Водородные соединения неметаллов представляют собой газообразные соединения, кроме воды. Они летучие и легкоподвижные, быстроиспаряемые.
Электроотрицательность неметаллов больше электроотрицательности водорода, поэтому в водородных соединениях неметаллы проявляют минимальную отрицательную степень окисления: углерод — минус четыре, азот — минус три, фосфор — минус три и так далее.
Водородные соединения неметаллов проявляют основные, кислотные или амфотэрные свойства. Водородные соединения неметаллов являются, как правило, сильными восстановителями.
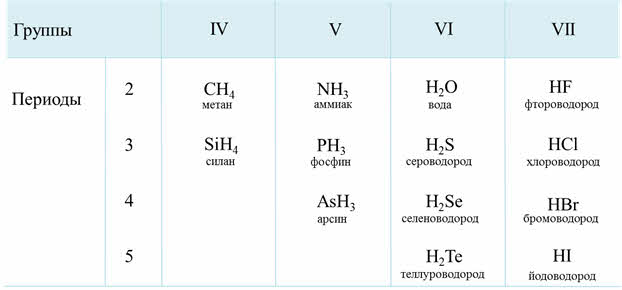
Так, углероду соответствует водородное соединение цэ-аш-четыре – метан, кремнию – силан, азоту – аммиак, фосфору – фосфин, мышьяку – арсин, кислороду – вода, сере – сероводород, селену – селеноводород, тэллуру – тэллуроводород, фтору – фтороводород, хлору – хлороводород, брому – бромоводород, йоду – йодоводород.
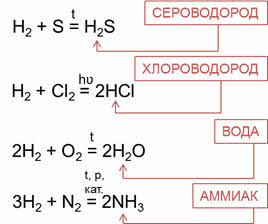
Водородные соединения неметаллов можно получить непосредственно взаимодействием неметалла с водородом. Сероводород можно получить реакцией водорода с серой, хлороводород – реакцией водорода с хлором, воду – реакцией водорода и кислорода, аммиак – реакцией водорода и азота.
В водородных соединениях присутствует ковалентная полярная связь, они имеют молекулярную кристаллическую решётку.
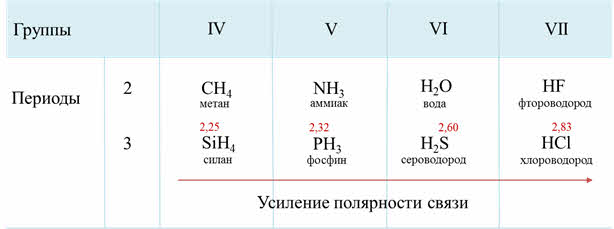
Как известно, электроотрицательность усиливается по периоду слева направо, поэтому полярность связи в водородных соединениях возрастает, а в группах сверху вниз электроотрицательность уменьшается, поэтому и полярность связи будет уменьшаться.
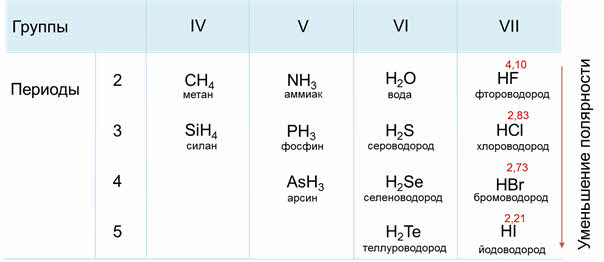
Если рассмотреть третий период, то от силена до хлороводорода будет наблюдаться усиление полярности связи из-за увеличения электроотрицательности неметаллов.
В седьмой A группе сверху вниз будет идти уменьшение полярности связи от фтороводорода к йодоводороду, потому что идёт уменьшение электрооотрицательности элемента-неметалла в водородном соединении.
Полярность связи влияет на растворимость водородного соединения в воде. Например, так как молекула воды сильно полярна, то возникает сильное межмолекулярное взаимодействие с образованием водородных связей.
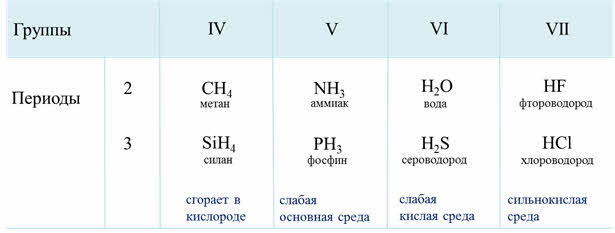
Если рассмотреть водородные соединения неметаллов третьего периода, то здесь можно проследить следующую закономерность: при растворении в воде силана не наблюдается проявление кислотно-основного характера соединения, он сразу сгорает в кислороде, фосфин в воде даёт слабую основную среду, сероводород – слабую кислую среду, а хлороводород – сильнокислую среду. Это объясняется тем, что от силана до хлороводорода радиус иона неметалла уменьшается, а заряд ядра увеличивается, полярность связи в молекулах возрастает, поэтому усиливаются кислотные свойства.
В группах сверху вниз кислотные свойства водородных соединений неметаллов усиливаются, так как прочность связи водород-элемент уменьшается, из-за увеличения длины связи.
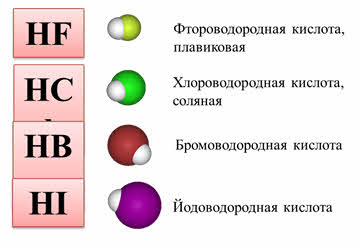
Например, водородные соединения седьмой A группы: хлороводород, бромоводород, йодоводород в воде – это сильные кислоты, которые полностью диссоциируют. Из этих кислот самой слабой является фтороводородная. Это объясняется тем, что у фтора самый маленький радиус, кроме этого, в этой молекуле присутствуют межмолекулярные водородные связи.
Таким образом, в периодах и группах главных подгруппах с увеличением заряда ядер элементов-неметаллов усиливаются кислотные свойства, а ослабевают основные свойства.
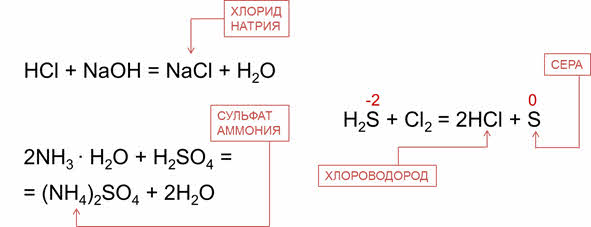
Например, водный раствор хлороводорода – проявляет кислотные свойства, поэтому реагирует со щелочами. Так, в реакции соляной кислоты с гидроксидом натрия образуется соль – хлорид натрия и вода. Водный раствор аммиака проявляет основные свойства, поэтому реагирует с кислотами. Так, в реакции аммиака с серной кислотой образуется сульфат аммония и вода.
Как было сказано, водородные соединения неметаллов проявляют восстановительные свойства, так как элемент-неметалл здесь в минимальной степени окисления. Например, в реакции сероводорода с хлором сероводород является восстановителем, потому что сера повышает свою степень окисления с минус двух до нуля.
Таким образом, все солеобразующие оксиды, образованные неметаллами, обладают кислотными свойствами, а сила кислотного оксида зависит от степени окисления неметалла и радиуса иона. В периодах слева направо кислотный характер гидроксидов, образованных оксидами неметаллов усиливается, а в группах сверху вниз кислотный характер гидроксидов ослабевает. В периодах слева направо кислотные свойства летучих водородных соединений элементов в водных растворах усиливаются. В группах сверху кислотные свойства водородных соединений увеличиваются. Водородные соединения неметаллов, обладающие в водных растворах кислотными свойствами, реагируют со щелочами. Водородные же соединения неметаллов, обладающие в водных растворах основными свойствами, реагируют с кислотами.

 Получите свидетельство
Получите свидетельство Вход
Вход




 19683
19683

