В нем металл и кислород,
Да еще плюс водород,
И такое сочетание
Называют основание.
Основания – это сложные вещества, состоящие из атомов металла и гидроксогруппы. Гидроксогруппа – это группа ОН.
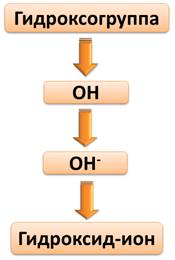
Степень окисления О (-2), Н (+1), поэтому суммарный заряд этого иона (1-). Т.е. гидроксогруппа представляет собой сложный ион, который еще называют гидроксид-ионом.
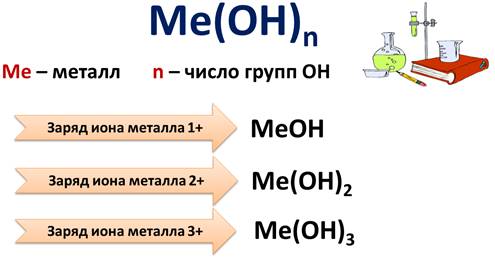
Состав оснований можно записать формулой Ме(ОН)n, где Ме – это металл, а n – число групп ОН.
Если заряд иона металла 1+, то с ионом металла связана 1 группа ОН-, формула таких оснований будет МеОН, а если заряд иона металла 2+, то с ионом металла связано 2 группы ОН- и формула таких оснований будет Ме(ОН)2 и т.д.
Название оснований состоит из слова гидроксид + название металла в родительном падеже. Например, КОН – гидроксид калия, Ва(ОН)2 – гидроксид бария, Al(OH)3 – гидроксид алюминия.

Если металл проявляет переменную степень окисления, то после названия в скобках римскими цифрами ставят численное значение степени окисления. Например: Cu(OH)2 – гидроксид меди (II), Fe(OH)3 – гидроксид железа (III), Mn(OH)2 – гидроксид марганца (II).
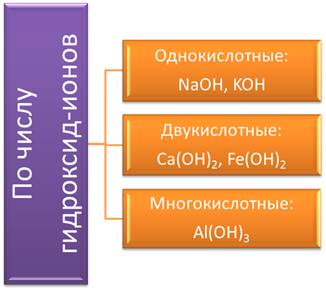
По числу гидроксид-ионов основания подразделяют на: однокислотные, в формулах которых 1 гидроксид-ион (NaOH, KOH); двукислотные, в формулах которых 2 гидроксид-иона (Ca(OH)2, Fe(OH); многокислотные основания, в которых три и более гидроксид-ионов (Al(OH)3).
По растворимости в воде основания делятся на растворимые в воде, или щёлочи и нерастворимые в воде. Растворимыми основаниями являются основания, образованные металлами I A группы и некоторыми металлами II A группы. Например, NaOH, Ba(OH)2, KOH. Растворимые в воде основания хорошо растворяются в воде, не образуя, осадка, а нерастворимые, наоборот, выпадают в виде осадка и нерастворимы в воде. Например, Cu(OH)2, Al(OH)3, Fe(OH)2.
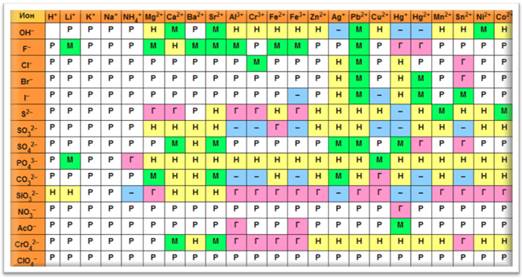
Для того чтобы определить растворимо или нерастворимо основание в воде, можно воспользоваться таблицей растворимости. Если в таблице на пересечении иона металла и гидроксид-иона стоит буква «Р», значит, это основание растворимо в воде, если на пересечении стоит буква «М», значит, основание мало растворимо в воде, а если буква «Н», значит, основание нерастворимо в воде.
Таблица растворимости
Рассмотрим некоторые щёлочи. Одной из наиболее распространённых щелочей является гидроксид натрия – NaOH. Это твердое белое вещество, гигроскопично, т.е. поглощает влагу из воздуха, поэтому оно расплывается на воздухе, хорошо растворимо в воде с выделением тепла.
Раствор гидроксида натрия мыльный на ощупь и очень едкий, поэтому его ещё называют едкий натр. Он разъедает ткани, кожу, бумагу и др. органические материалы. С гидроксидом натрия и его раствором обращаться нужно осторожно, при попадании на кожу вызывает долго не заживляющие раны. Гидроксид натрия широко используется в мыловарении, кожевенной, фармацевтической промышленности, бумажной и текстильной промышленности. Его техническое название – «каустическая сода».
Гидроксид калия – КОН – является тоже твердым белым веществом, которое хорошо растворимо в воде, при этом выделяется большое количество теплоты.
Его раствор мыльный на ощупь и очень едкий, поэтому гидроксид калия тоже называют едкое кали. Его применяют при производстве мыла и тугоплавкого стекла.
Гидроксид кальция Са(ОН)2 называют еще гашёной известью. Его получают реакцией негашёной извести с водой. Гидроксид кальция представляет собой рыхлый белый порошок, малорастворимый в воде. Этот гидроксид используют при кладке и штукатурке стен, побелке деревьев, для получения хлорной извести.
Прозрачный раствор гидроксида кальция называют известковой водой. Если через нее пропустить углекислый газ, то она помутнеет, вследствие образования нерастворимого карбоната кальция. Эта реакция является качественной на углекислый газ. Качественные реакции – это реакции, с помощью которых распознают определенные вещества. Следовательно, углекислый газ распознают по помутнению известковой воды.
Для того чтобы определить щёлочи, используют специальные вещества, которые называют индикаторами. Индикаторы – это вещества, которые изменяют свою окраску под действием различных веществ. Сравним окраску индикаторов в нейтральной среде, или в воде и в растворах щелочей.
Наиболее распространенными индикаторами являются: лакмус, метиловый оранжевый и фенолфталеин. В нейтральной среде лакмус – фиолетовый, метиловый оранжевый – оранжевый, фенолфталеин – бесцветный.
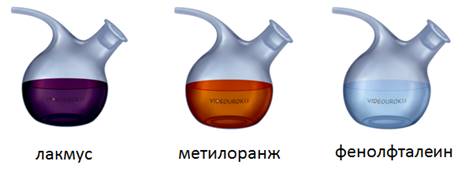
Если мы капнем в щелочь лакмуса, то он станет синим, метиловый оранжевый – желтым, а фенолфталеин и вовсе станет малиновым. Поэтому c помощью индикаторов можно отличить щелочи от других классов соединений.
Изменение окраски индикаторов в зависимости от среды


 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 17141
17141


