Следует различать массу и количество: 2 кг яблок – это масса, а 2 яблока – это количество. В жизни мы часто используем определённые порции, например, коробок спичек или мешок зерна, ведь никто из нас не будет поштучно покупать спички или зерно.
В химии для измерения количество вещества была выбрана единица, которая объединила в себе число частиц и массу. Эта единица называется моль и обозначается буквой n (эн). Чтобы измерить 1 моль любого вещества, нужно взять его столько грамм, какова относительная атомная или относительная молекулярная масса вещества.
Давайте посмотрим на вещества количеством один моль: сравните, как отличается 1 моль воды, соли, кислоты и сахара. Почему? У этих веществ различная относительная молекулярная масса. У воды – 18, соли – 58,5, кислоты – 98, а сахара – 332, поэтому и масса вещества их тоже различна.

Например, 1 моль воды имеет массу 18 г, т.к. относительная молекулярная масса вода равна 18; 1 моль азота имеет массу 28 г, потому что относительная молекулярная масса его равна 28; 1 моль меди равен 64 г, т.к. относительная молекулярная масса ее равна 64.
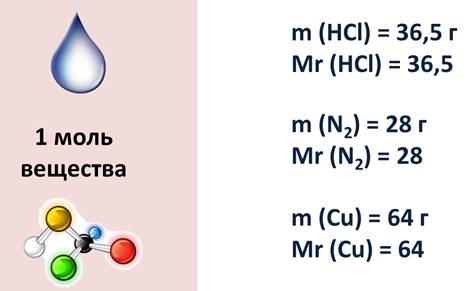
А если нам нужно узнать, какую массу имеет вода количеством 2 моль, то мы 2 умножим на 18, т.е. 36 г; 0,5 моль азота имеет массу 14 г, т.к. 0,5 умножить на 28, будет 14.
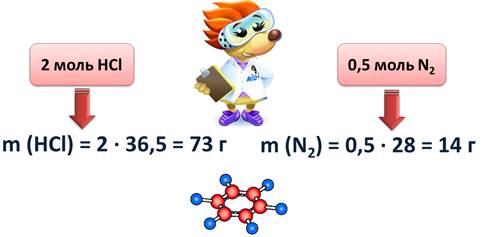
Количество вещества не только связано с массой, но и с числом частиц.
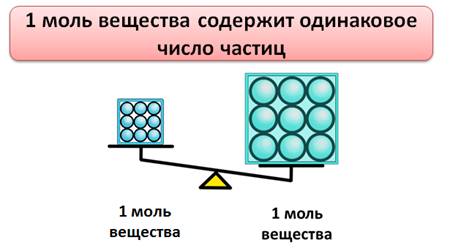
Установлено, что 1 моль любого вещества содержит одинаковое число частиц. Это число равно 6,02 · 1023. Это число называется постоянной Авогадро, в честь итальянского ученого А. Авогадро и обозначается оно NA.
<![if !vml]><![endif]>
Т.е. 1 моль воды имеет массу 18 г и содержит 6,02 · 1023 частиц; 2 моль воды имеет массу 36 г и содержит 12,04 · 1023 частиц; 0,5 моль азота имеет массу 14 г и содержит 3,01 · 1023 частиц.

Для того чтобы узнать число частиц (N), которое содержится в определенном количестве вещества, можно использовать формулу:
N = NA · n
где n – количество вещества, т.е. число молей; N – число частиц.
Из этой формулы верны и следующие выражения:
NA = N/ n
n = N/ NA
Теперь дадим определение понятия моль – это такое количество вещества, в котором содержится 6,02 · 1023 частиц этого вещества.
Используя новые формулы, решим задачи.
1. Определите количество вещества кислорода, в котором содержится 18,06 · 1023 молекул.
Нам дано число молекул кислорода, найти нужноколичество вещества кислорода. Для решения этой задачи используем формулу n = N/ NA, подставляем значения в выражение и находим результат (величина NA является потоянной). Получается 3 моль. Следовательно, количество кислорода равно 3 моль.

2. Определите число молекул хлора (Cl2) которое, содержится в порции этого газа количеством вещества 0,1 моль.
В этой задаче по условию нам дано количество вещества хлора. Найти нужно число молекул. Следовательно, используем формулу N = NA · n, подставим данные в формулу, получаем результат 0,602 · 1023 молекул. Получается, что порция хлора количеством 0,1 моль содержит 0,602 · 1023 молекул.


 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 23617
23617

