
Тема 1.2. «Свойства основных ЭТМ»
Предмет «ЭМВ»
Преподаватель Арсламбекова О.Г.

The role of this topic in the study of the discipline

- tasks:
- teaching
- developmental
- educative

homework:
- «МВ и СД»»
с.3
https://learningapps.org/myapps.php

questions:
- 1. Общие понятия
- 2. Физико-химическая природа материалов.
- 3. Анализ химических связей.
- 4.Типы химических связей

- все материалы в интересующей нас области техники должны обладать вполне определенным набором свойств, благодаря которым они находят конкретное применение.

- Объединяющее началом всех ЭТМ- набор их свойств по отношению к эл.магнитному полю.
- При взаимодействии с эл.магнитным полем проявляются электрические и магнитные свойства.
- Это позволяет дать определение понятия «электротехнические материалы» и классифицировать их.

ФИЗИКО-ХИМИЧЕСКАЯ ПРИРОДА МАТЕРИАЛОВ
- Все существующие в природе материалы независимо от их агрегатного состояния (газообразные, жидкие, твердые) построены из атомов более чем 100 химических элементов.
- Любое вещество (материал) состоит из огромного количества электрически заряженных частиц — электронов и атомных ядер химических элементов, которые и определяют его свойства.

- Существуют способы упрощенного анализа свойств материалов, позволяющие использовать часть макроскопических характеристик, полученных экспериментально.
- При этом наиболее существенные особенности взаимодействия между электронами и ядрами химических элементов, образующих вещество, учитываются интегрально или автоматически.

анализ химических связей элементов вещества
- Различия типов веществ обусловлены различием в характере распределения электронов в атомах и молекулах, и особенно в характере распределения наиболее удаленных от ядра валентных электронов и ионных атомных остовов.
- Сопоставляя между собой расположение атомов в структуре вещества, электронную конфигурацию этих атомов, тип химической связи между ними, можно ответить на ряд важных вопросов таких, как электропроводность, способность к намагничиванию, плотность, твердость, пластичность, температура плавления и т.д.

По характеру взаимодействия между частицами, составляющими вещество, различают шесть типов химической связи:
- 1. ковалентная неполярная;
- 2. ковалентная полярная, или гомеополярная;
- 3. ионная, или гетерополярная;
- 4. донорно-акцепторная;
- 5. металлическая;
- 6. межмолекулярная.

Ковалентная неполярная связь
- характерна для диэлектриков и полупроводников.

Соединения с гомеополярной связью
- могут быть диэлектриками (полимерные органические материалы) и полупроводниками.

Ионная связь
- характерна для диэлектриков.
- Ионные силы взаимодействия достаточно велики, поэтому вещества с ионной связью имеют сравнительно высокие механическую прочность, температуру плавления и испарения.
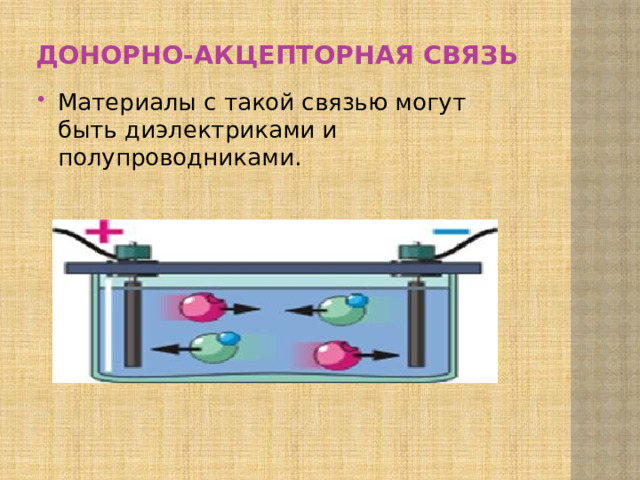
Донорно-акцепторная связь
- Материалы с такой связью могут быть диэлектриками и полупроводниками.

Металлическая связь
- возникает между атомами в металлах и является следствием обобществления всех валентных электронов, образующих электронный газ и компенсирующих заряд ионов кристаллической решетки.
- Поэтому уже при очень слабых внешних электрических полях проявляется высокая электропроводность металлов.

Межмолекулярная, или остаточная, связь
- характерна для веществ органического происхождения, например парафина.
- материалы имеют низкие температуру плавления и механические характеристики, свидетельствующие о непрочности молекулярной структуры вещества.

terms dictionary



Reflection:
Урок сегодня прошел
Я на уроке
1.
Итог
1.
2.
2.
3.
1. Понял материал
.2.Узнал больше, чем знал
3.
3.Не понял ничего

БІЛІМ АУКЦИОНЫ
AUCTION KNOWLEDGE

 Получите свидетельство
Получите свидетельство Вход
Вход












 Свойства основных электротехнических материалов (3.62 MB)
Свойства основных электротехнических материалов (3.62 MB)
 0
0 196
196 0
0 Нравится
0
Нравится
0


