
Берцелиус (Berzelius) Йенс Якоб (1779-1848)
Органические вещества

Долгое время считали, что органические вещества содержатся только в организмах

Александр
Михайлович
Бутлеров

- Какие теории предшествовали теории
А.М.Бутлерова?
2)В чем основная идея теории ?
3)Сформулируйте основные положения
теории А.М.Бутлерова.
4) Что такое изомерия и изомеры?
Сколько изомеров среди веществ?
а) СН 3 – О – СН 3
б) СН 3 - СН 2 ОН
в) СН 2 = СН 2
5)Какова роль теории строения органи-
ческих веществ в современной химии?

… ЭТО ОСОБЫЙ ХИМИЧЕСКИЙ ЭЛЕМЕНТ : ОН ОСНОВА МНОГООБРАЗИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ, ИЗ КОТОРЫХ ПОСТРОЕНЫ ВСЕ ЖИВЫЕ ОРГАНИЗМЫ.
Д.И.Менделеев

Строение атома углерода. Валентные состояния атома углерода.
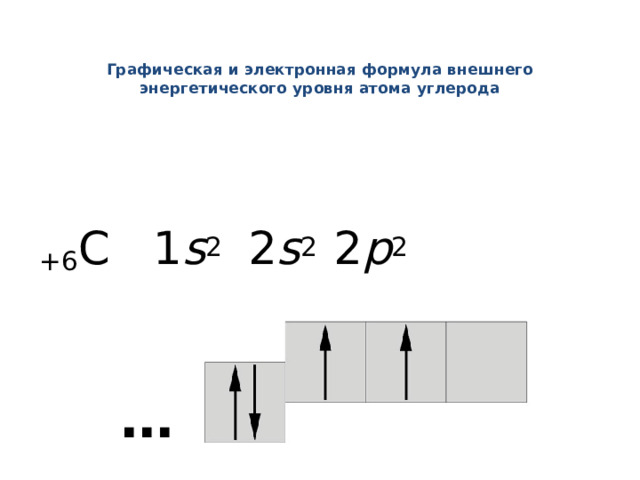
Графическая и электронная формула внешнего энергетического уровня атома углерода
+6 С 1 s 2 2 s 2 2 p 2
……
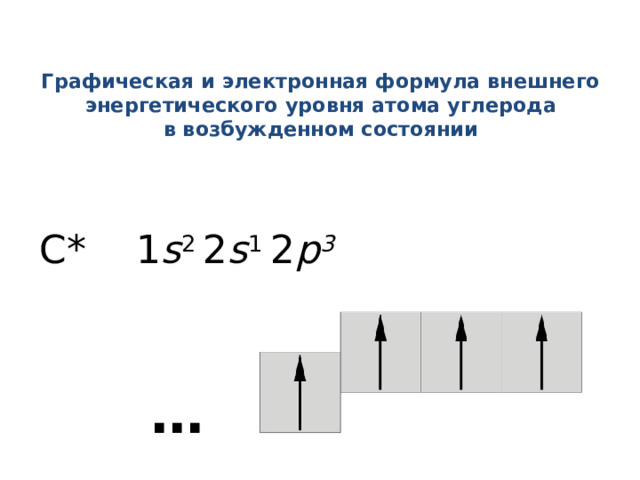
Графическая и электронная формула внешнего энергетического уровня атома углерода в возбужденном состоянии
С* 1 s 2 2 s 1 2 p 3
1 s -электрон и 3 p -электрона внешнего энергетического уровня атома углерода, то, следовательно, химические связи должны быть неравноценными по прочности и длине.
……

- Гибридизация – взаимное выравнивание электронных облаков в атоме углерода (Л.Полинг, 20-е годы XX века )
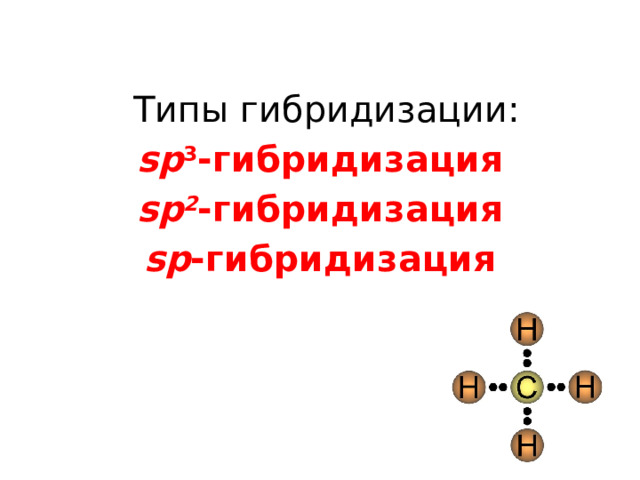
Типы гибридизации:
sp 3 -гибридизация
sp 2 -гибридизация
sp -гибридизация
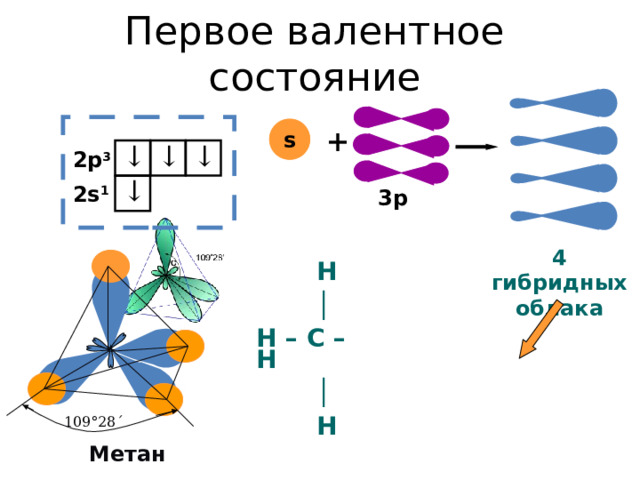
Первое валентное состояние
s
+
↓
↓
↓
2p 3
↓
2s 1
3p
4 гибридных облака
Н
│
Н – С – Н
│
Н
109 °28´
Метан
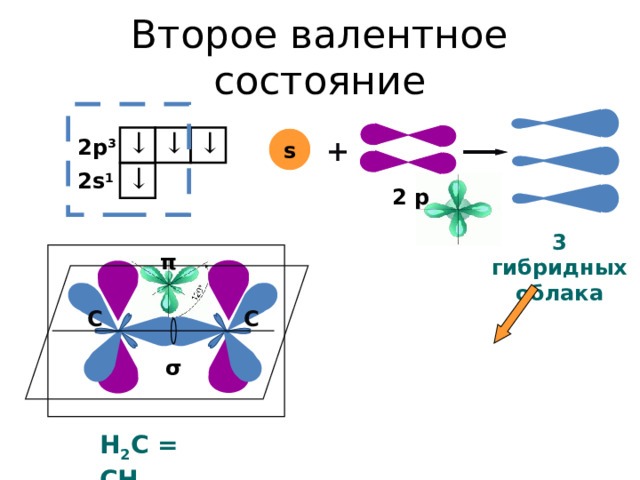
Второе валентное состояние
↓
↓
↓
s
+
2p 3
↓
2s 1
2 p
3 гибридных облака
π
C C
σ
Н 2 С = СН 2
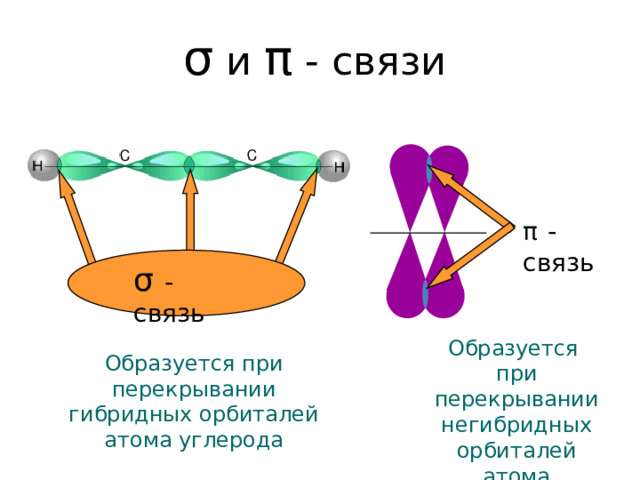
σ и π - связи
π - связь
σ - связь
Образуется при перекрывании негибридных орбиталей атома углерода
Образуется при перекрывании гибридных орбиталей атома углерода
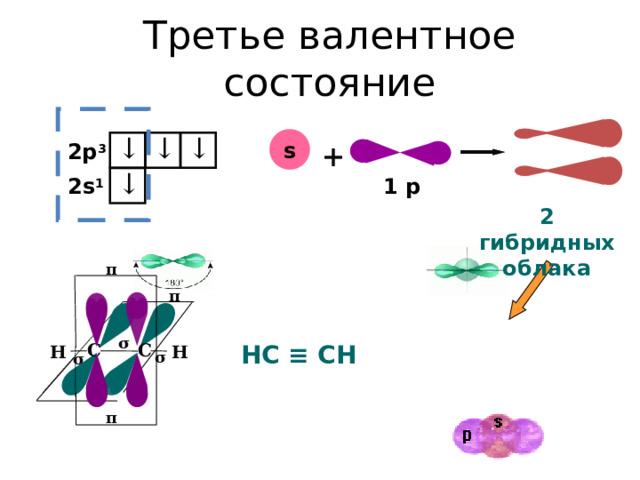
Третье валентное состояние
↓
↓
↓
s
+
2p 3
↓
2s 1
1 p
2 гибридных облака
π
π
σ
С
С
НС ≡ СН
Н
Н
σ
σ
π
π

Определите гибридное состояние каждого атома углерода, число сигма- и пи-связей в молекулах веществ:
1) СН 3 – СН 2 – СН 3
2) СН 2 = СН – СН = СН 2
3) СН 2 = СН 2

1) Что такое гибридизация? Какие бывают типы гибридизации?
2) Какие типы перекрывания электронных облаков есть у атома углерода?

1. Каких веществ на Земле больше?
а) органических; б) неорганических; в) одинаково; г)амфотерных
2. Теорию химического строения органических веществ сформулировал:
а) Н.Н.Зинин; б) Ф.Велер; в) А.М.Бутлеров; г) Д.И.Менделеев.
3. Явление существования нескольких веществ одинакового состава, с одной и той же формулой, но с разным строением молекул – это:
а) амфотерность; б) гомология; в) изомерия; г) аллотропия
4 .Сколько изомеров среди веществ?
1) СН 3 –СН 2 –СН 2 ОН 2) СН 3 – О –СН 2 – СН 3 3) СН 2 = СН2
а) 1 б)2 в)3 г)0
5. Сколько пи - связей в формуле вещества СН 2 = СН2 ?
а) 1 б)2 в)3 г)0
Тест

Ответы на тестовые задания:
1 – а; 2 – в; 3 – в; 4 – б; 5 – а

Задание на дом:
п.3,4, № 1(с.25) устно; №1,3*(с.20-21), №2(с.25) письменно

 Получите свидетельство
Получите свидетельство Вход
Вход











 Строение атома углерода (11.23 MB)
Строение атома углерода (11.23 MB)
 0
0 649
649 24
24 Нравится
0
Нравится
0


