
Расскажу сегодня, что ли, О зловредной роли моли. Моль съедает шерсть и мех Просто паника у всех…. Ну а в химии- изволь! Есть другое слово «МОЛЬ»
21.02.19
Решение задач с использованием понятия «количество вещества»
8 класс
21.02.19
Кузнецова Ольга Александровна МОУ СОШ №7 г. Обнинск

Существует физическая величина, прямо пропорциональная числу частиц, составляющих данное вещество и входящих во взятую порцию этого вещества, которую называют количеством вещества ( ) .
![Молярная масса - это масса одного моля вещества . М= [ г/моль ] ( молярная масса численно равна относительной молекулярной массе ) , отсюда](https://fsd.videouroki.net/html/2019/02/21/v_5c6f03bec8ba6/img3.jpg)
Молярная масса
- это масса одного моля вещества .
М= [ г/моль ]
( молярная масса численно равна относительной молекулярной массе )
, отсюда
21.02.19
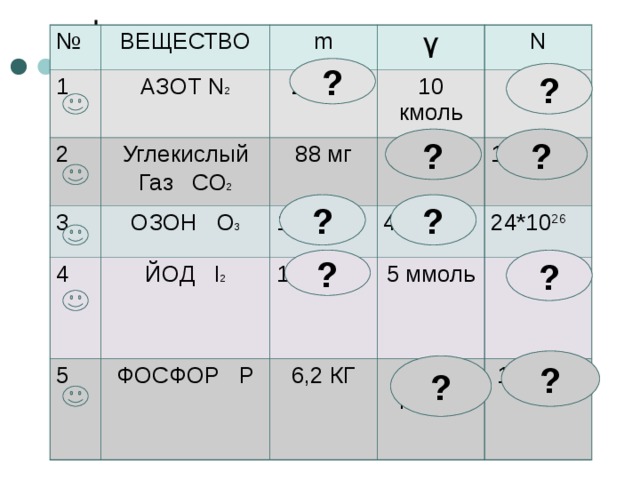
№
ВЕЩЕСТВО
1
АЗОТ N 2
2
m
Углекислый
Газ CO 2
۷
280 кг
3
ОЗОН O 3
10 кмоль
4
N
88 мг
5
6*10 27
ЙОД I 2
2 ммоль
192 кг
ФОСФОР P
1,27 г
4 кмоль
12*10 20
6,2 КГ
5 ммоль
24*10 26
3*10 21
0,2 кмоль
1,2*10 26
?
?
?
?
?
?
?
?
Решения задач открываются по гиперссылке – смайлу, последовательность действий по щелчку. Ответы к задачам открываются последовательно по щелчку на слайде №2.
?
?
21.02.19
Кузнецова Ольга Александровна МОУ СОШ №7 г. Обнинск

Дано:
۷ (N 2 ) = 10 кмоль
Найти:
m (N 2 ) - ?
N (N 2 ) - ?
Решение:
M (N 2 )= 28 кг/кмоль
m (N 2 )=10 кмоль*28 кг/кмоль = 280 кг
N(N 2 ) = 10 кмоль* 6*10 26 1/кмоль= 6*10 27
Ответ: m (N 2 )= 280 кг
N(N 2 ) = 6*10 2 7
21.02.19

Дано:
۷ (I 2 ) = 5 ммоль
Найти:
m - ?
N - ?
Решение:
M (I 2 )= 254 мг/ммоль
m (I 2 )= 5 ммоль*254мг/ммоль = 1270мг =1,27г
N(I 2 ) = 5 ммоль* 6*10 20 1/ммоль= 3*10 21
Ответ: m (I 2 )= 1,27г
N(I 2 ) = 3*10 21
21.02.19
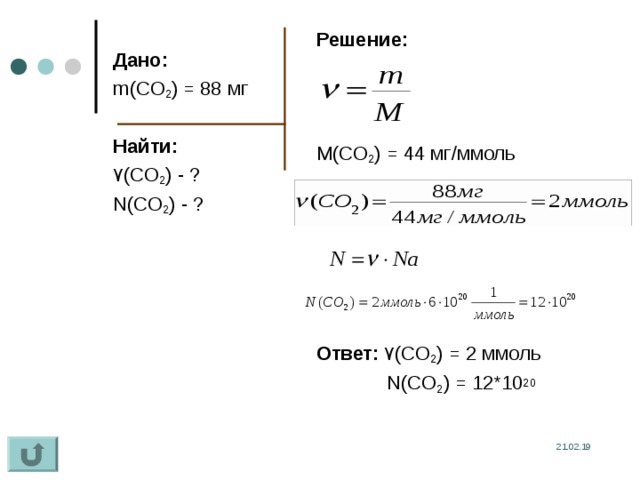
Решение:
M(CO 2 ) = 44 мг/ммоль
Ответ: ۷ (CO 2 ) = 2 ммоль
N(CO 2 ) = 12*10 20
Дано:
m(CO 2 ) = 88 мг
Найти:
۷ (CO 2 ) - ?
N(CO 2 ) - ?
21.02.19
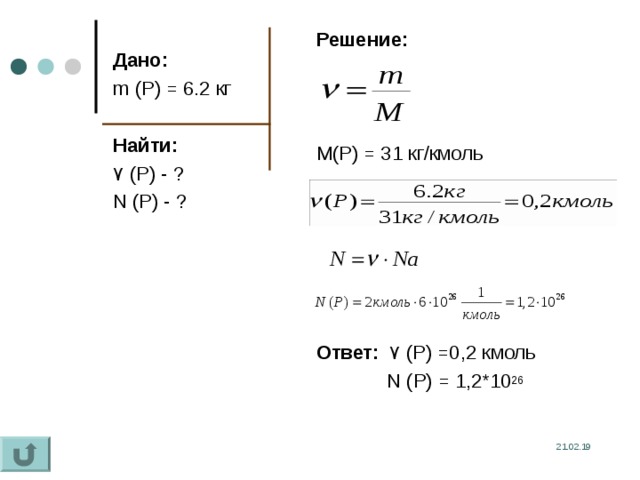
Решение:
M(P) = 31 кг/кмоль
Ответ: ۷ (P) =0 ,2 кмоль
N (P) = 1 , 2*10 26
Дано:
m (P) = 6.2 кг
Найти:
۷ (P) - ?
N (P) - ?
21.02.19
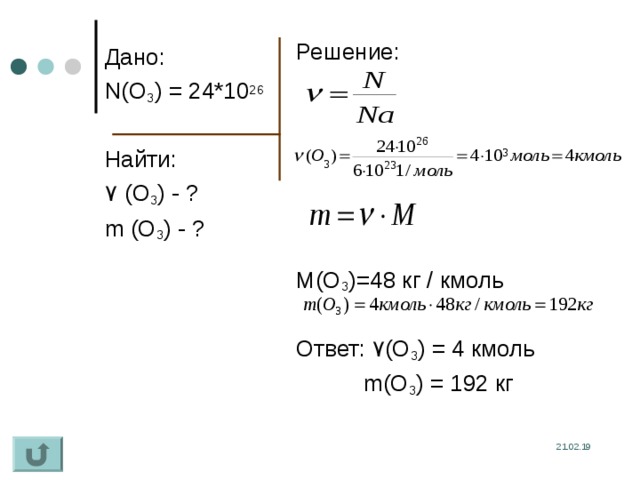
Решение:
М(О 3 )=48 кг / кмоль
Ответ: ۷ (O 3 ) = 4 кмоль
m(O 3 ) = 192 кг
Дано:
N(O 3 ) = 24*10 26
Найти:
۷ (O 3 ) - ?
m (O 3 ) - ?
21.02.19

Задачи (закрепление)
- Найдите число молекул в 2 молях водорода.
- Найдите массу 3 моль углекислого газа (СО2 )
- Рассчитайте массу 112 л водорода (н.у.)
- Что тяжелее: 2 моль СО2 или 2 моль СаО ?
- Найдите количество вещества серной кислоты ( H2SO4) массой 4,9 г
- Какой объем займет сернистый газ ( SO2) , масса которого равна 3,2 г?

 Получите свидетельство
Получите свидетельство Вход
Вход












 Решение задас с использованием величин Количество вещества и молярная масса (1.07 MB)
Решение задас с использованием величин Количество вещества и молярная масса (1.07 MB)
 0
0 504
504 38
38 Нравится
0
Нравится
0


