Областное государственное бюджетное образовательное учреждение
среднего профессионального образования
Ульяновский техникум приборостроения
РАБОЧАЯ ПРОГРАММА УЧЕБНОЙ ДИСЦИПЛИНЫ
Химия
270839.01 Монтажник санитарно-технических, вентиляционных систем и оборудования
151902.03 Станочник (металлообработка)
151903.02 Слесарь
140446.03 Электромонтер по ремонту и обслуживанию электрооборудования
( по отраслям)
Ульяновск- 2014 г.
| РЕКОМЕНДОВАНА
|
УТВЕРЖДАЮ |
| на заседании МК Председатель МК Л. А. Жукова Протокол заседания МК №_______ от «__»________20___г. | Заместитель директора по теоретическому обучению ОГБОУ СПО УТПС С.В.Кузнецова «__»________20___г.
|
Автор-разработчик:
Анчикова Лариса Федоровна – преподаватель химии и биологии
Рецензент:
Рабочая программа разработана в соответствии с «Рекомендациями по реализации образовательной программы среднего (полного) общего образования в образовательных учреждениях начального профессионального и среднего профессионального образования в соответствии с федеральным базисным учебным планом и примерными учебными планами для образовательных учреждений Российской Федерации, реализующих программы общего образования» (письмо Департамента государственной политики и нормативно-правового регулирования в сфере образования Минобрнауки России от 29.05.2007 № 03-1180), а также примерной программы учебной дисциплины «Химия», предназначенной для изучения истории в учреждениях начального и среднего профессионального образования, реализующих образовательную программу среднего (полного) общего образования при подготовке квалифицированных рабочих и специалистов среднего звена, одобренной ФГУ «Федеральный институт развития образования» 10.04.2008г. и утвержденной Департаментом государственной политики и нормативно-правового регулирования в сфере образования Минобрнауки России 16.04.2008г.
Содержание
1.Паспорт рабочей программы учебной дисциплины 3
2.Структура и примерное содержание учебной дисциплины 4
3.Условия реализации рабочей программы учебной дисциплины 14
4.Контроль и оценка результатов освоения учебной дисциплины 16
1. Паспорт рабочей программы учебной дисциплины
Химия.
1.1. Область применения рабочей программы:
Рабочая программа учебной дисциплины является частью программы подготовки квалифицированных рабочих, служащих технического профиля. Обучающиеся по данному профилю изучают химию в объёме 78 часов.
Рабочая программа ориентирована на достижение следующих целей:
- усвоение знаний о химической составляющей естественнонаучной картины мира, важнейших химических понятиях, законных и теориях;
- овладение умениями применять полученные знания для объяснения разнообразных химических явлений и свойств веществ, оценки роли химии в развитии современных технологий и получении новых материалов;
- развитие познавательных интересов и интеллектуальных способностей в процессе самостоятельного приобретения химических знаний с использованием различных источников информации, в том числе интерактивных;
- воспитание убеждённости в позитивной роли химии в жизни современного общества, необходимости химически грамотного отношения к собственному здоровью и окружающей среде;
- применение полученных знаний и умений для безопасности использования веществ и материалов в быту, на производстве и в сельском хозяйстве, для решения практических задач в повседневной жизни, для предупреждения явлений, наносящих вред здоровью человека и окружающей среде.
В профильную составляющую программы включено профессионально направленное содержание, необходимое для усвоения профессиональной образовательной программы, формирования у обучающихся профессиональных компетенций.
Отбор содержания проводился на основе следующих ведущих идей:
- материальное единство веществ природы и их генетическая связь;
- причинно-следственные связи между составом, строением, свойствами и применением веществ;
- познаваемость мира и закономерностей химических процессов;
- объясняющая и прогнозирующая роль теоретических знаний для фактологического материала;
- конкретное химическое соединение представляет собой звено в непрерывной цепи превращений веществ, оно участвует в круговороте химических веществ и в химической эволюции;
- законы природы объективны и познаваемы, знание законов химии даёт возможность управлять превращениями веществ, находить экологически безопасные способы производства веществ и материалов и охраны окружающей среды от химического загрязнения;
4
- наука и практика взаимосвязаны: требования практики – движущая сила развития науки, успехи практики обусловлены достижениями науки;
- развитие химической науки и химизация народного хозяйства служат интересам человека и общества в целом, имеют гуманистический характер и призваны способствовать решению глобальных проблем человечества.
Реализация дедуктивного подхода к изучению химии способствует развитию таких логических операций мышления, как анализ и синтез, обобщение и конкретизация, сравнение и аналогия, систематизация и классификация и др.
Специфика изучения химии при овладении профессиями и специальностями технического профиля отражена в каждой теме «примерное содержание учебной дисциплины» в рубрике «Профильные и профессионально значимые элементы содержания». Этот компонент реализуется при индивидуальной самостоятельной работе обучающихся (написание рефератов, подготовка сообщений, защита проектов), в процессе учебной деятельности под руководством преподавателя (выполнение химического эксперимента – лабораторных опытов и практических работ, решение практико-ориентированных расчётных задач и т.д.).
В программе теоретические сведения дополняются демонстрациями, лабораторными опытами и практическими работами.
При изучении химии значительное место отводится химическому эксперименту. Он открывает возможность формировать у обучающихся специальные предметные умения работать с веществами, выполнять простые химические опыты, учит безопасному и экологически грамотному обращению с веществами, материалами и процессами в быту и на производстве.
В процессе изучения химии важно формировать информационную компетентность обучающихся. Поэтому при организации самостоятельной работы необходимо акцентировать внимание обучающихся на поиске информации в средствах масс-медиа, интернете, в учебной и специальной литературе с соответствующим оформлением и представлением результатов.
Программа может использоваться другими образовательными учреждениями профессионального и дополнительного образования, реализующими образовательную программу среднего (полного) общего образования.
1.2. Место учебной дисциплины в структуре основной профессиональной образовательной программы: дисциплина входит в общеобразовательный цикл.
1.3.Цели и задачи учебной дисциплины- требования к результатам освоения учебной дисциплины:
В результате освоения учебной дисциплины обучающийся должен уметь:
Называть: изученные вещества по тривиальной или международной номенклатуре;
Определять: валентность и степень окисления химических элементов, тип химических реакций, тип химической связи в соединениях, заря иона, характер среды в водных растворах неорганических и органических соединений, принадлежность веществ к разным классам неорганических и органических соединений:
5
Характеризовать: элементы малых периодов по положению их в Периодической системе Д.И. Менделеева; общие химические свойства металлов, неметаллов, основных классов неорганических и органических соединений; строение и химические свойства изученных неорганических и органических соединений.
Объяснять: зависимость свойств веществ от их состава и строения, природу химической связи (ионной ковалентной, металлической и водородной), зависимость скорости химической реакции и положении химического равновесия от различных факторов;
Выполнять химический эксперимент по распознаванию важнейших неорганических и органических соединений;
Проводить: самостоятельный поиск химической информации с использованием различных источников (научно-популярных изданий, компьютерных баз данных, ресурсов интернета), использовать компьютерные технологии для обработки и передачи химической информации и её представления в различных формах;
Связывать изученный материал со своей профессиональной деятельности;
Использовать приобретённые знания и умения в практической деятельности и повседневной жизни: для объяснения химических явлений, происходящих в природе, быту и на производстве; определения возможности протекания химических прекращений в различных условиях и оценки их последствий экологически грамотного поведения в окружающей среде; оценки влияния химического загрязнения окружающей среды на организм человека и другие живые организмы; безопасного обращения с горючими и токсичными веществами и лабораторным оборудованием; приготовления растворов заданной концентрации в быту и на производстве; критической оценки достоверности химической информации, поступающий из разных источников.
В результате освоения учебной дисциплины обучающийся должен знать:
Важнейшие химические понятия: вещество, химический элемент, атом, молекула, относительная атомная и молекулярная масса, ион, аллотропия, изотопы, химическая связь, электроотрицательность, валентность, степень окисления, моль, молярная масса, молярный обьем газообразных веществ, растворы , электролит и неэлектролит, теория электролитической диссоциации, окислитель и восстановитель, тепловой эффект реакции, скорость химических реакций, катализ, химическое равновесие, углеродный скелет, функциональная группа, изомерия, гомология.
Основные законы химии: периодический закон Д.И. Менделеева, закон сохранения массы веществ, закон постоянства состава веществ.
Основные теории химии: электролитической диссоциации, химической связи, строения неорганических и органических соединений.
Важнейшие вещества и материалы: важнейшие металлы и сплавы; серная, соляная, уксусная, азотная кислоты; благородные газы водород, кислород, галогены; щелочные металлы; Основные , кислотные и амфотерные оксиды и гидроксиды, щелочи, углекислый и угарный газы, алканы , алкены , бензол, метанол, этанол, сложные эфиры, жиры, мыла, моносахариды , дисахариды, полисахариды, анилин, аминокислоты, белки, искусственные и синтетические волокна, каучуки, пластмассы.
Содержание учебной дисциплины «Химия» направлено на формирование следующих общих компетенций:
ОК 1. Понимать сущность и социальную значимость своей будущей профессии, проявлять к ней устойчивый интерес.
ОК 2. Организовывать собственную деятельность, исходя из цели и способов ее достижения, определенных руководителем.
ОК 3. Анализировать рабочую ситуацию, осуществлять текущий и итоговый контроль, оценку и коррекцию собственной деятельности, нести ответственность за результаты своей работы.
ОК 4. Осуществлять поиск информации, необходимой для эффективного выполнения профессиональных задач.
ОК 5. Использовать информационно-коммуникационные технологии в профессиональной деятельности.
ОК 6. Работать в команде, эффективно общаться с коллегами, руководством, клиентами.
1.4. Рекомендуемое количество часов на освоение рабочей программы учебной дисциплины:
Обязательной аудиторной учебной нагрузки обучающегося 78 часов
Раздел 1.” Общая и неорганическая химия “ 40 часов
Раздел 2. “Органическая химия” 38 часов
Структура и содержание учебной дисциплины.
2.1. Объём учебной дисциплины и виды учебной работы.
| Вид учебной работы. | Объём часов. |
| Максимальная учебная нагрузка (всего) | 102 |
| Обязательная аудиторная учебная нагрузка (всего) | 78 |
| В том числе: |
|
| Лабораторные работы | 12 |
| Контрольные работы | 4 |
| Практические занятия | 4 |
| Самостоятельная работа обучающегося (всего). | 24 |
| Дифференцированный зачёт | 2 |
2.2. Тематический план и содержание учебной дисциплины «Химия».
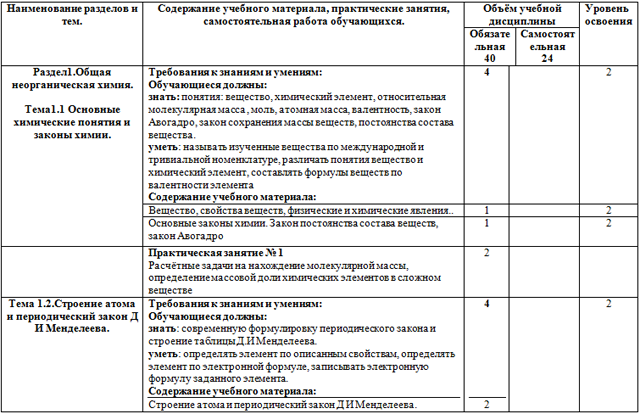
| Наименование разделов и тем. | Содержание учебного материала, практические занятия, самостоятельная работа обучающихся. | Объём учебной дисциплины | Уровень освоения |
| Обязательная 40 | Самостоятельная 24 |
| Раздел1.Общая неорганическая химия.
Тема1.1 Основные химические понятия и законы химии. | Требования к знаниям и умениям: Обучающиеся должны: знать: понятия: вещество, химический элемент, относительная молекулярная масса , моль, атомная масса, валентность, закон Авогадро, закон сохранения массы веществ, постоянства состава вещества. уметь: называть изученные вещества по международной и тривиальной номенклатуре, различать понятия вещество и химический элемент, составлять формулы веществ по валентности элемента Содержание учебного материала: | 4 |
| 2 |
| Вещество, свойства веществ, физические и химические явления.. | 1 |
| 2 |
| Основные законы химии. Закон постоянства состава веществ, закон Авогадро | 1 |
| 2 |
|
| Практическая занятие № 1 Расчётные задачи на нахождение молекулярной массы, определение массовой доли химических элементов в сложном веществе | 2 |
|
|
| Тема 1.2.Строение атома и периодический закон Д И Менделеева. | Требования к знаниям и умениям: Обучающиеся должны: знать: современную формулировку периодического закона и строение таблицы Д.И Менделеева. уметь: определять элемент по описанным свойствам, определять элемент по электронной формуле, записывать электронную формулу заданного элемента. Содержание учебного материала: Строение атома и периодический закон Д И Менделеева. | 4
2 |
| 2 |
| Лабораторная работа №1 Моделирование ПСХЭ | 1 |
|
|
| Контрольная работа № 1 По теме ПСХЭ | 1 |
|
|
| Тема1 .3.Строение вещества. | Требования к знаниям и умениям: Обучающиеся должны: знать: виды химической связи, механизм образования химических связей, типы кристаллических решеток. уметь: определять характер химической связи в различных соединениях и степень окисления элемента. Содержание учебного материала: | 4 |
| 2 |
| Виды химической связи. Кристаллические решетки | 2 |
| 2 |
| Чистые вещества и смеси. Дисперсные системы | 2 |
| 2 |
| Внеаудиторная самостоятельная работа. Составление структурных формул молекулярных соединений. Подготовка сообщений и рефератов |
| 4 |
|
| Тема1 .4. Вода. Растворы. Электролитическая диссоциация. | Требования к знаниям и умениям: Обучающиеся должны: знать: теорию электролитической диссоциации; электролиты и неэлектролиты. уметь: записывать уравнения реакций ионного обмена, решать задачи на нахождение массовой доли растворенного вещества. Содержание учебного материала: | 4 |
| 2 |
| Вода как растворитель. Растворы. Растворимость веществ, массовая доля вещества в растворе. | 1 |
| 2 |
| Электролитическая диссоциация Электролит и неэлектролит, механизм диссоциации, слабые и сильные электролиты. | 1 |
| 2 |
| Практическая занятие №2 Решение задач на массовую долю растворённого вещества | 1 |
|
|
| Лабораторная работа № 2 Приготовление растворов заданной концентрации. | 1 |
|
|
| Тема.1.5. Классы неорганических соединений и их свойства. | Требования к знаниям и умениям: Обучающиеся должны: знать: Основные классы неорганических соединений, их классификацию, химические свойства, способы получения, гидролиз солей. уметь: Составлять уравнения реакций, характеризующие химические свойства веществ, составлять уравнения реакций гидролиза солей. Содержание учебного материала: | 6 |
| 2 |
| Оксиды. Классификацию оксидов: основные, кислотные, амфотерные. Основания. Химические свойства оснований в свете теории электролитической диссоциации | 2 |
| 2 |
| Кислоты как электролиты, свойства кислот, основные способы получения кислот. | 2 |
| 2 |
| Соли кислые, основные, средние. Способы получения солей. | 1 |
| 2 |
| Лабораторная работа№3 Испытание растворов кислот и оснований. | 1 |
|
|
| Внеаудиторная Самостоятельная работа Составление уравнений гидролиза солей. Подготовка рефератов по теме: « Применение кислот и оснований как электролитов в аккумуляторах». |
| 4 |
|
| Тема 1.6. Закономерности протекания химических реакций. | Требования к знаниям и умениям: Обучающиеся должны: знать: основные факторы, влияющие на скорость химической реакции, на смещение химического равновесия, основные понятия и сущность окислительно-восстановительных реакций уметь: применять понятия: прямая и обратная реакции, эндо - и экзотермические реакции выявлять условия протекания обратной реакции в нужном направлении, скорость химической реакции, химическое равновесие и условие его смещения. Содержание учебного материала: | 7 |
| 2 |
| Классификация химических реакций. Реакции соединения, разложения, обмена, замещения, обратимые, необратимые, экзотермические, эндотермические, окислительно-восстановительные. Термохимические уравнения. | 2 |
| 2 |
| Скорость химических реакций. Химическое равновесие. Факторы влияющие на скорость химических реакций | 2 |
| 2 |
| Практическая занятие №3 Составление уравнений ОВР методом электронного баланса. Определение окислителей и восстановителей. | 2 |
|
|
| Лабораторная работа № 4 Определение факторов, влияющих на скорость химической реакции | 1 |
|
|
| Тема 1.7. Металлы и неметаллы. | Требования к знаниям и умениям: Обучающиеся должны: знать: положение металлов в периодической системе, особенности строения их атомов, понятие о коррозии и способы защиты металлов от коррозии. Положение неметаллов в периодической системе, особенности строения неметаллов , свойства, получение и применение уметь: определять свойства металлов в зависимости от его положения в электрохимическом ряду напряжения металлов, характеризовать общие свойства неметаллов, распознавать хлорид-, карбонат -анионы; выполнять химические опыты, подтверждающие свойства неметаллов, металлов и их соединений Содержание учебного материала: . | 11 |
| 2 |
| Металлы. Особенности строения атомов металлов. Физические и химические свойства металлов электрохимический ряд напряжения металлов. | 2 |
| 2 |
| Металлы в современной технике. Способы получения металлов. Сплавы. Понятия металлургия, пирометаллургия, электрометаллургия, черные и цветные сплавы. | 2 |
| 2 |
| Коррозия металлов | 2 |
| 2 |
| Лабораторная работа №5 Структура белого и серого чугуна | 1 |
|
|
| Неметаллы. Особенности строения неметаллов | 2 |
| 2 |
| Лабораторная работа №6 Получение, собирание и распознавание газов | 1 |
|
|
| Итоговая контрольная работа № 2 Общая и неорганическая химия | 1 |
|
|
| Внеаудиторная самостоятельная работа Подготовка рефератов по теме « Сплавы металлов», « Железо и его соединения», « Применение металлов и сплавов в технике». |
| 4 | 2 |
| Раздел 2 Органическая химия. |
| 38 | 12 |
|
| Тема. 2.1.Основные понятия органической химии и теория строения органических соединений А.М. Бутлерова. Изомерия. | Требования к знаниям и умениям: Обучающиеся должны: знать: основные положения теории химического строения А.М. Бутлерова; явления изомерии. уметь: объяснять причину многообразия органических соединений. Содержание учебного материала: | 2 |
| 2 |
| Внеаудиторная самостоятельная работа. Подготовить рефераты на тему «Жизнь и научная деятельность А. М. Бутлерова», « Многообразие органических соединений». |
| 2 |
|
| Тема 2.2. Углеводороды и их природные источники. . | Требования к знаниям и умениям: Обучающиеся должны: знать: общую формулу алканов, алкенов, алкинов, диеновых и ароматических углеводородов ,характер связи в их молекулах; понятие гомологов, правила рациональной и систематической номенклатуры уметь: называть алканы, алкены, алкины, диеновые и ароматические углеводороды по рациональной и систематической номенклатуре; составлять молекулярные и структурные формулы углеводородов и их галогенопроизводных; составлять уравнения химических реакций, подтверждающих их свойства Содержание учебного материала: | 12 |
|
|
| Предельные углеводороды. Химические и физические свойства предельных углеводородов. Получение и применение предельных углеводородов. Гомологи. Изомеры. Лабораторная работа №7 Изготовление моделей органических веществ | 3 |
| 2 |
| Непредельные углеводороды. Этилен. Химические и физические свойства. Получение и применение. Гомологи. Изомеры. | 2 |
| 2 |
| Лабораторная работа №8 Качественная реакция на непредельные углеводороды | 1 |
|
|
| Диеновые углеводороды. Природный и синтетический каучуки их свойства получение и применение, резина её свойства и применение. | 2 |
| 2 |
| Алкины и ароматические углеводороды Химические и физические свойства. Получение и применение. Гомологи. Изомеры.. | 2 |
| 2 |
| Внеаудиторная самостоятельная работа Решение задач на нахождение молекулярной формулы углеводородов. Составление структурных формул изомеров. |
| 2 |
|
| Природный газ. Нефть. Состав природного газа и нефти, способы переработки нефти, продукты переработки и их применение. | 1 |
| 2 |
| Контрольная работа № 3 По теме Углеводороды | 1 |
|
|
| Внеаудиторная самостоятельная работа. Подготовка рефератов и творческих работ по темам: Охрана окружающей среды при нефтепереработке. Использование нефтепродуктов. Нефть и политика. Историческое развитие общества и изменение потребления нефти. |
| 2 |
|
| Тема 2.3. Кислородосодержащие органические соединения. | Требования к знаниям и умениям: Обучающиеся должны: знать: определение, строение, общие формулы, функциональную группу, гомологов , изомеров, получение и применение спиртов, фенолов, альдегидов, карбоновых кислот, углеводов, жиров, сложных и простых эфиров. Меры по охране окружающей среды от промышленных отходов, содержащих фенол; о губительном воздействии спиртов на организм человека. уметь: составлять структурные формулы и изомеров спиртов, фенолов, альдегидов, карбоновых кислот, углеводов, жиров, простых и сложных эфиров. Называть их по систематической и тривиальной номенклатуре. Содержание учебного материала: | 12 |
| 2 |
| Спирты. Фенолы. Многоатомные спирты. Физические и химические свойства. Получение и применение. | 2 |
| 2 |
| Лабораторная работа №9 Свойства глицерина | 1 |
|
|
| Альдегиды. Физические и химические свойства. Получение и применение | 2 |
| 2 |
| Карбоновые кислоты. . Физические и химические свойства. Получение и применение | 2 |
| 2 |
| Сложные эфиры. Жиры. Физические и химические свойства. Получение и применение | 2 |
| 2 |
| Лабораторная работа № 10 Доказательство непредельного характера жидкого жира | 1 |
|
|
| Углеводы. Моносахариды, дисахариды, полисахариды. . Физические и химические свойства. Получение и применение. Понятие о реакциях поликонденсации и гидролиза. | 1 |
| 2 |
| Лабораторная работа №11. Взаимодействие глюкозы и сахарозы с гидроксидом меди(II) | 1 |
|
|
| Самостоятельная работа обучающихся Подготовка сообщений по темам: « Действие метанола и этанола на живые организмы», « Негативное влияние спиртов на организм человека», « Применение формальдегида», « Промышленное получение формальдегида и ацетальдегида.» Ознакомиться с составом , свойствами. Правилами использования антифризов, применяемых в автомашинах. |
| 4 |
|
| Тема 2.4.Азот содержащие органические соединения. Полимеры. | Требования к знаниям и умениям: Обучающиеся должны: знать: строение, функциональные группы ,названия , химические и физические свойства аминов, аминокислот. Структуру белков, свойства и значение, биологическую роль и превращение белков в организме. Определение полимеров, состав, строение и свойства уметь: определять наличие белковых соединений качественными реакциями; составлять уравнения реакций. Содержание учебного материала: | 10 |
| 2 |
| Амины. Аминокислоты. Химические и физические свойства аминов, аминокислот Получение и применение. | 4 |
| 2 |
| Белки. Структура, свойства и значение | 2 |
| 2 |
| Полимеры. Волокна. Реакции полимеризации и поликонденсации. Представители пластмасс, синтетических и натуральных волокон. | 2 |
| 2 |
| Лабораторная работа№12. Денатурация белка солями тяжёлых металлов, спиртом. | 1 |
|
|
| Итоговая контрольная работа.№ 4 Общая и органическая химия. | 1 |
|
|
| Внеаудиторная самостоятельная работа Подготовить сообщения по теме« Промышленное получение формальдегида и ацетальдегида». «Применение формальдегида». Решение задач на вычисление массы исходного вещества, если известен практический выход продукта реакции. |
| 2 |
|
| Дифференцированный зачёт |
| 2 |
|
|
| Итого | 78 | 24 |
|
3. Условия реализации учебной дисциплины.
3.1. Требования к минимальному материально-техническому обеспечению
Реализация программы дисциплины требует наличия учебного кабинета и лаборатории химии.
Оборудование учебного кабинета и лаборатории:
- посадочные места по количеству обучающихся,
- рабочее место преподавателя,
- демонстрационный стол,
- вытяжной шкаф,
- учебно-наглядные пособия по химии,
- лабораторное оборудование (периодическая система химических элементов Д. И. Менделеева, ряд напряжений металлов, ряж электроотрицательности неметаллов, таблица растворимости солей, кислот и оснований в воде, плакаты по общей, неорганической и органической химии, химическая посуда, химические реактивы, лабораторные весы и разновесы, коллекции «Металлы», «Горные породы», «Пластмассы и волокна», модели органических веществ).
3.2. Информационное обеспечение обучения.
Перечень рекомендуемых учебных изданий, интернет-ресурсов. дополнительной литературы.
Основные источники:
Габриелян О.С. Химия в тестах, задачах, упражнениях: учеб. Пособие для студ. сред. проф. учеб. заведений/ О.С.Габриелян, Г.Г. Лысова. – М., 2009. 213с
Габриелян О.С. Практикум по общей, неорганической и органической химии: учеб. пособие для студ. сред. проф. учеб. заведений/Габриелян О.С., Остроумов И.Г., Дорофеева Н.М. – М., 2008. 234с
Габриелян О.С. Химия 10 класс. Базовый уровень: учеб. для общеобразоват. учреждений. – М., 2008.346с
Габриелян О.С. Химия 11 класс. Базовый уровень: учеб. для общеобразоват. учреждений. – М., 2009. 368с
Ерохин Ю.М. Химия. – М., 2008. 267с
Дополнительные источники:
1. Габриелян О.С. Химия для преподавателя: учебно-методическое пособие/ О.С. Габриелян, Г.Г. Лысова. – М., 2013.386с
2. Габриелян О.С. Настольная книга учителя химии: 11 класс: в 2 ч./ О.С. Габриелян, Г.Г. Лысова, А.Г. Введенская. – М., 2004. 368с
3. Ерохин Ю.М., Фролов В.И. Сборник задач и упражнений по химии (с дидактическим материалом): учеб. пособие для студентов сред. проф. завед. – М., 2004.245с
4. Кузнецова Н.Е. Обучение химии на основе межпредметной интеграции/ Н.Е. Кузнецова, М.А. Шаталов. – М., 2004. 346с
5. Пичугина Г.В. Химия и повседневная жизнь человека. – М., 2009.245с
6. Титова И.М. Химия и искусство. – М., 2007.167с
7. Химия в школе: научно-методический журнал учреждён Министерством образования и науки РФ.
8. 1 сентября Химия: приложение к газете «1 сентября». Учреждён Министерством образования и науки Российской Федерации.
9. Свет: научно-теоретический журнал учреждён Министерством сельского хозяйства Российской Федерации.
10. Электронное учебное пособие «Демонстрационное планирование «Общая химия» ООО «РМТ компании» г. Волгоград.
11. Электронное учебное пособие «Органическая химия + все опыты органики» ООО «Руссобит Паблишинг» г. Сергиев Посад.
12. Мультимедийный репетитор «Химия» ООО «Мультимедиа технологии и дистанционное обучение» 2010 г. Санкт-Петербург.
13. Интернет-ресурс. Механизмы органических реакций. Форма доступа http://www.tI.ru/gimnI3/docs/ximia/him
14. Интернет-ресурс. Химия для всех. Электронный справочник за полный курс химии. Форма доступа http://www.informatika.ru/text/database/cheiny/START.html
15. http://academia-moscow.ru/ ЭБ: Образовательно- издательский центр «Академия»
16. http://znanium.com/ ЭБ: Издательство НИЦ «Инфа- М»
4. Контроль и оценка результатов освоения дисциплины.
Контроль и оценка результатов освоения дисциплины осуществляется преподавателем в процессе проведения практических занятий и лабораторных работ, тестирования, а также выполнения обучающимися индивидуальных заданий, проектов, исследований.
| Результаты (освоенные умения, усвоенные знания) | Формы и методы контроля и оценки результатов обучения |
| Знания: |
|
важнейшие химические понятия: вещество, химический элемент, атом, молекула, относительные атомная и молекулярная массы, ион, аллотропия, изотопы, химическая связь, электроотрицательность, валентность, степень окисления, моль, молярная масса, молярный объем газообразных веществ, вещества молекулярного и немолекулярного строения, растворы, электролит и неэлектролит, электролитическая диссоциация, окислитель и восстановитель, окисление и восстановление, тепловой эффект реакции, скорость химической реакции, катализ, химическое равновесие, углеродный скелет, функциональная группа, изомерия, гомология;
| тестирование, экспертная оценка хода и результата выполнения практического занятия№1, №2, №3, лабораторной работы№1, №2, №3, №4 контрольная работа№1 |
|
| тестирование, устный опрос |
|
| экспертная оценка хода и результата выполнения лабораторной работы№2, практического занятия№2 |
важнейшие вещества и материалы: важнейшие металлы и сплавы; серная, соляная, азотная и уксусная кислоты; благородные газы, водород, кислород, галогены, щелочные металлы; основные, кислотные и амфотерные оксиды и гидроксиды, щелочи, углекислый и угарный газы, сернистый газ, аммиак, вода, природный газ, метан, этан, этилен, ацетилен, хлорид натрия, карбонат и гидрокарбонат натрия, карбонат и фосфат кальция, бензол, метанол и этанол, сложные эфиры, жиры, мыла, моносахариды (глюкоза), дисахариды (сахароза), полисахариды (крахмал и целлюлоза), анилин, аминокислоты, белки, искусственные и синтетические волокна, каучуки, пластмассы;
| экспертная оценка хода и результата выполнения лабораторных работ№3,№5,№6 ,№7, №8,№9, №10, №11, №12 практической работы№4 устный опрос тестирование |
| Умения: |
|
| Составлять структурные формулы и формулы изомеров органических соединений называть их по систематической номенклатуре. | тестирование, устный опрос |
| Определять валентность и степень окисления химических элементов, тип химической связи в соединениях, заряд иона, характер среды в водных растворах неорганических и органических соединений, окислитель и восстановитель, принадлежность веществ к разным классам неорганических и органических соединений. | экспертная оценка хода и результата выполнения лабораторных работ№1,№2,№3 практических занятий№2, №3, тестирование, устный опрос |
| Характеризовать элементы малых периодов по их положению в периодической системе Д.И. Менделеева, общие химические свойства металлов, неметаллов, основных классов неорганических и органических соединений, строение и химические свойства изученных неорганических и органических соединений | тестирование, устный опрос, экспертная оценка хода и результата выполнения лабораторных работ№1-№12 |
| Объяснять зависимость свойств веществ от их состава и строения, природу химической связи (ионной ковалентной, металлической и водородной), зависимость скорости химической реакции и положение химического равновесия от различных факторов | тестирование, устный опрос |
| Выполнять химический эксперимент по распознаванию важнейших неорганических и органических соединений | экспертная оценка хода и результата выполнения лабораторных работ№1-№12 |
| Проводить самостоятельный поиск химической информации с использованием различных источников (научно-популярных изданий, компьютерных баз данных, ресурсов интернета), использовать компьютерные технологии для обработки и передачи химической информации и её представления в различных формах | индивидуальные творческие задания |
| Связывать изученный материал со своей профессиональной деятельностью | индивидуальные творческие задания |
| Решать расчётные задачи по химическим формулам и уравнениям | экспертная оценка хода и результата выполнения практических работ№1-№4 тестирование, устный опрос |
| Использовать приобретённые знания и умения в практической деятельности и повседневной жизни | индивидуальные творческие задания |

 Получите свидетельство
Получите свидетельство Вход
Вход











 Рабочая программа по химии для студентов СПО (0.22 MB)
Рабочая программа по химии для студентов СПО (0.22 MB)
 0
0 1248
1248 177
177 Нравится
0
Нравится
0



