
1курс
Составитель
преподаватель
физики ГПОУ ТО «НТК»Бондарчук Т.В.


Подготовка к восприятию нового
материала
Фронтальный опрос
1. Дать определение внутренней энергии.
2. Способы изменения внутренней энергии.
3. Как определить работу,совершенную газом при его расширении ?
4. Как с помощью графика в координатах ( p,V ) определить работу по изменению состояния газа ?
5 .Что называют количеством теплоты ?

План урока
- Содержание 1-ого закона термодинамики
- Применение 1-ого закона термодинамики к изопроцессам в газах
- Адиабатический процесс
- Необратимость процессов в природе
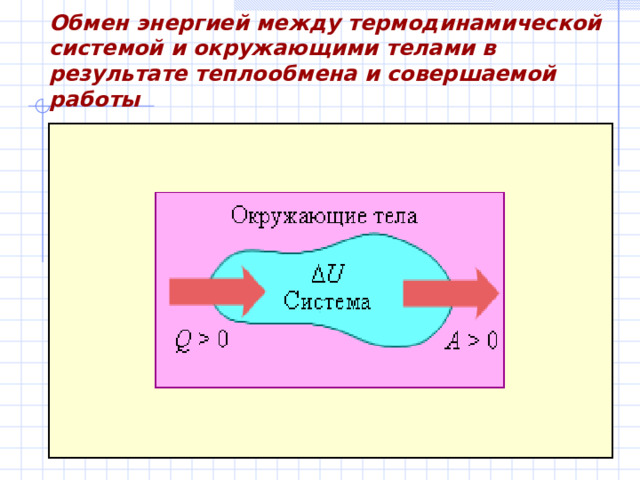
Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой
работы

Первый закон термодинамики
Изменение Δ U внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы A внешних сил и количества теплоты Q, переданного системе
ΔU = Q + A

Вторая запись первого закона термодинамики
Q = ΔU + A’
Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.
Виды изопроцессов
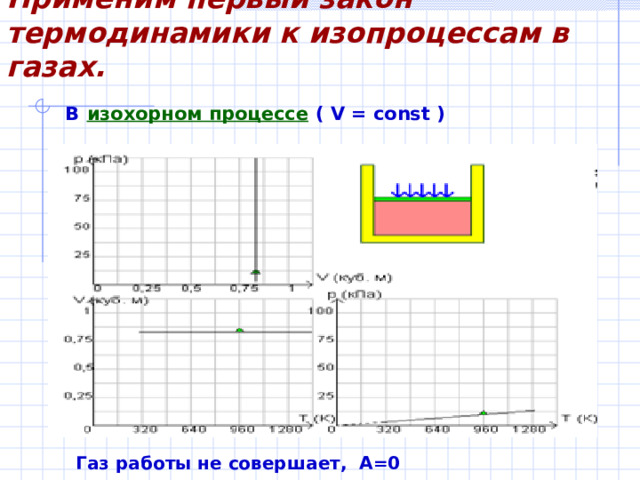
Применим первый закон термодинамики к изопроцессам в газах.
В изохорном процессе ( V = const )
Газ работы не совершает, А=0
 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q " width="640"
0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q " width="640"
Первый закон термодинамики для изохорного процесса
Q = Δ U = U (T 2 ) – U (T 1 )
Здесь U (T1) и U (T2) – внутренние энергии газа в
начальном и конечном состояниях.
- При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q
- При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q
- При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q
- При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q
- При изохорном нагревании тепло поглощается газом (Q 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q
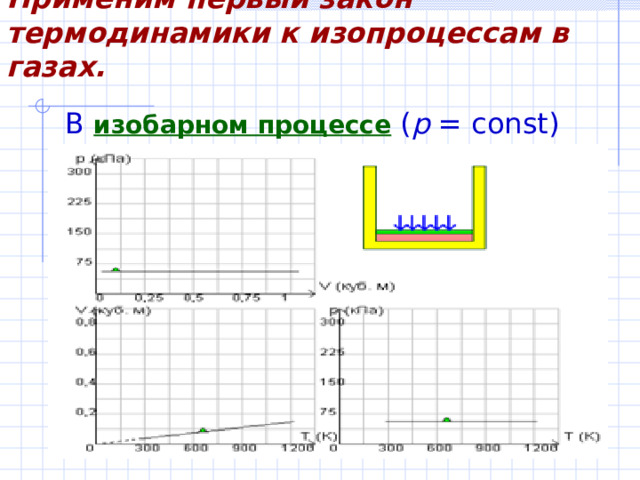
Применим первый закон термодинамики к изопроцессам в газах.
В изобарном процессе ( p = const)

Работа, совершаемая газом, выражается соотношением
p- давление
V1,V2- объем в начальном и конечном состояниях соответственно
A = p (V 2 – V 1 ) = p ΔV
 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U " width="640"
0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U " width="640"
Применим первый закон термодинамики к изопроцессам в газах.
Первый закон термодинамики для изобарного процесса :
Q = U (T 2 ) – U (T 1 ) + p (V 2 – V 1 ) = ΔU + p ΔV
- При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу.
- При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу.
- При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу.
- При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу.
- При изобарном расширении Q 0 – тепло поглощается газом, и газ совершает положительную работу.
При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U
- При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U
- При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U
- При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U
- При изобарном сжатии Q A T 2 T 1 ; внутренняя энергия убывает, Δ U
Применим первый закон термодинамики к изопроцессам в газах.
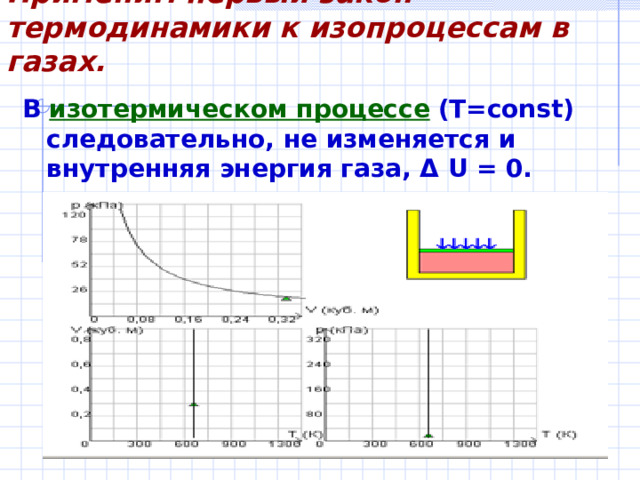
В изотермическом процессе ( T=const) следовательно, не изменяется и внутренняя энергия газа, Δ U = 0.
Количество теплоты Q , полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам.

Первый закон термодинамики для изотермического процесса выражается соотношением
Q = A
Количество теплоты Q, полученной газом в процессе изотермического расширения,
превращается в работу над внешними телами.
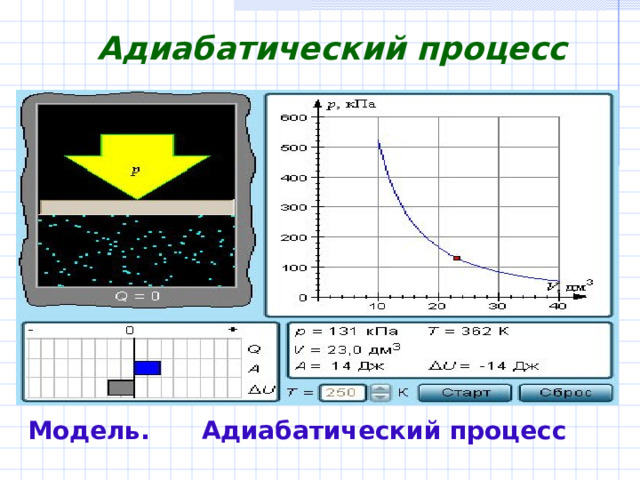
Адиабатический процесс
Модель. Адиабатический процесс

В адиабатическом процессе Q = 0; поэтому первый закон термодинамики принимает вид
A = –ΔU
. газ совершает работу за счет убыли его внутренней энергии.
 0); поэтому его внутренняя энергия уменьшается (Δ U (A 0) (Δ U " width="640"
0); поэтому его внутренняя энергия уменьшается (Δ U (A 0) (Δ U " width="640"
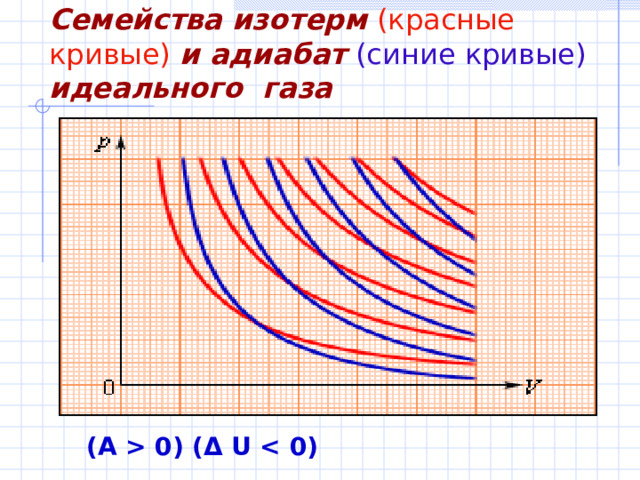
Семейства изотерм (красные кривые) и адиабат (синие кривые) идеального газа
На плоскости ( p , V ) процесс адиабатического расширения (или сжатия) газа изображается кривой, которая называется адиабатой . При адиабатическом расширении газ совершает положительную работу ( A 0); поэтому его внутренняя энергия уменьшается (Δ U
(A 0) (Δ U

В координатах (p, V) уравнение адиабатного процесса имеет вид
pV γ = const
Это соотношение называют уравнением Пуассона . Здесь γ = Cp / CV – показатель адиабаты, Cp и CV – теплоемкости газа в процессах с постоянным давлением и с постоянным объемом.

Работа газа в адиабатическом процессе просто выражается через температуры T 1 и T 2 начального и конечного состояний
A = C V (T 2 – T 1 )

Расширение газа в пустоту
. В этом процессе Q = 0, т.к. нет теплообмена с окружающими телами, и A = 0, т.к. оболочка недеформируема.
Из первого закона термодинамики следует: Δ U = 0, т. е.
внутренняя энергия газа осталась неизменной.

Закрепление знаний,умений,навыков .
Ответьте на вопросы:
1)
а ) п ри быстром сжатии газа температура его повысилась.Можно ли сказать,что
- газу сообщено некоторое количество теплоты ?
- в нутренняя энергия газа увеличилась ?
б) м ожно ли передать газу некоторое количество теплоты,не вызывая при этом повышения его температуры ?
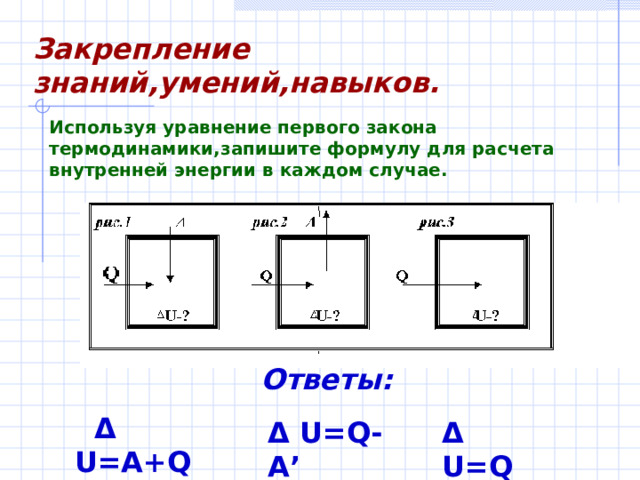
Закрепление знаний,умений,навыков.
Используя уравнение первого закона термодинамики,запишите формулу для расчета внутренней энергии в каждом случае.
Ответы:
Δ U=A+Q
Δ U=Q
Δ U=Q-A’

Закрепление знаний,умений,навыков.
Выберите правильный вариант ответа.
Ответы.
Изобарный- изменяются
параметры V,T
Изохорный - A=0
Изотермический-изменяются
параметры p,V
Адиабатный - Q=0

Домашнее задание
Параграф 26-28
повторить КПД теплового двигателя (“Физика 8”); превращение энергии и использование машин (“Физика 9”).

Использован
учебник
электронный

 Получите свидетельство
Получите свидетельство Вход
Вход











 Презентация к уроку "Первый закон термодинамики" (958 KB)
Презентация к уроку "Первый закон термодинамики" (958 KB)
 0
0 891
891 82
82 Нравится
0
Нравится
0


