
ПСХЭ Д.И.Менделеева.
11 класс урок 3.

Дмитрий Иванович Менделеев ( 1834-1907 )
Выдающийся русский химик, открывший периодический закон и создавший периодическую систему химических элементов.
.
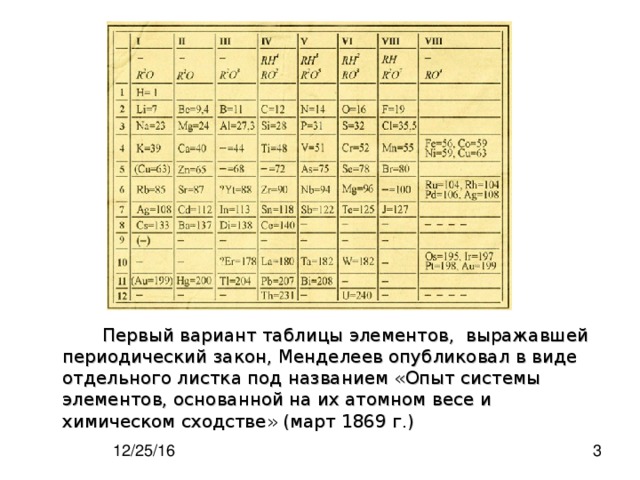
Первый вариант таблицы элементов, выражавшей периодический закон, Менделеев опубликовал в виде отдельного листка под названием «Опыт системы элементов, основанной на их атомном весе и химическом сходстве» (март 1869 г.)

Современная периодическая таблица Д.И.Менделеева
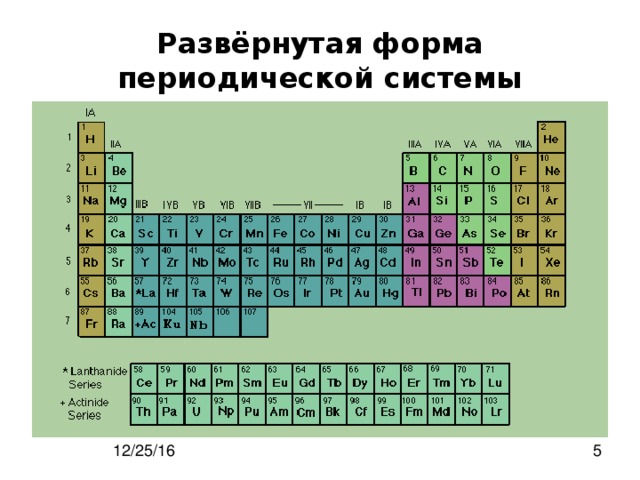
Развёрнутая форма периодической системы

Структура периодической системы:
Формулировка периодического закона
Понятие периода
«Свойства простых тел находятся в периодической зависимости от заряда атомного ядра».
А) Период – это расположение элементов по горизонтали..
Б) Период начинается с щелочного металла и заканчивается инертном газом.
В) В периодической системе всего 7 периодов, 1,2,3 малые и 4,5,6,7 большие
Г) Период показывает количество энергетических уровней.
Д) Количество элементов на периодах: 1-2, 2-8, 3-8, 4-18, 5-18, 6-32, 7-28.
В) В настоящее время в периодической системе находится 116 элементов.
Принцип построения периодической системы
«Периодическая система построена в порядке возрастания атомной массы».
Принцип периодичности
«Периодичность - это повторение химических свойств через каждые семь элементов на восьмой»

Структура периодической системы:
Понятие группы
А) Группа – это расположение элементов по вертикале.
Б) В периодической системе всего 8 групп, каждая группа подразделяется на:
главную, в которой происходит заполнение электронов на внешнем энергетическом уровне и побочную в которой происходит заполнение предвнешнего энергетического уровня.
В) Группа показывает количество электронов на внешнем энергетическом уровне только в главных подгруппах.
Г) Группа показывает наивысшую валентность по кислороду.
Понятие порядкового номера
Порядковый номер показывает:
А) Заряд ядра атома.
Б) Количество электронов, которые движутся вокруг атома и несут отрицательный заряд.
В) Количество протонов.
Г) Количество нейтронов, которые вычисляются между разностью молярной масс и порядковым номером.

Задание: заполни пропуски
В периодах:
1) Металлические свойства _ _ _ _ _ _ _ _ _ _
2) Неметаллические свойства _ _ _ _ _ _ _ _ _ _ _
3) Степень окисления в высших оксидах и гидроксидах _ _ _ _ _ _ _ _ _ _ _ _ _ от _ _ до _ _
4) Высшие оксиды от_ _ _ _ _ _ _ _ через _ _ _ _ _ _ _ _ _ _ сменяются _ _ _ _ _ _ _ _ _ _
5) Высшие гидроксиды от_ _ _ _ _ _ _ _ _ через _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ сменяются _ _ _ _ _ _ _ _ _

Задание: впиши пропущенные слова
В пределах одного периода с увеличением порядкового номера элемента металлические свойства _ _ _ _ _ _ _ _ _ _ , а неметаллические _ _ _ _ _ _ _ _ _ _, так как:
- Заряды атомных ядер _ _ _ _ _ _ _ _ _ _ _ _ _
- Число электронов на внешнем электронном слое _ _ _ _ _ _ _ _ _ _ _ _ _
- Число электронных слоев _ _ _ _ _ _ _ _ _ _ _ _
(оно равно номеру _ _ _ _ _ _ _ )
- Радиус атома _ _ _ _ _ _ _ _ _ _ _

Задание: впиши пропущенные слова
В пределах одной группы (главной подгруппы) с увеличением порядкового номера элемента металлические свойства _ _ _ _ _ _ _ _ _ _ _ , а неметаллические _ _ _ _ _ _ _ _ _ _, так как:
- Заряды атомных ядер _ _ _ _ _ _ _ _ _ _ _ _ _
- Число электронов на внешнем электронном слое _ _ _ _ _ _ _ _ _ _ _ _
(оно равно номеру _ _ _ _ _ _)
- Число электронных слоев _ _ _ _ _ _ _ _ _ _ _ _ _
- Радиус атома _ _ _ _ _ _ _ _ _ _ _ _ _

План характеристики химического элемента:
1. Положение в ПСХЭ:
- Порядковый номер
- Номер периода
-Номер группы
-Главная или побочная подгруппа
2. Строение атома:
- Число электронов, протонов, нейтронов
Распределение электронов по уровням
-Электронная формула
3. Прогноз свойств:
- Металл или неметалл
-Предполагаемые формулы и свойства соединений

Задание. Дай характеристику элементу № 20, 3 5

Задание: подчеркните символы химических элементов-металлов и расположите их в порядке ослабления металлических свойств:
А) Cl; Al; S; Na; P; Mg; Si
Б) Sn; As; N; Ge; C; Pb

Задание: подчеркните символы химических элементов-неметаллов и расположите их в порядке усиления неметаллических свойств:
А) Li; F; N; Be; O; B; C
Б) Bi; As; N; Sb; P

Задание.
Расположи химические элементы в порядке возрастания
- неметаллических свойств:
а) P; S; Si.
б) P; Cl; Mg.
в) Ga; B; In.
- металлических свойств:
а) Ga; Al; In.
б) Ga; B; Tl.
в) P; Na; Al.

Задание: Сравните атомы поставив знаки › , ‹ или = :
А) заряд ядра: Al … Si; C…N; O…S; Mg…Ca
Б) число электронных слоев: Al … Si; C…N; O…S; Mg…Ca
B) Число электронов на внешнем слое: Al … Si; C…N; O…S; Mg…Ca
Г) Радиус атома: Al … Si; C…N; O…S; Mg…Ca
Д) Металлические свойства: Al … Si; C…N; O…S; Mg…Ca
Е) Неметаллические свойства: Al … Si; C…N; O…S; Mg…Ca

Химическая викторина
- Какой элемент может быть легким, как сажа, а твердый как алмаз
(углерод)
- Название элемента похоже на планету
(уран, плутон)
- Назвать химический элемент, состоящий из двух млекопитающих
(мышьяк)
- Элементы, названные в честь стран
(франций, германий, полоний, америций)
- Самый распространенный элемент на планете
(кислород)

Химическая викторина
- Назвать благородные металлы
(золото, серебро, платина)
- Назвать металл, который обладает наивысшей электропроводностью
(серебро)
- Назвать самый твердый металл
(хром)
- Назвать самый легкий металл
(литий)
- Назвать самый тяжелый металл
(осмий)

Химическая викторина
(зеленый)
- Назвать аллотропную модификацию кислорода
(озон)
- Назвать газ, необходимый для дыхания
(кислород)
- Назвать самый сильный окислитель
(фтор)
(ртуть)


 Получите свидетельство
Получите свидетельство Вход
Вход































 Презентация к уроку химии "ПСХЭ Д.И.Менделеева" (0.85 MB)
Презентация к уроку химии "ПСХЭ Д.И.Менделеева" (0.85 MB)
 1
1 3470
3470 413
413 Нравится
0
Нравится
0





