В условиях перехода основной школы на ФГОС одной из основных задач учителя – реализация личностно ориентированного обучения, так как итогом деятельности педагога и обучающегося кроме предметных знаний и умений являются и метапредметные, и личностные результаты.
Реализация личностно ориентированного обучения через овладение учащимися естественно-научного цикла знаний в предметной области «Химия» позволяет формировать у обучающихся различные мыслительные умения, создает возможности для формирования метапредметных и личностных качеств, вносит существенный вклад в формирование системы знаний об окружающем мире (картина мира), формирование современного мировоззрения и экологической грамотности.
Являясь составной частью общего образования, учебный предмет «химия» помогает овладеть научными методами познания, исследовательской деятельностью, возможностью самостоятельного постановки проблем и нахождения способов их решения. Обощенные способы действий учащихся с учебным материалом позволяют успешно решать поставленные задачи.
Используя знания математики, накопленный жизненный опыт учащихся нами составлена схема решения первых задач по химии. Наглядность и доступность (простота) действий используется нами для решения задач по теме «Чистые вещества и смеси. Массовая доля компонентов в смеси». Этот способ мы называем «рисуем задачу».
Подготовительный этап:
в химический стакан (№1) насыпается взвешенное количество обычной поваренной соли (хлорида натрия) из магазинной упаковки (например - 30г. );
во второй химический стакан (№2), имеющий калибровку, наливается вода (например – 150 мл). Уточняем, что плотность воды равна единице, значит, для воды численное значение объема и массы совпадают;
учитель задает вопрос: есть ли в чистой воде (для научности эксперимента используем дистиллированную воду, о которой на предыдущих уроках уже были сделаны выводы как о веществе- конденсате) растворенное вещество? Нет. Следовательно, процент растворенного вещества в воде равен 0%.

учитель задает вопрос: наливали ли мы воду в стакан с солью? Нет. Следовательно, в стакане 100%-ное безводное вещество (только для данного опыта) ;
переместим содержимое стаканов № 1 и № 2 в стакан № 3. Данное действие необходимо для зрительного запоминания алгоритма решения задач.
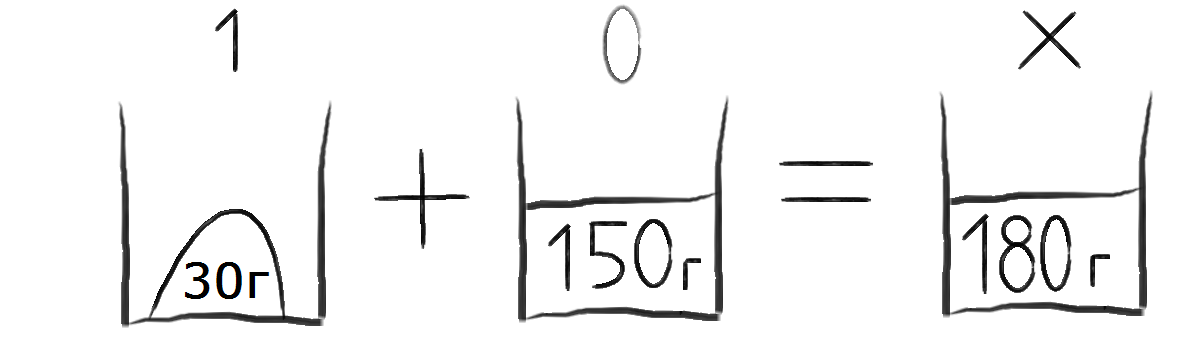
Нарисуем схему наших действий и сделаем вывод, что в результате наших действий получился раствор соли, для которого мы можем рассчитать процентное содержание соли в растворе. Для наглядности решения в «стакан» («чашку») записываем массу вещества в граммах.
Над «стаканом» пишем содержание вещества в каждом стакане (чашке), при этом процент записываем числом (100% = 1, 0% = 0). Действие соединения веществ записываем математическим знаком «+», результат действия соответственно знаком равенства «=». Таким образом, получаем картинку...
Затем записываем задачу - картинку математическим выражением - 30 x 1 + 150 x 0 = 180 x X.
Число в чашке умножаем на число над этой чашкой плюс следующее произведение чисел, знак равенства и произведение чисел в третьем стакане. При написании чисел в третьем стакане ребята сразу видят массу раствора, а неизвестную нам массовую долю растворенного вещества обозначаем Х
Осталось решить математическое выражение и найти Х.
30 x 1 + 150 x 0 = 180 x X
30=180Х
Х= 30 180
Х=0, 1666 или 16, 66%
(при этом повторяем математическое правило перевода числа в %).
Наиболее часто встречающиеся ошибки при решении такого типа задач – математические, ребята могут делить большее число на меньшее (180/30), нарушая правила математики.
Затем на основании полученного раствора можно решать задачи на увеличение концентрации раствора: добавлением соли или упариванием раствора (при упаривании раствора перед стаканом с водой поставим знак «-», соответственно и в математическом выражении ).
Весь материал - в документе.

 Получите свидетельство
Получите свидетельство Вход
Вход




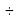 180
180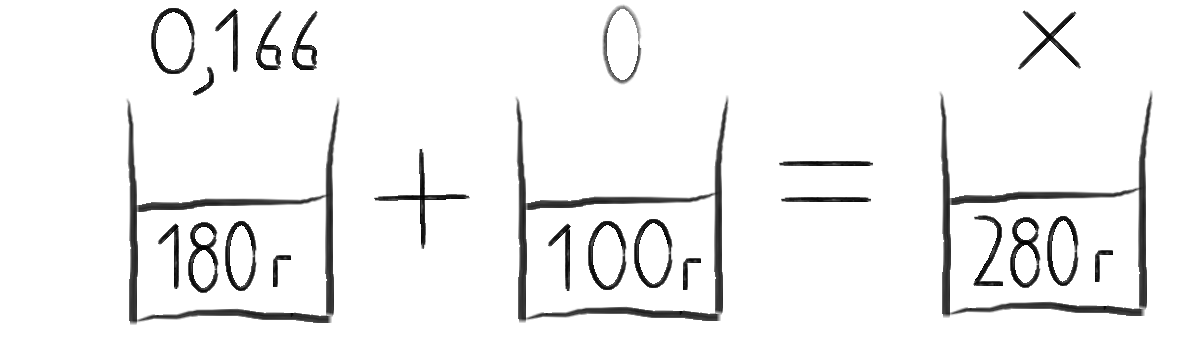
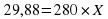
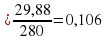
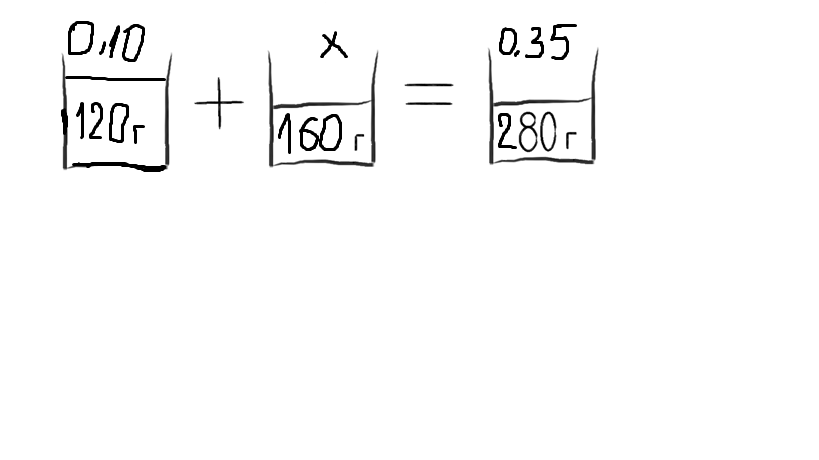









 Графический метод решения задач по химии (0.13 MB)
Графический метод решения задач по химии (0.13 MB)
 0
0 1286
1286 73
73 Нравится
0
Нравится
0


