Практическая работа
Решение задач по теме: «Газовые смеси. Теплоемкость»
Задача 1
Газовая смесь в сосуде состоит из 5 кг диазота N2, 2 кг диоксида углерода СО2 и 3 кг паров воды H2O. Рассчитать парциальные давления составляющих смеси pi, среднюю молярную массу смеси 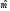 и молярные доли смеси xi , если объём смеси V= 2 м3 и температура T = 500 К.
и молярные доли смеси xi , если объём смеси V= 2 м3 и температура T = 500 К.
Решение.
Определяются молярные массы компонентов смеси
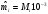 кг/моль, количества веществ
кг/моль, количества веществ 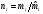 , моль, молярные доли
, моль, молярные доли 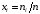 и количество вещества смеси
и количество вещества смеси 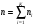 , моль. Результаты расчета сводятся в таблицу:
, моль. Результаты расчета сводятся в таблицу:
|
| вещество |
|
|
|
|
|
| |
| 1 | N2 | 5 | 28 | 0,028 | 178,57 | 0,457 | 0,3711761 | |
| 2 | CO2 | 2 | 44 | 0,044 | 45,46 | 0,116 | 0,0944932 | |
| 3 | H2O | 3 | 18 | 0,018 | 166,67 | 0,427 | 0,3463991 | |
| Смесь | 10 |
|
|
|
|
| ||
Определяется средняя молярная масса смеси
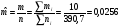 кг/моль
кг/моль
Определяются парциальные давления составляющих смеси
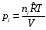 , Па
, Па
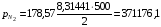 Па
Па
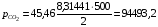 Па
Па
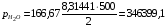 Па
Па
Давление смеси по закону Дальтона
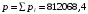 Па
Па
Задача 2.
Газовая смесь состоит из 5 кг диоксида углерода СО2 и 8 кг диазота N2. Изобарные молярные теплоемкости этих газов при температуре Т=298,15 К равны 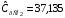 Дж/моль·К,
Дж/моль·К, 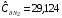 Дж/моль·К. Рассчитать удельную изохорную теплоемкость смеси
Дж/моль·К. Рассчитать удельную изохорную теплоемкость смеси 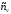 , Дж/кг·К.
, Дж/кг·К.
Решение.
Определяются молярные массы и количества веществ компонентов смеси
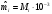 кг/моль,
кг/моль, моль, масса и количество вещества смеси
кг,
, моль и сводятся в таблицу:
| i | вещество |
|
|
|
| |||
| 1 | СО2 | 44 | 0,044 | 5 | 113,636 | |||
| 2 | N2 | 28 | 0,028 | 8 | 285,714 | |||
| Смесь |
| m=13 | n =399,35 | |||||
Определяется общая изобарная теплоемкость смеси
Дж/К.
По уравнению Майера определяется общая изохорная теплоемкость смеси
Дж/К.
Определяется удельная изохорная теплоемкость смеси
Дж/кг·К

 Получите свидетельство
Получите свидетельство Вход
Вход


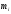 ,кг
,кг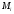
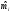 , кг/моль
, кг/моль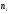 , моль
, моль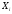
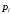 , МПа
, МПа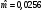
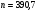
 0,8120684
0,8120684








 Газовые смеси. Теплоемкость (55.04 KB)
Газовые смеси. Теплоемкость (55.04 KB)
 0
0 365
365 0
0 Нравится
0
Нравится
0









