

Эпиграф урока
«Жизнь есть способ существования белковых тел»
Ф.Энгельс

1.Белки (полипептиды)
2.Функции белков
3. Физические свойства белков
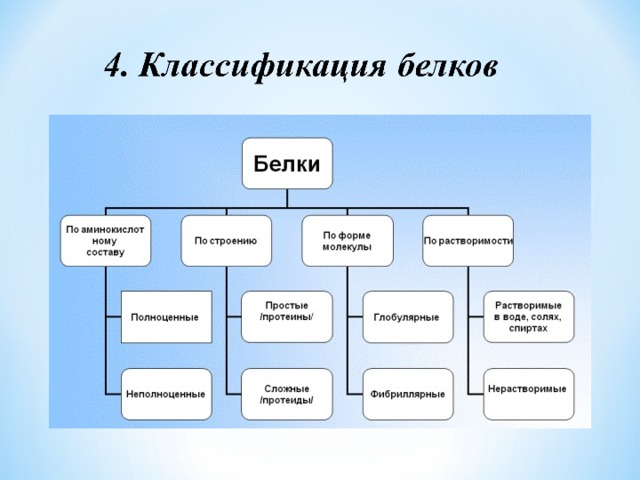
4.Классификация белков
5.Строение белков
6. Химические свойства белков
7.Превращение белков в организме

Происхождение слова белки.
Белки (протеины) «Protos» - первый
Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями. В состав этих биополимеров входят мономеры 20 типов (α-аминокислоты).

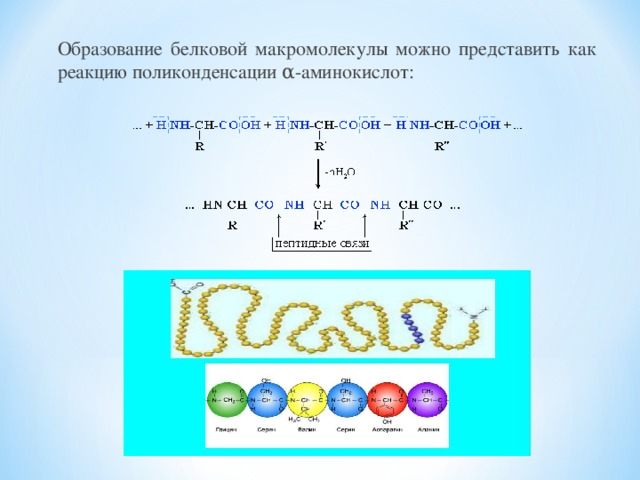
Образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот:

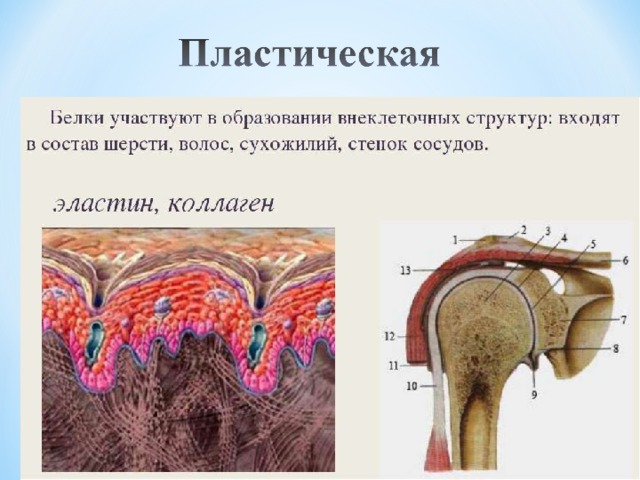
1. Пластическая
Строительный материал клетки
2. Транспортная
Коллаген, мембранные белки
Переносят различные вещества
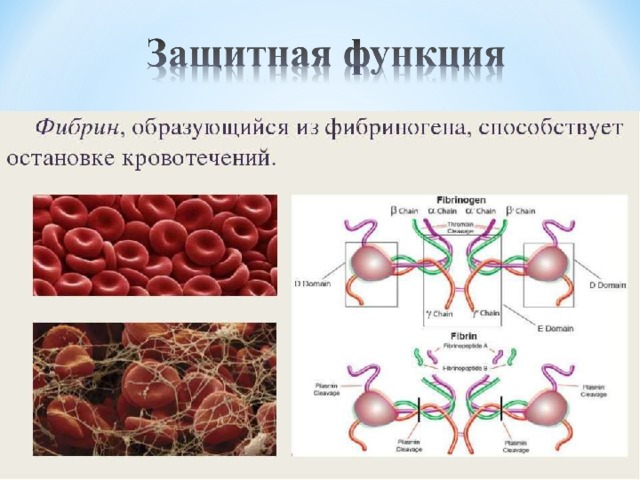
3. Защитная
Гемоглобин
Обезвреживают чужеродные вещества
4. Энергетическая
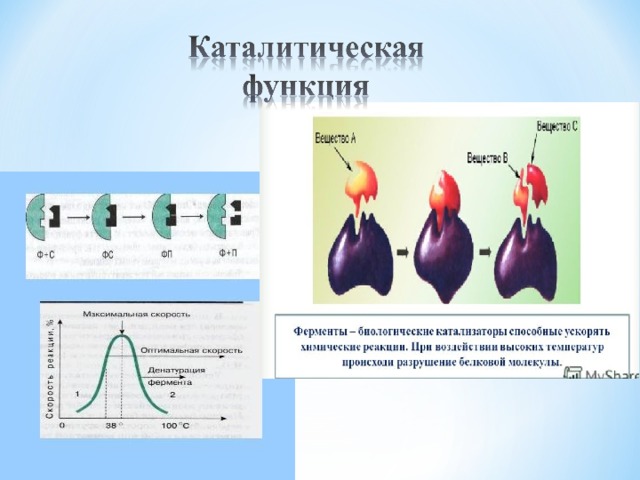
5. Каталитическая
Снабжают организм энергией
γ- глобулин сыворотки крови
При расщеплении 1 г белка освобождается 17,6 кДж энергии
Ускоряют протекание химических реакций в организме
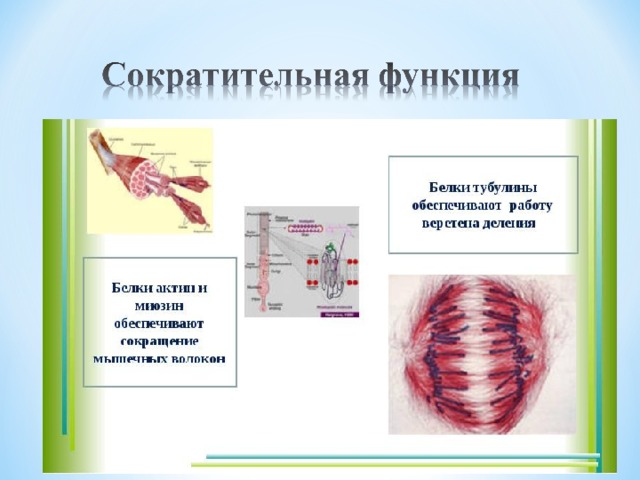
6. Сократительная
Все ферменты по своей химической природе являются белками. Например, рибонуклеаза
Выполняет все виды движений, к которым способны клетки и организмы
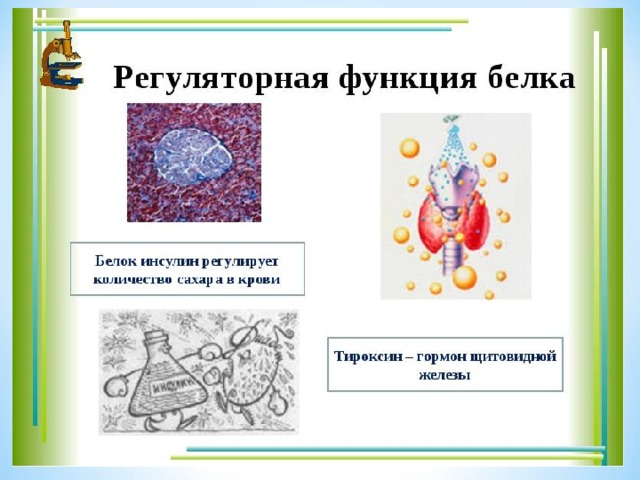
7. Регуляторная
Миозин (белок мышц)
Регулируют обменные процессы
Гормоны, например, инсулин (обмен глюкозы)



3. Физические свойства белков
Работа с учебником

Внимательно прочитайте текст учебника, рассмотрите рисунки. Перечертите в тетрадь и заполните таблицу:
Структура белковой молекулы
Характеристика структуры
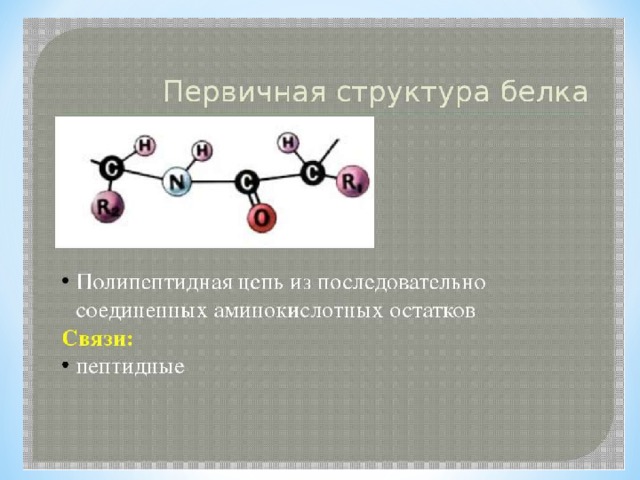
Первичная
Тип связи, определяющий структуру
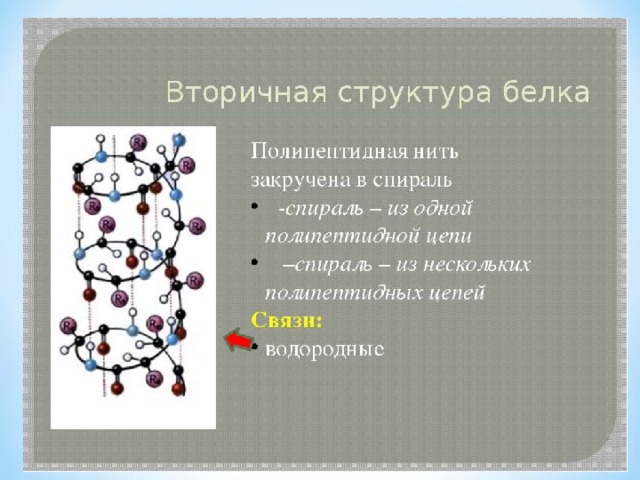
Вторичная
Графическое изображение
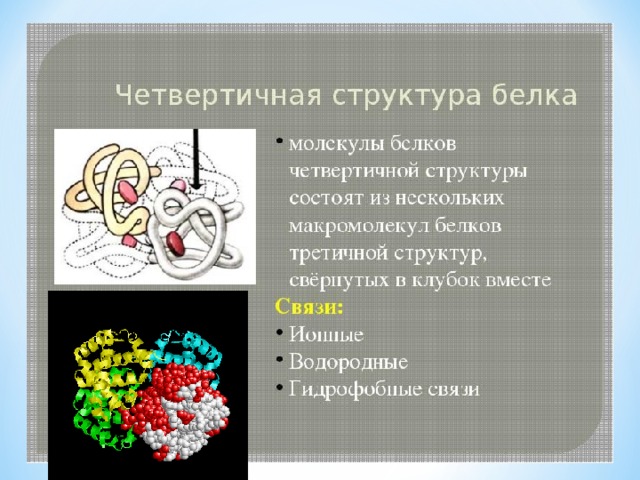
Третичная



Химические свойства белков
В радикалах аминокислотных остатков белки содержат различные функциональные группы, которые способны вступать в реакции. Белки вступают в реакции окисления-восстановления, этерификации, алкилирования, нитрования, могут образовывать соли как с кислотами, так и с основаниями (белки амфотерны).

Химические свойства белков

а) ксантопротеиновая реакция (на остатки аминокислот, содержащих бензольные кольца):
белок + HNO 3 (конц.) → жёлтое окрашивание


б) биуретовая реакция (на пептидные связи):
белок + CuSO 4 (насыщ.) + NaOH (конц.) → ярко-фиолетовое окрашивание


в) цистеиновая реакция (на остатки аминокислот, содержащих серу):
белок + NaOH + Pb ( CH 3 COO ) 2 → чёрное окрашивание


Прием «Микрофон»
Вопросы:
В чем причина несовместимости тканей при пересадке органов от одного организма к другому?
Научное название белков.
Из чего построены молекулы белков?
Сколько структур белка существует?
Структура белка, свернутая в спираль?
Как называется четвертичная структура белка?
Как называется связь - NH – CO - ?
Разрушение структуры белка.
Реакции, определяющие наличие белка?
Пищевые продукты с большим содержанием белка.
Самая неустойчивая структура белка?

Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных водородными связями. В состав этих биополимеров входят мономеры 20 типов.
Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание. Данная реакция называется ксантопротеиновой реакцией. Вторичная структура белков – это чередование аминокислотных остатков в линейной структуре. Денатурация – процесс изменения цвета белковой молекулы. Содержание белка в яйце меньше , чем в молоке и молочных продуктах. При варке яиц белок не меняет свой цвет.

1.На учебном занятии я работал 2.Своей работой на занятии я 3.Учебное занятие для меня показался 4.За учебное занятие я 5.Мое настроение 6.Материал занятия мне был
активно / пассивно доволен / не доволен коротким / длинным не устал / устал стало лучше / стало хуже понятен / не понятен полезен / бесполезен интересен / скучен

 Получите свидетельство
Получите свидетельство Вход
Вход











 "Белки: их строение и свойства" (7.52 MB)
"Белки: их строение и свойства" (7.52 MB)
 0
0 1213
1213 26
26 Нравится
0
Нравится
0



