
Сабақтың тақырыбы:
«Азот»
10-сынып
Сабақтың мақсаты:
Білімділігі: Периодтық жүйедегі азоттың орнына байланысты оны V топ элементі ретінде сипаттау; оқушыларды оның физикалық – химиялық қасиеттерімен таныстыру.
Тәрбиелігі: Дәстүрлі емес оқыту әдісін қолдана отырып,оқушылардың химияға танымдық қызығушылығын арттыру.
Дамытушылығы: О қушыларды өзіндік жұмысқа дағдыландыру және сараптау,салыстыру қабілеттерін дамыту.Өзін-өзі бақылау мен талдауды іске асыру.

Сабақтың түрі:
Жаңа білімді меңгерту
Сабақтың өту әдісі:
Сын тұрғысынан ойлауды дамыту технологиясы.
Д.И.Менделеевтің периодтық жүйесі
Периоды
Қатар
Элементтердің топтары
III
II
I
V
VIII
IV
VII
VI
He
H
1
2
I
1
4,003
1.00797
Гелий
Водород
C
В
Be
F
O
Ne
N
Li
9
10
4
5
7
6
8
3
II
2
18.9984
12,011
10 .811
14.0067
15.996
20,18
9,012
6,939
Вериллий
Неон
Литий
Кислород
фтор
Бор
Азот
Углерод
Cl
Na
Al
S
P
Mg
Si
Ar
11
16
18
17
13
15
14
12
III
3
39,948
35,453
30,9738
32,064
28,086
22,9898
26,9815
24,312
Натрий
Сера
Фосфор
Кремний
Хлор
Алюминий
Магний
Аргон
Ni
K
Sс
Co
Mn
Fe
V
Ca
Cr
Ti
28
22
27
20
21
26
24
23
19
25
IV
4
44.956
58.933
58.71
54.938
39.102
47.90
51.996
40,08
50.942
55.847
Никель
Кальций
Титан
Марганец
Ванадий
Железо
Калий
Скандий
Кобальт
Хром
Cu
Ga
Zn
Br
As
Kr
Se
Ge
35
34
30
29
31
36
33
32
5
78.96
79.904
74.9216
83,8
72.59
69.72
65.37
63.546
Мышьяк
Селен
Медь
Цинк
Галлий
Бром
Криптон
Германий
Pd
Ru
Rb
Nb
Rh
Y
Sr
Mo
Tс
Zr
45
43
42
44
37
38
41
46
40
39
6
V
88.9059
92.906
106.4
95.94
99
87.62
101.07
91.224
85.47
102.905
Рубидий
Родий
Ниобий
Молибден
Палладий
Цирконий
Технеций
Иттрий
Стронций
Рутений
In
Sb
Ag
Sn
Cd
Xe
I
Te
51
47
53
50
52
54
48
49
7
126.904
131,3
127.60
107.868
112.41
121.75
114.82
118.71
Серебро
Ксенон
Индий
Иод
Теллур
Олово
Сурьма
Кадмий
Cs
Hf
W
Ta
Ba
Os
La
Ir
Pt
Re
75
73
74
57
78
76
56
72
55
77
8
VI
195.09
180.9479
178.49
192.2
190.2
137.34
186.2
183.85
132.905
138.81
Барий
Иридий
Цезий
Гафний
Осмий
Лантан
Вольфрам
Рений
Тантал
Платина
Po
Pb
Hg
Rn
Bi
At
Tl
Au
79
85
81
84
82
83
80
86
9
210
[222]
200.59
196.966
207.2
208.98
204.383
208.982
Таллий
Свинец
Ртуть
Полоний
Радон
Висмут
Астат
Золото
Bh
Hs
Ac
Fr
Sg
Db
Rf
Ra
Mt
106
107
104
108
88
105
87
89
109
VII
10
227.028
[262]
[265 ]
[262]
[261]
[223]
[263]
[266 ]
[226]
Резерфордий
Мейтнерий
Радий
Дубний
Актиний
Сиборгий
Франций
Хассий
Борий
4

Азот
Азотты 1772 жылы ағылшын ғалымы Даниэль Резерфорд ашқан. Жер қыртысындағы азоттың мөлшері 0.03%. Табиғатта азот дербес және қосылыстар күйінде кездеседі және негізгі қоры екі атомнан тұратын молекула түрінде ауа құрамында болады. Азоттың ауадағы салмақ үлесі 75.6% , көлем үлесі 78.1%. Жер қыртысының 1 т массасына 1 кг азоттан келеді, әрі ол бейорганикалық және органикалық қосылыстар күйінде кездеседі. Оның бейорганикалық қосылыстарының негізгілеріне натрий нитраты (чили селитрі), калий нитраты (үнді селитрі) жатады. Органикалық қосылыстар күйіндегі азоттың негізгі қоры барлық тірі ағзалардың ақуыздарында құрамына кіреді. Кезінде жанбайтын қасиетіне байланысты “тіршіліксіз” деп аталып кеткенімен азот тіршілікке өте керек элемент. Қалыпты температурада азот түссіз, иіссіз газ.Қайнау температурасы – 196 °C, қату температурасы– 210 °C. Су бір өлшем көлемінде (20 °C-та) 0.0154 көлем азот ериді, яғни азоттың суда ерігіштігі оттектің ерігігтігінен төмен. Ауадан аздап жеңіл болады.

Next
“ Кім білімпаз?”
2
3
1
4
Тапсырмалар
7
5
6

Азот атомының
электрондық
конфигурациясын
жаз.
Back

Азот топшасына
кіретін
элементтер
саны?
Back

Азот қандай тотығу
дәрежелерін көрсетеді?
Back

Азоттың бес валентті
оксидіндегі көрсететін
тотығу дәрежесі?
Back

Азот топшасы
орналасқан
топ нөмірі.
Back

Азоттың сутекті
қосылысының
атауы?
Back

Азот элементінің
атомдық массасы
қанша?
Back

ІІ.”Мағынаны ашу.”
А з о т

Табиғатта
таралуы
Ауада – 78,09%
Адам ағзасында – 3,1 %
(ақуыз, дәрумен, гармон)
Өсімдіктер (ион түрінде)
Топырақта – 0,01 – 0,04 %
Азот - өмір элементі

1772 ж Д. Резерфорд
азотты ашқан
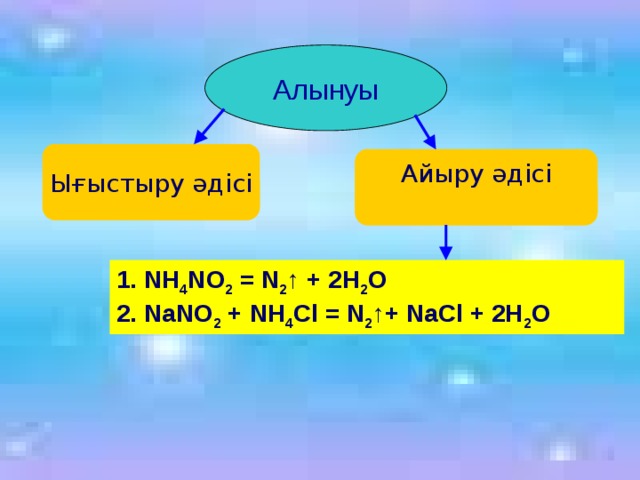
Алынуы
Ығыстыру әдісі
Айыру әдісі
1. NH 4 NO 2 = N 2 ↑ + 2H 2 O
2. NaNO 2 + NH 4 Cl = N 2 ↑+ NaCl + 2H 2 O

Физикалық
қасиеттері
Инертті газ
g = 1,25 г/л(қ.ж)
tб = -210 0 С
tқ = -195,8 0 С
Mr = 28
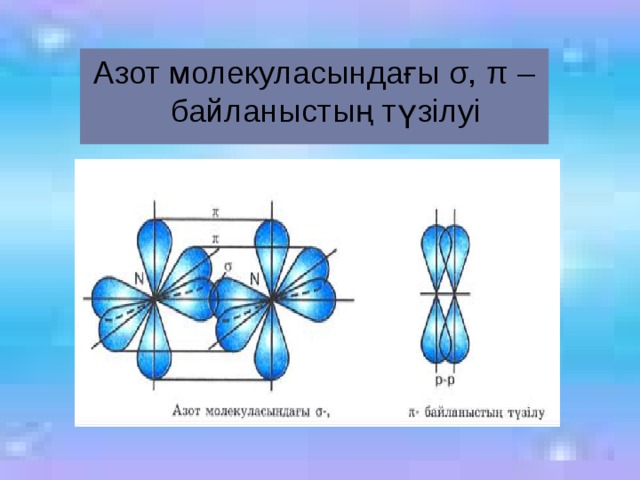
Азот молекуласындағы σ, π – байланыстың түзілуі

Химиялық қасиеттері:
6Li = 2Li3N
2Al = 2AlN
N2 +
O2 = 2NO
3H2 =2NH3
Қолданылуы
Аммиак
Нитрид
синтезінде
алу үшін
Азот
Түрлі
тыңайтқыштар
Азот
қышқылын
Салқындатқыш
жүйе
Инертті
ортада

Азоттың табиғаттағы айналымы

ІІІ кезең:
“ Ой толғау”

“ Кім жылдам? ”
1. Азоттың тотығу дәрежесі +5 болатын қатарды көрсетіңіз:
NO 2
HNO 2
KNO 3
NO
HNO 3
N 2
KNO 3
NaNO 3
NH 4 NO 3
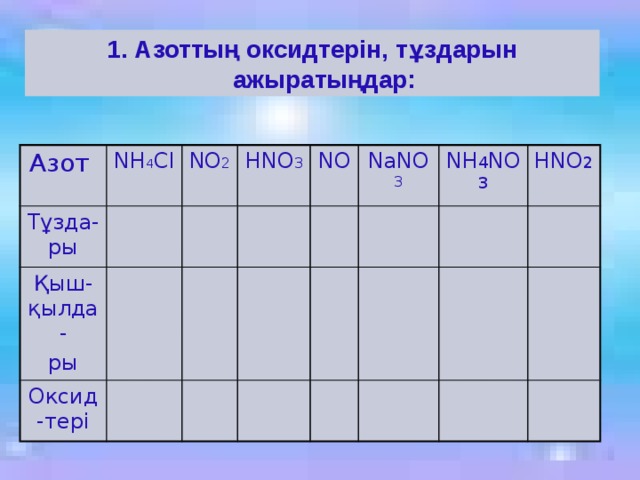
1. Азоттың оксидтерін, тұздарын ажыратыңдар:
Азот
NH 4 Cl
Тұзда-ры
NO 2
Қыш-қылда-
HNO 3
ры
Оксид-тері
NO
NaNO 3
NH 4 NO 3
HNO 2

Сергіту сәті

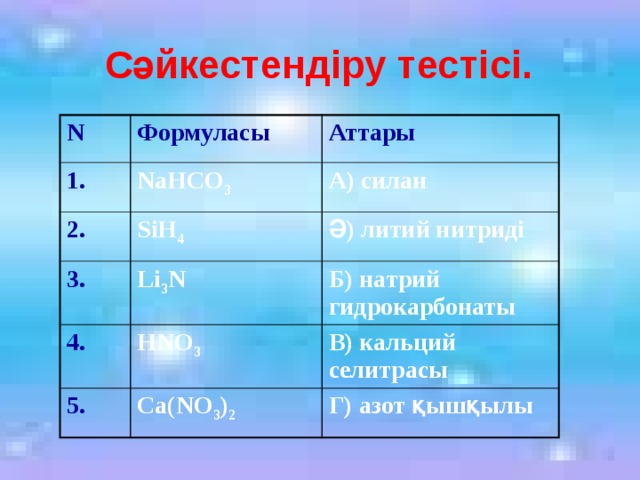
Сәйкестендіру тестісі.
N
Формуласы
1.
Аттары
NaHСO 3
2.
SiH 4
А) силан
3.
4.
Ә) литий нитриді
Li 3 N
HNO 3
Б) натрий гидрокарбонаты
5.
В) кальций селитрасы
Ca(NO 3 ) 2
Г) азот қышқылы

Үйге тапсырма:
§8.9. №7

 Получите свидетельство
Получите свидетельство Вход
Вход











 Азоттың ашылу тарихы (833.77 KB)
Азоттың ашылу тарихы (833.77 KB)
 0
0 1173
1173 5
5 Нравится
0
Нравится
0



