ГБПОУ
САЛАВАТСКИЙ ИНДУСТРИАЛЬНЫЙ КОЛЛЕДЖ
МЕТОДИЧЕСКАЯ РАЗРАБОТКА УРОКА
на тему:
«ПРИМЕНЕНИЕ КАТАЛИЗАТОРОВ В ХИМИЧЕСКОЙ ТЕХНОЛОГИИ. МЕХАНИЗМ ДЕЙСТВИЯ КАТАЛИЗАТОРОВ»
по учебной дисциплине «Теоретические основы химической технологии».
Салават – 2020
Рассмотрено
на заседании цикловой методической комиссии
строительно-технологических дисциплин
Протокол № ____ от ________ 2020г.
Председатель ЦМК
________________ Савина С.Б.
Разработал:
Преподаватель ГБПОУ СИК Е.Г. Алексеева
Рецензент:
Преподаватель ГБПОУ СИК О.Ю. Логинова
Содержание
Аннотация
Учебно-методическая карта урока
Организационная структура урока
Ход урока
Приложение
Список использованных источников
Учебно-методическая карта урока
Тема урока: «Применение катализаторов в химической технологии. Механизм действия катализаторов».
Учебная дисциплина: Теоретические основы химической технологии
Тип урока: урок изучения и первичного закрепления нового материала.
Цели урока:
Обучающие:
- сформировать знания о каталитических процессах и применяемых катализаторах, автокатализе;
- познакомиться с теорией промежуточных соединений в катализе, термодинамические и кинетические аспекты;
- сформировать умения классифицировать каталитические процессы.
Развивающие:
- продолжить формирование навыков работы с различными источниками информации, умения извлекать необходимую информацию из источника.
- развитие интеллектуальных качеств, таких как самостоятельность, гибкость мышления, умение обобщать и анализировать;
- развитие речи, логического мышления.
Воспитательные:
- осуществлять поиск, анализ и оценку информации, необходимой для постановки и решения профессиональных задач, профессионального и личностного развития;
- ставить цели, организовывать и контролировать работу с принятием на себя ответственности за результат выполнения заданий.
Методы и приемы:
- методы словесной передачи и слухового восприятия информации (приемы: информационный рассказ, беседа);
- методы наглядной передачи информации и зрительного восприятия информации (прием: показ компьютерной презентации, видеофрагментов);
- Метод постановки проблемных вопросов в ходе изложения материала;
- рефлексивный метод.
Междисциплинарные связи: ФКХ, органическая и аналитическая химия
Учебно-методическое обеспечение урока:
1. Техническое: ноутбук, проектор, экран.
2. Дидактическое: опорный конспект и раздаточный материал для студентов, мультимедийная презентация, видеофрагменты.
Организационная структура урока
| Этапы урока | Методы обучения | Деятельность преподавателя | Деятельность студентов |
| Организационный момент Задача: обеспечить нормальную внешнюю обстановку для работы на занятии и психологически подготовить студентов к обучению и предстоящему занятию |
| -приветствие; - определение отсутствующих; - определение готовности студентов к уроку.
| - приветствуют преподавателя; - проверяют обеспечение раздаточным материалом.
|
| Мотивация и целеполагание Задача: организовать и направить деятельность студентов, подготовить их к усвоению нового материала; научить учащихся формулировать цель и выбирать конкретные пути ее достижения. | Метод наглядности передачи информации и зрительного восприятия информации. Метод словесной передачи информации и слухового восприятия информации. | Демонстрация презентации
- предлагает студентам обсудить презентацию и самостоятельно сформулировать тему и задачи урока | - Просмотр слайда
- формулируют вместе с преподавателем тему, цели и задачи урока. |
| Усвоение нового материала Задача: мотивировать обучающихся к познавательной деятельности; дать студентам конкретное представление по теме изучаемого вопроса.
| Лекция-диалог. Метод постановки проблемных вопросов в ходе изложения материала. Метод словесной передачи информации и слухового восприятия информации.
| - излагает теоретический материал с использованием презентации;
-задает вопросы по пройденному ранее материалу;
| - слушают преподавателя;
- работают с опорным конспектом;
- отвечают на вопросы преподавателя
|
| Этапы урока | Методы обучения | Деятельность преподавателя | Деятельность студентов |
| Первичная проверка понимания студентами изученного материала Задача: добиться усвоения и воспроизведения изучаемого материала.
| Метод словесной передачи информации и слухового восприятия информации. Метод наглядности передачи информации и зрительного восприятия информации. | - предлагает поучаствовать в ответах на вопросы | - отвечают на вопросы. |
| Закрепление знаний Задача: применение приобретенных знаний в решении задач | Метод словесной передачи информации и слухового восприятия информации. Метод наглядности передачи информации и зрительного восприятия информации. Иллюстрация слайдов презентации с размещением ситуаций. | - предлагает студентам ответить на тестовые задания | - выполняют задание |
| Подведение итогов урока, рефлексия | Метод словесной передачи информации и слухового восприятия;
Рефлексивные методы: самооценка. | - помогает оценить результаты проделанной работы студентов; - отмечает подготовленность студентов к занятию; - определяет степень достижения целей занятия; - выставляет и объявляет оценки | - слушают преподавателя;
- осмысливают и анализируют замечания преподавателя; - оценивают вместе с преподавателем свою работу.
|
| Домашнее задание |
| - сообщает о домашнем задании, комментирует его выполнение; | - слушают преподавателя; - записывают домашнее задание. |
Ход урока
Организационный момент.
Добрый день, уважаемые гости и ребята! Давайте сегодняшнее занятие проведем успешно! Главная задача – быть внимательными, активными, находчивыми, а главное – трудолюбивыми. Показать, как умеем работать.
Мотивация и целеполагание.
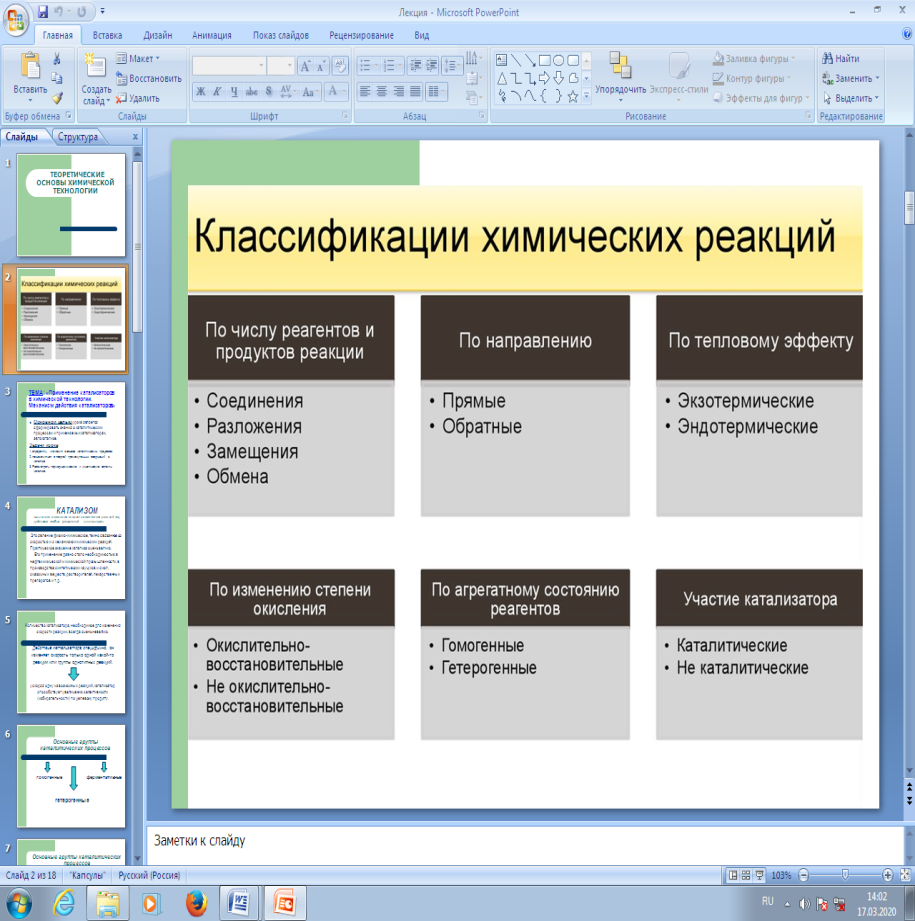
Внимание на экран. Посмотрите внимательно на слайд презентации, где представлена классификация химических реакций по различным признакам. По применению катализаторов – есть каталитического и некаталитического характера. Порядка 90% процессов в химической технологии – каталитические!
Демонстрируется слайд.
Следовательно тема урока - (Сл2) «Применение катализаторов в химической технологии. Механизм действия катализаторов».
Исходя из темы урока давайте попытаемся определить цели и задачи нашего сегодняшнего урока. (Учащиеся участвуют в определении задач урока.)
Основной целью урока является сформировать знания о каталитических процессах и применяемых катализаторах, автокатализе.
(Сл2) Задачи урока:
1. определить, что лежит в основе каталитических процессов
2. познакомиться с теорией промежуточных соединений в катализе
3. Рассмотреть термодинамические и кинетические аспекты катализа.
3. Усвоение нового материала:
(Сл3) Катализом называется изменение скорости химических реакций под действием особых ускорителей – катализаторов.
Катализ – явление физико-химическое, темно связанное со скоростью и с механизмом химических реакций. Практическое значение катализа очень велико. Его применение давно стало необходимостью в нефтехимической и химической промышленности, в производстве синтетических каучуков и смол, смазочных веществ, растворителей, лекарственных препаратов и т. д.
(Сл4) Количество катализатора, необходимое для изменения скорости реакции, всегда очень невелико. Действие катализатора специфично, он изменяет скорость только одной какой-то реакции или группы однотипных реакций.
Таким образом, ускоряя одну из возможных реакций, катализатор способствует увеличению селективности (избирательности) по целевому продукту.
(Сл5) Основные группы каталитических процессов:
- гомогенные;
- гетерогенные;
- ферментативные.
Как же отличить эти группы…
(Сл6) При гомогенном катализе и катализатор, и реагенты находятся в одной фазе (газовой или жидкой). При гетерогенном катализе катализатор и реагенты или продукты реакции находятся в разных фазах (обычно применяют твердые катализаторы). При ферментативном катализе катализатор находится в коллоидном состоянии. Ферментативные каталитические процессы протекают в биологических системах под воздействием ферментов.
Наша задача рассмотреть сущность гомогенного и гетерогенного катализа.
(Сл7) Сущность катализа заключается в образовании промежуточных активированных комплексов субстрата с катализатором. Это вызывает перераспределение электронной плотности в молекуле субстрата и делает ее реакционноспособной.
Любой каталитический процесс является равновесным процессом. Образование промежуточного активированного комплекса, а затем перегруппировка связей в нем требует затраты энергии активации. Распад промежуточного комплекса связан с увеличением энтропии, т.е. термодинамически возможен и самопроизволен. Использование катализатора способствует либо распаду (разрыхлению) промежуточного комплекса, либо его образованию. И то, и другое приводит к увеличению скорости реакции. В гетерогенном катализе образование активированного промежуточного комплекса связано с сорбцией исходных веществ на поверхности катализатора, т.е. с адсорбцией (Сл 8-9).
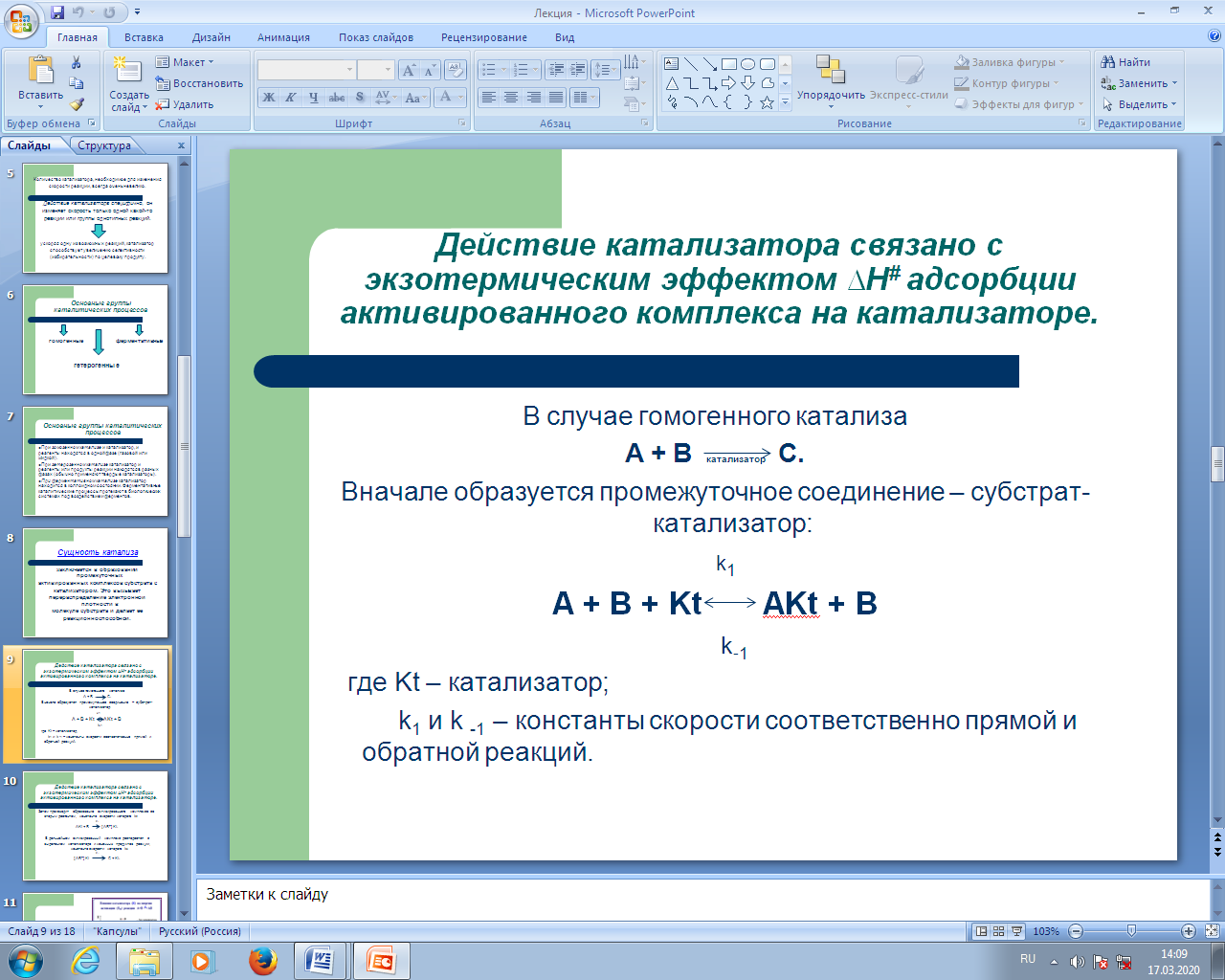
(Сл10) Действие катализатора связано с экзотермическим эффектом ∆Н# адсорбции активированного комплекса на катализаторе.
адсорбции активированного комплекса на катализаторе.
В случае гомогенного катализа
А + В 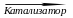 С.
С.
Вначале образуется промежуточное соединение – субстрат-катализатор:
k1
А + В + Kt ↔ AKt + B,
k-1
где Kt – катализатор;
k1 и k -1 – константы скорости соответственно прямой и обратной реакций.
(Сл11) Затем происходит образование активированного комплекса со вторым реагентом, константа скорости которого k2
AKt + B 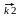 [ AB#] Kt.
[ AB#] Kt.
В дальнейшем активированный комплекс распадается с выделением катализатора и конечных продуктов реакции, константа скорости которого k3
[ AB#] Kt 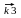 C + Kt.
C + Kt.
(Сл12) Действие гомогенного катализа в подавляющем большинстве случаев определяется экзотермическим эффектом образования активированного комплекса. В гомогенном катализе скорость реакции прямо пропорциональна концентрации катализатора.
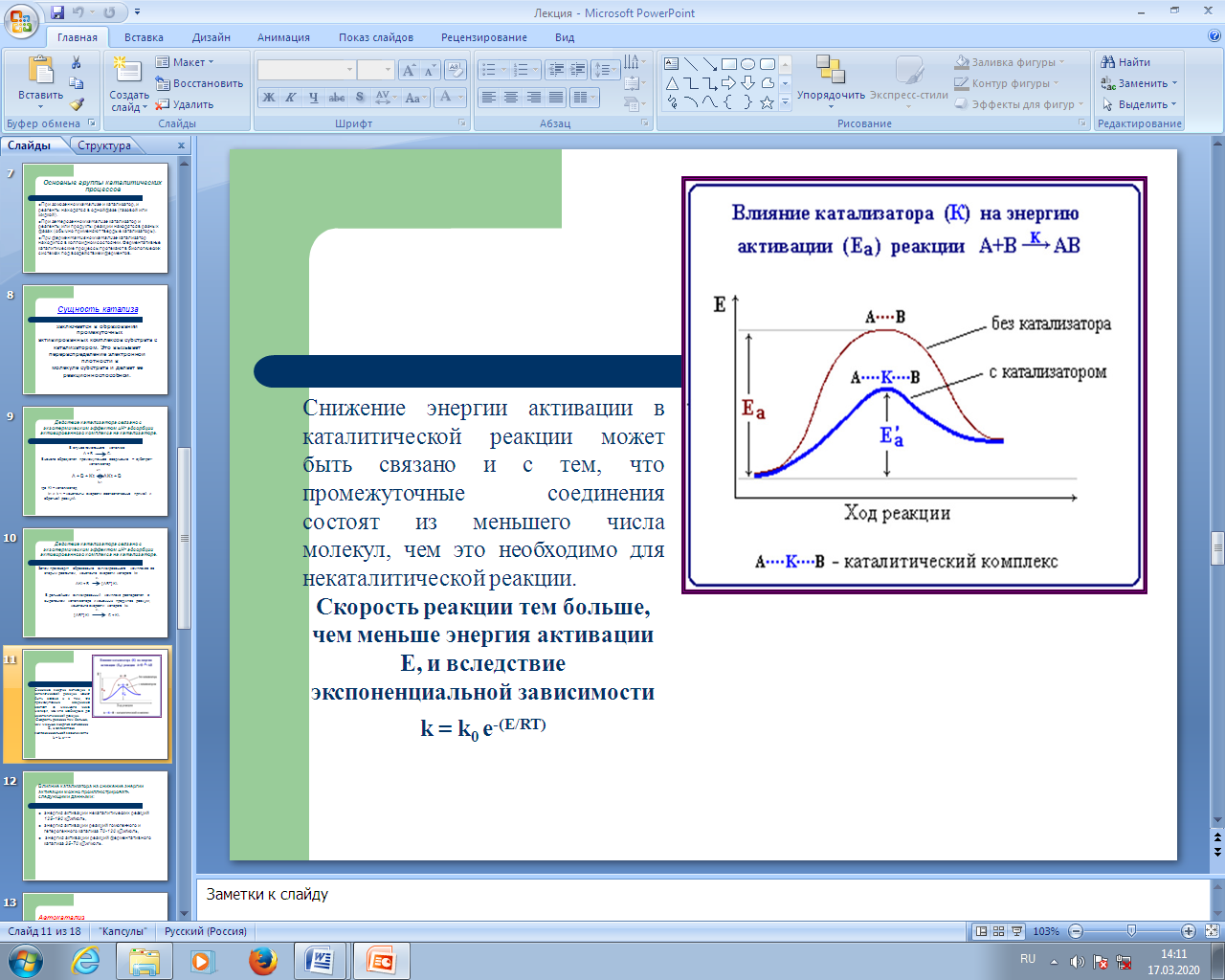
Снижение энергии активации в каталитической реакции может быть связано и с тем, что промежуточные соединения состоят из меньшего числа молекул, чем это необходимо для некаталитической реакции.
Скорость реакции тем больше, чем меньше энергия активации Е, и вследствие экспоненциальной зависимости
k = k0 e-(E/RT)
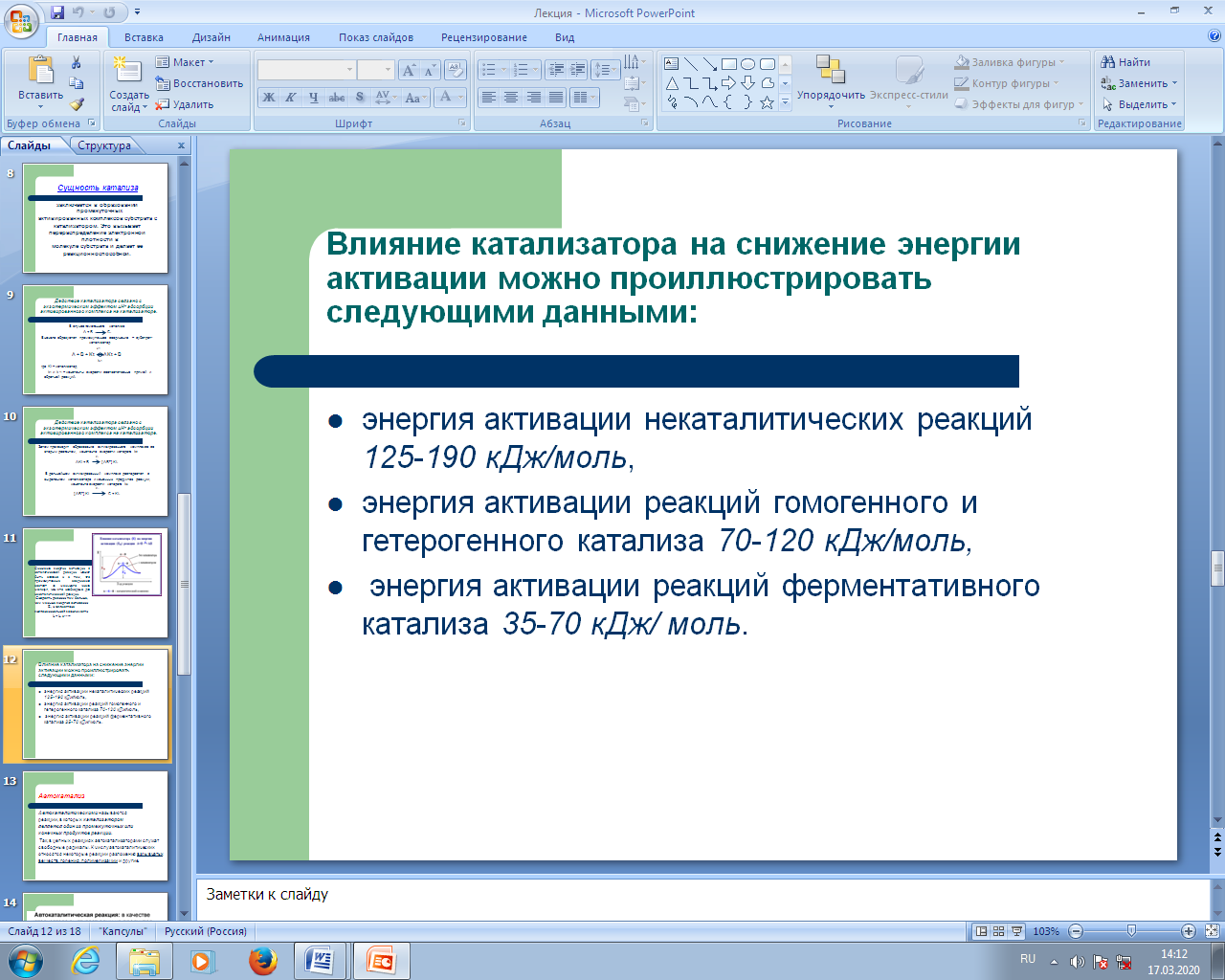
(Сл13) Влияние катализатора на снижение энергии активации можно проиллюстрировать следующими данными: энергия активации некаталитических реакций 125-190 кДж/моль, энергия активации реакций гомогенного и гетерогенного катализа 70-120 кДж/моль, энергия активации реакций ферментативного катализа 35-70 кДж/ моль.
Предлагаю рассмотреть понятие «автокатализ». (Сл14) Автокаталитическими называются реакции, в которых катализатором является один из промежуточных или конечных продуктов реакции. Так, в цепных реакциях автокатализаторами служат свободные радикалы. К числу автокаталитических относятся некоторые реакции разложения взрывчатых веществ, горения, полимеризации и другие.
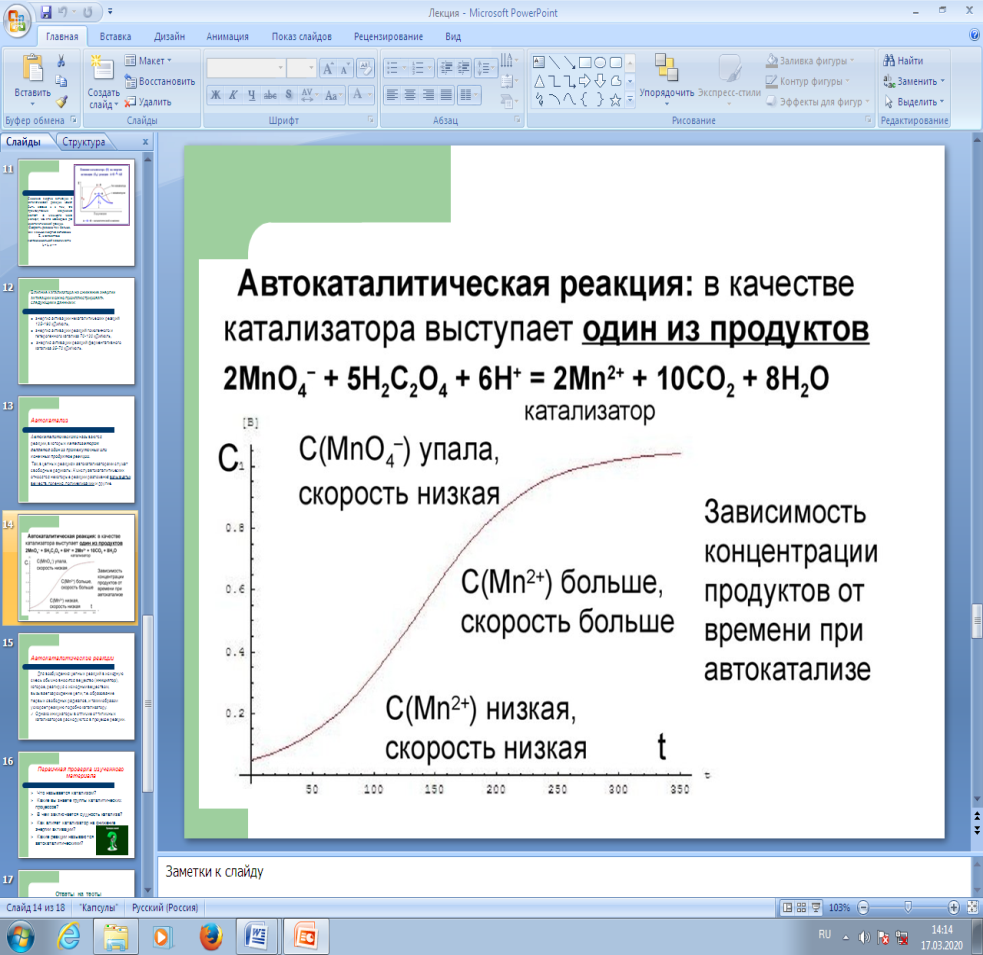
(Сл15) Для автокатализа характерна малая скорость реакций в начальный период, называемый периодом индукции, и быстрое нарастание выхода продукта в последующий период в результате возрастания количества катализатора. В дальнейшем выход продукта увеличивается согласно закону действующих масс, так же как и для обычных реакций.
(Сл16) Для возбуждения цепных реакций в исходную смесь обычно вносится вещество (инициатор), которое, реагируя с исходным веществом, вызывает зарождение цепи, т.е. образование первых свободных радикалов, и таким образом ускоряет реакцию подобно катализатору. Однако инициаторы в отличие от типичных катализаторов расходуются в процессе реакции.
Теперь необходимо закрепить вышесказанное.
Первичная проверка изученного материала
А сейчас я предлагаю вам поучаствовать в ответах на следующие вопросы (Сл17):
Что называется катализом?
Какие вы знаете группы каталитических процессов?
В чем заключается сущность катализа?
Как влияет катализатор на снижение энергии активации?
Какие реакции называются автокаталитическими?
Закрепление
Решение теста по закреплению материала.
На столах учащихся лежат листы с тестами, на которые необходимо ответить в течение 5-7 минут, после чего меняемся ответами с рядом сидящими товарищами.
| Вопрос | Варианты ответа |
| 1. Изменение скорости химических реакций под действием особых ускорителей, называется? | А) изомеризация Б) катализ В) экстракция |
| 2. Реакции, в которых катализатор является одним из промежуточных или конечных продуктов реакции, называются? | А) автокаталитическими Б) изотермическими В) обратимыми |
| 3. Образование промежуточных активированных комплексов субстрата с катализатором представляет собой? | А) ферментативность Б) адсорбция В) сущность катализа |
| 4.При каком виде катализа - катализатор, реагенты и продукты реакции находятся в разных фазах? | А) гомогенный Б) гетерогенный В) ферментативный |
| 5.Самое низкое значение энергии активации для какого вида катализа?
| А) гетерогенный Б) гомогенный В) ферментативный |
Затем ОТВЕТЫ представлены на (Сл18).
Поднимите руки, получившие минимальное количество ошибок(0-1).
7. Подведение итогов, рефлексия
Этап рефлексии.
Преподаватель предлагает оценить свою работу на уроке.
Закончите предложения:
- Сегодня я узнал…
- Самым интересным было…
Преподаватель объявляет оценки.
(Сл 19) Домашнее задание – перенести опорный конспект в тетрадь, повторить пройденный материал.
Использованные источники
Основные источники:
1. Москвичев Ю.А., Григоричев А.К., Павлов О.С. Теоретические основы химической технологии. – М.:ACADEMA, 2018. – 272с.
2. Мухленов И.П. и др. Общая химическая технология. Том 1: Теоретические основы химической технологии. – М.: Альянс, 2016.- 255с.
3. Мухленов И.П. и др. Общая химическая технология. Том 2: Важнейшие химические производства. – М.: Альянс, 2016.- 264с.
4. Тимофеев В.С., Серафимов Л.А., Тимошенко А.В. Принципы технологии основного органического и нефтехимического синтеза. – М.: Высшая школа, 2017. – 408с.
Интернет-ресурсы:
1. Портал фундаментального химического образования http://www.chemnet.ru
2. Каталог образовательных Интернет-ресурсов http://www.edu.ru
3. Электронная библиотека по химии и технике http://rushim.ru
Рецензия
на методическую разработку урока по учебной дисциплине
«Теоретические основы химической технологии»,
представленную Алексеевой Екатериной Геннадьевной
Тема урока: «Применение катализаторов в химической технологии. Механизм действия катализаторов».
Из конспекта урока и презентации к уроку видно, что урок продуман и хорошо спланирован. В разработке указаны цели и задачи урока, подробно описан ход урока.
Содержание планируемого занятия направлено на формирование общих, профессиональных компетенций, качеств активной личности. Урок разработан таким образом, чтобы приобретенные студентами знания имели практическую направленность.
Урок насыщен необходимым для работы оборудованием, наглядностью, дидактическим и раздаточным материалом. Материал урока связан с темой урока, таким образом, наблюдается логическое соответствие между темой урока и выбором заданий. Использование на уроке компьютера позволяет не только усилить наглядное представление изучаемого материала, но и способствует более осмысленному его усвоению. Слайдовая презентация содержит весь необходимый, наглядный и практический материал. Все это позволяет увеличить плотность урока и оптимально увеличить его темп.
Таким образом, представленная к рецензии методическая разработка урока соответствует обучению в рамках ФГОС, способствует освоению общих и профессиональных компетенций для специальности «Переработка нефти и газа».
Рецензент:
преподаватель ГБПОУ СИК О.Ю. Логинова
Аннотация
Данный урок является частью раздела «Катализ в химической технологии» курса Теоретические основы химической технологии.
Тема «Применение катализаторов в химической технологии. Механизм действия катализаторов» очень актуальна для современного производства. Данный материал поможет студентам получить базовые знания в области химической технологии, который позволит студентам глубже понять химико-технологические системы.
Основной целью урока является сформировать общие, профессиональные компетенции - знания о каталитических процессах и применяемых катализаторах, познакомиться с теорией промежуточных соединений в катализе. Понимать термодинамические и кинетические аспекты.
Изучая данный материал, студенту необходимо знать основополагающие принципы – классификацию химических реакций, кинетические особенности.
При изучении нового материала применяется словесный, наглядный и практический методы обучения с элементами технологии проблемного обучения.
Познавательная структура урока будет способствовать развитию методов исследовательской работы, профессионального интереса и углублению знаний данной специализации.
Оснащение урока способствует достижению поставленных задач. Используется мультимедийная презентация, раздаточный материал.
Приложение
Приложение 1
«Применение катализаторов в химической технологии. Механизм действия катализаторов».
(опорный конспект)
КАТАЛИЗОМ
называется изменение скорости химических реакций под действием особых ускорителей – катализаторов.
Основные положения науки о катализе:
- катализатором является вещество, которое ускоряет определенную реакцию, непосредственно участвуя в ней, но после окончания реакции выделяется вновь в неизменном виде;
- катализатор лишь ускоряет реакцию, но не смещает термодинамического равновесия в сторону образования целевого продукта.
ОСНОВНЫЕ ГРУППЫ КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ
При гомогенном катализе и катализатор, и реагенты находятся в одной фазе (газовой или жидкой). При гетерогенном катализе катализатор и реагенты или продукты реакции находятся в разных фазах (обычно применяют твердые катализаторы). При ферментативном катализе катализатор находится в коллоидном состоянии. Ферментативные каталитические процессы протекают в биологических системах под воздействием ферментов.
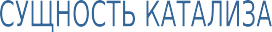
заключается в образовании промежуточных активированных комплексов субстрата с катализатором. Это вызывает перераспределение электронной плотности в молекуле субстрата и делает ее реакционноспособной.
В случае гомогенного катализа
А + В 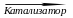 С.
С.
Вначале образуется промежуточное соединение – субстрат-катализатор:
k1
А + В + Kt ↔ AKt + B,
k-1
где Kt – катализатор;
k1 и k -1 – константы скорости соответственно прямой и обратной реакций.
Автокаталитическими называются реакции, в которых катализатором является один из промежуточных или конечных продуктов реакции.
ПРИМЕРЫ: некоторые реакции разложения взрывчатых веществ, горения, полимеризации и другие.
П 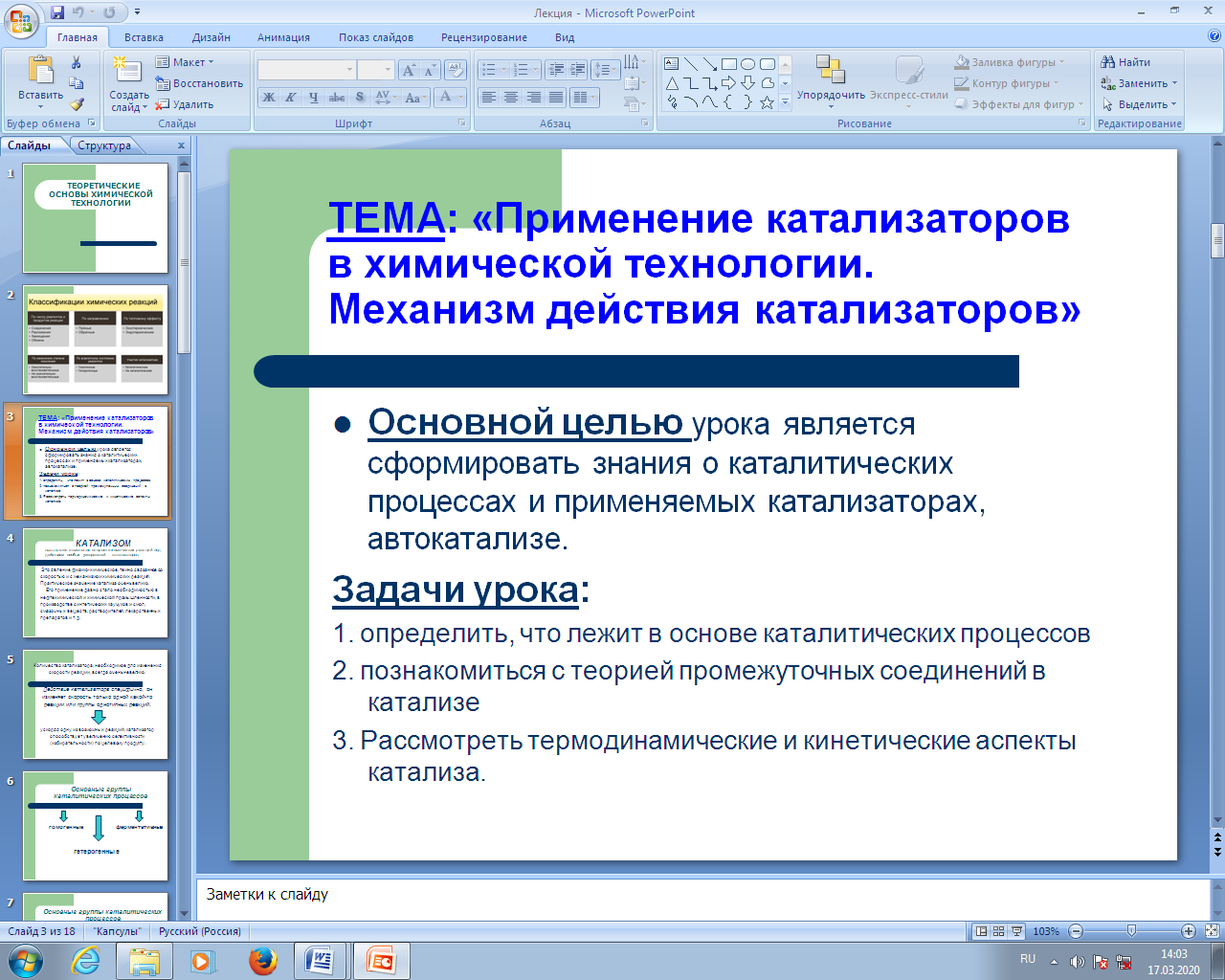 риложение 2
риложение 2




 Получите свидетельство
Получите свидетельство Вход
Вход












 Применение катализаторов в химической технологии. механизм действия катализаторов (4.08 MB)
Применение катализаторов в химической технологии. механизм действия катализаторов (4.08 MB)
 0
0 229
229 1
1 Нравится
0
Нравится
0


