
Сабақтың тақырыбы
- Қаныққан көмірсутектер

Сабақтың мақсаты:
- Алкандар,жалпы формуласы, гомологтық қатары, изомерлері, атаулары ,алкандарды алу және химиялық қасиеттері мен қолданылуы туралы жалпы түсінік беру
- Көмірсутектер туралы білімдерін нығайту және ойлау, есте сақтау дағдыларын дамыту
- Тапсырмаларды орындай отырып , ұқыптылыққа, жауапкершілікке тәрбиелеуге ұмтылу

Сабақтың жоспары:
I . Ұйымдастыру
II. Өткенді қайталау
III. Жаңа сабақ
- Қаныққан көмірсутектердің жалпы формуласы, анықтамасы.
- Гомологтық қатары.
- Изомерия түрлері.
- Атом құрылысы.
- Физикалық қасиеті.
- Алыну жолдары.
- Химиялық қасиеті.
- Қолданылуы.
IV. Сабақты бекіту
V. Қорытындылау
VI. Үйге тапсырма

Алкандар
Алкандар – көміртектің барлық атомдары дара (σ-) сигма байланыспен байланысқан жалпы формуласы мынандай көмірсутектер
C n H 2n+2

Метанның гомологтық қатары
Гомологтар – құрылысы мен қасиеті ұқсас, бір немесе
бірнеше СH 2 . тобына айырмасы бар жалпы формуласы
бірдей заттар
- СН 4 мет ан
- С 2 H 6 эт ан
- C 3 H 8 проп ан
- C 4 H 10 бут ан
- C 5 H 12 пент ан
- C 6 H 14 гекс ан
- C 7 H 16 гепт ан
- C 8 H 18 окт ан
- C 9 H 20 нон ан
- C 10 H 22 дек ан
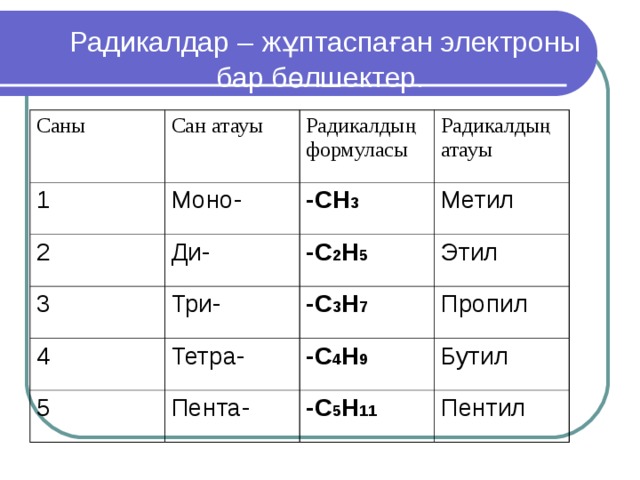
Радикалдар – жұптаспаған электроны бар бөлшектер.
Саны
Сан атауы
1
Моно-
Радикалдың формуласы
2
Радикалдың атауы
-СН 3
Ди-
3
Три-
Метил
-С 2 Н 5
4
5
Тетра-
Этил
-С 3 Н 7
Пропил
Пента-
-С 4 Н 9
Бутил
-С 5 Н 11
Пентил

Алкандардың Изомериясы және номенклатурасы
Құрылымдық:
CH 3 – CH - CH 2 - CH 3
│
CH 3
Алгоритм.
- Негізгі тізбекті таңдап алу:
CH 3 – CH - CH 2 - CH 3
│
CH 3
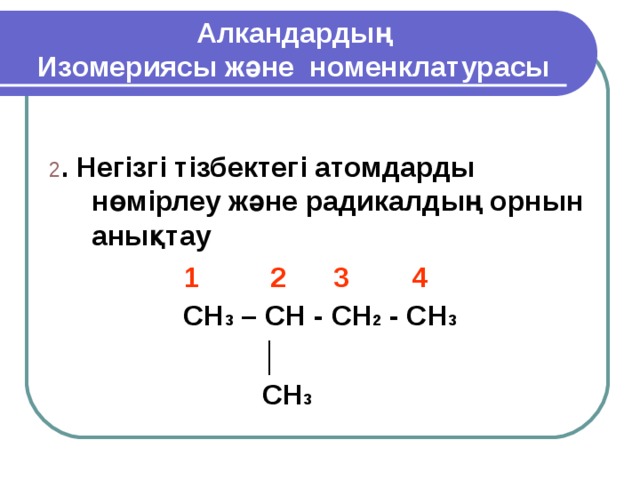
Алкандардың Изомериясы және номенклатурасы
2 . Негізгі тізбектегі атомдарды нөмірлеу және радикалдың орнын анықтау
1 2 3 4
CH 3 – CH - CH 2 - CH 3
│
CH 3
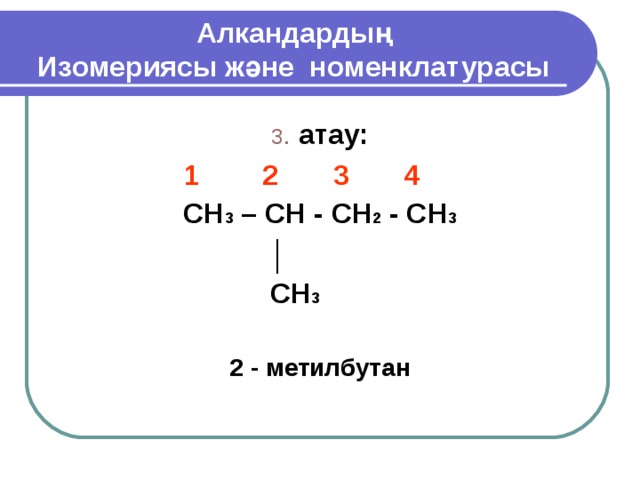
Алкандардың Изомериясы және номенклатурасы
3 . атау:
1 2 3 4
CH 3 – CH - CH 2 - CH 3
│
CH 3
2 - метилбутан
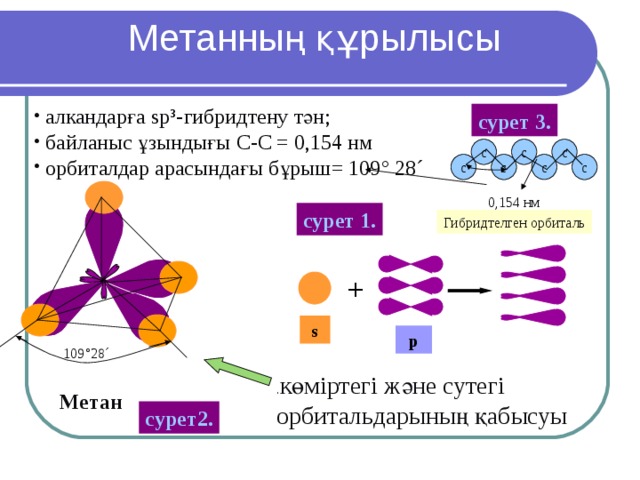
Метанның құрылысы
- алкандарға sp ³- гибридтену тән;
- байланыс ұзындығы С-С = 0,154 нм
- орбиталдар арасындағы бұрыш= 109 ° 28´
сурет 3.
c
c
c
c
c
c
c
0,154 нм
сурет 1.
Гибридтелген орбиталь
+
s
р
109 °28´
. көміртегі және сутегі орбитальдарының қабысуы
Метан
сурет2.
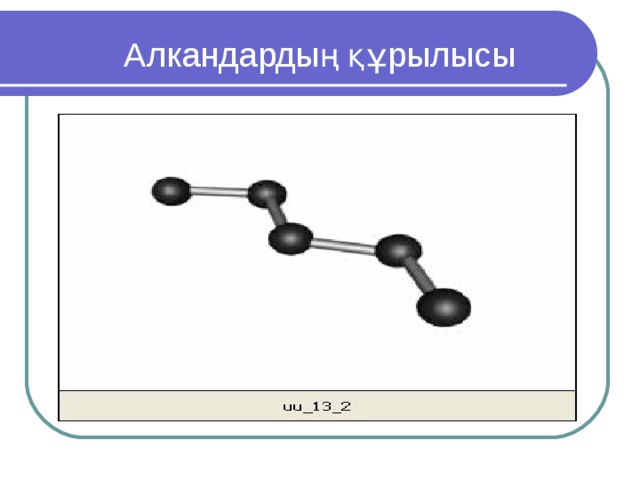
Алкандардың құрылысы
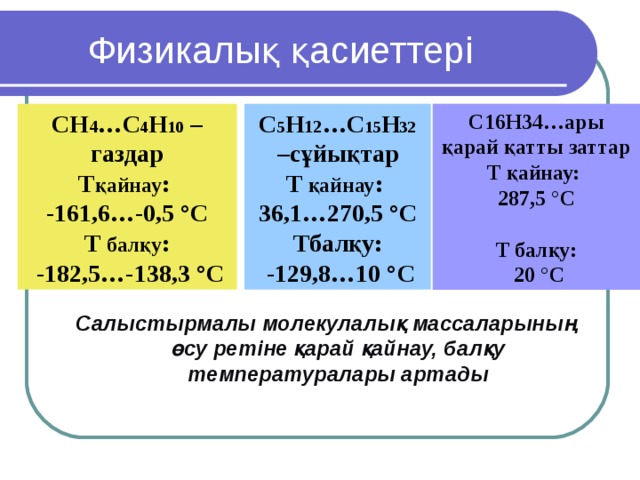
Физикалық қасиеттері
СН 4 …C 4 Н 10 – газдар
T қайнау :
-161,6…-0,5 °C
T балқу :
-182,5…-138,3 °C
С16Н34…ары қарай қатты заттар
T қайнау:
287,5 °C
T балқу:
20 °C
С 5 Н 12 …C 15 Н 32 –сұйықтар
T қайнау :
36,1…270,5 °C
Tбалқу:
-129,8…10 °C
Салыстырмалы молекулалық массаларының өсу ретіне қарай қайнау, балқу температуралары артады

Алынуы
- Өнеркәсіпте
а) мұнай өнімдерін крекингілеу :
C 16 H 34 → C 8 H 18 + C 8 H 16
2) Зертханада :
а) карбидті гидролиздеу:
Al 4 C 3 +12 H 2 O = 3 CH 4 + 4 Al(OH) 3 ↓
б) Вюрц реакциясы :
C 2 H 5 Cl + 2Na → C 4 H 10 + 2NaCl
в) карбон қышқылының натрий тұздарын декарбоксилдеу
СН 3 СООNa + 2NaОН → СН 4 ↑ + Nа 2 СО 3

Метанды алу
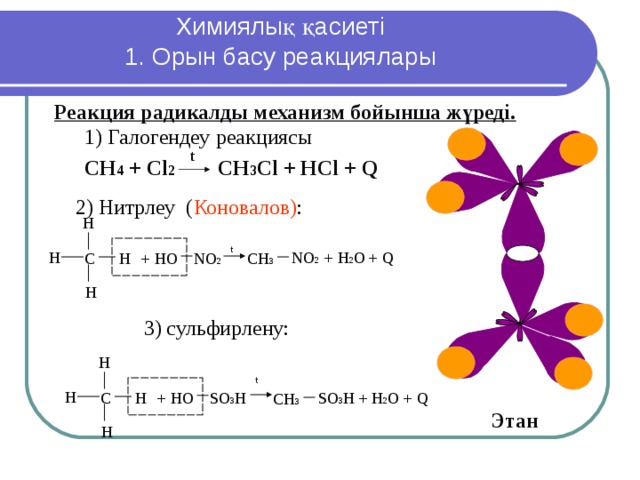
Химиялық қасиеті 1. Орын басу реакциялары
Реакция радикалды механизм бойынша жүреді.
1) Галогендеу реакциясы
t
СН 4 + Сl 2 CH 3 Cl + HCl + Q
2) Нитрлеу ( Коновалов) :
б) Нитрование
Н
t
NO 2
+ H 2 O + Q
Н
+ НО NO 2
СН 3
С Н
Н
в) Сульфирование
3) сульфирлену:
Н
t
Н
SO 3 H
+ H 2 O + Q
С Н
+ НО SO 3 H
СН 3
Этан
Н

t, катализатор
СН 3 СН 2 СН 2 СН 2 СН 3
СН 3 СН СН 2 СН 3
СН 3
800 ° С
СН 4 + Н 2 О СО + 3Н 2
синтез-газ
1500 ° С
2СН 4 Н С ≡ С Н + 3Н 2 + Q
СН 3 СН 3 Н 2 С=СН 2 + Н 2 + Q
Қаныққан көмірсутектер оттегі жеткілікті болғанда
көмірленбей жанады )
3СО 2 + 4Н 2 О + Q
С 3 Н 8 + 5О 2
Катализаторт қатысында тотығады:
О
500 ° С, катализатор
СН 4 + О 2
+ Н 2 О + Q
Н С
Н
2СН 3 (СН 2 ) 34 СН 3 + 5О 2
4СН 3 (СН 2 ) 16 СООН +2Н 2 О + Q

6. Жану тотығу: CH 4 + 2O 2 → CO 2 + 2H 2 O + Q

Алкандардың қолданылуы
Отын ретінде, іштен жанатын двигательдердің отыны ретінде кеңінен қолданылады.

қолданылуы
1-3 – өндірісте күйе
(1 – картрижи;
2 – резина;
3 – типографиялықбояу)
4-7 – органикалық заттар
(4 – еріткіштер;
5 – тоңазытқыштарда;
6 – метанол;
7 - ацетилен)

Бекіту.Бағалау
- Гептанның барлық изомерлерін құрып ата.
- Пентанның екі жақын гомологын жазып ата.
- Ауа бойынша тығыздығы 2 –ге тең көмірсутекті анықта.
Қорытындылау
- «INSERT» кестесінің белгілерін қоя отырып сабақты қорытындылау .
V - ТАНЫС
+ ЖАҢА
? - БІЛГІМ КЕЛЕДІ.
- ОЙЛАҒАН ОЙҒА КЕРІ

 Получите свидетельство
Получите свидетельство Вход
Вход











 Презентация на тему "Алкандар" (1.18 MB)
Презентация на тему "Алкандар" (1.18 MB)
 0
0 4026
4026 99
99 Нравится
0
Нравится
0


