Профильный уровень Тема: Алкадиены (диолефины).
Алкадиены – органические соединения, углеводороды алифатического (ациклического) непредельного характера, в молекуле которых между атомами углерода – две двойные связи, и которые соответствуют общей формуле CnH2n-2, где n =3 или n 3.
1 2 3 4
CH2 == CH –––– CH == CH2бутадиен-1,3
ПУ: Для алкенов характерна sp2-гибридизация. У бутадиена-1,3 у четырех негибридных
p-электронов образуется общее π -электронное облако, в результате чего происходит делокализация двойных связей в молекуле, связи между молекулами C1 и C2, C3 и C4 удлиняются (по сравнению с двойной связью – 0,134 нм), а связь между C2 и C3 укорачивается (по сравнению с одинарной связью – 0,154 нм):
1 2 3 4
CH2 = = = CH = = = CH = = = CH2
0,136нм 0,146 нм 0,136 нм
Такая особенность строения называется эффектом сопряжения двойных связей и определяет реакционную способность алкадиенов.
В названии алкенов содержится суффикс –диен («две» «двойные связи»), обозначающий принадлежность соединения к данному классу.
Классификация| Тип диена | Взаимное расположение двойных связей в молекулах | Примеры |
| 1. Диены с кумулированными связями | Две двойные связи находятся у одного атома углерода | CH2 = C = CH2 Пропадиен (аллен) |
| 2. Диены с сопряженными связями | Двойные связи разделены одной одинарной связью | CH2 = CH – CH = CH2 Бутадиен-1,3 (дивинил) |
| 3. Диены с изолированными связями | Двойные связи разделены двумя или более одинарными связями | CH2 = CH – CH2 – CH = CH2 Пентадиен-1,4 |
Номенклатура: в определении названия алкадиена (как и у всех непредельных углеводородов) положение кратной связи имеет при нумерации преимущество перед остальными.
Виды изомерии:
Для алкадиенов характерны следующие виды изомерии:
Структурная изомерия:
а) изомерия углеродного скелета
1 2 3 4 5 1 2 3 4
CH2=CH – CH = CH – CH3 CH2= C – CH = CH2
|
CH3
пентадиен-1,3 2-метилбутадиен-1,3 (изопрен)
б) изомерия положения кратной связи
1 2 3 4 5 1 2 3 4 5
CH2=CH – CH = CH – CH3 CH3–CH = C = CH – CH3
пентадиен-1,3 пентадиен-2,3
в) Межклассовая изомерия (с циклоалкенами и алкинами)
1 2 3 4 5
CH2=CH – CH = CH – CH3 CH = CH
пентадиен-1,3 | |
CH2 CH2
CH ≡ C – CH2 – CH2 – CH3 \ /
CH2
 пентин-1 циклопентен
пентин-1 циклопентен
ПУ 2. Пространственная изомерия:
а) геометрическая изомерия
5 4 3 2 1
CH3 – CH = CН – CH = CH2
пентадиен-1,3
H Н CH3 H
\ / \ /
C = C C = C
/ \ / \
СH3 CН = CН2 Н CН = CН2
цис-изомер транс-изомер
Физические свойства.
Бутадиен-1,3 и пропадиен – газы; 2-метилбутадиен-1,3 - летучая жидкость; алкадиены с изолированными двойными связями – жидкости; высшие алкадиены – твердые вещества.
Химические свойства.
Химические свойства алкадиенов с изолированными связями протекают так же, как и у алкенов – только в два этапа, а у алкадиенов с сопряженными связями - с некоторыми особенностями: способность присоединять молекулы как в положения 1 и 2 (подобно алкадиенам с изолированными связями – 1,2-присоединение), так и в положении 1 и 4 (перераспределение двойной связи – 1,4-присоединение) – зависит от условий и способа проведения реакций.
Реакции присоединения
гидрирование
а) с изолированными связями
1 2 3 4 5 5 4 3 2 1
CH2=CH – CH2 – CH = CH2 + H – H CH3 – CH2 – CH2 – CH = CH2
пентадиен-1,4 пентен-1
5 4 3 2 1
CH3 – CH2 – CH2 – CH = CH2 + H – H CH3 – CH2 – CH2 – CH2 – CH3
пентен-1 пентан
б) с сопряженными связями
1 2 3 4 5 1 2 3 4 5
CH2 = CH – CH = CH – CH3 + H – H CH3 – CH = CH – CH2 – CH3
пентадиен-1,3 пентен-2
1 2 3 4 5
CH3 – CH = CH – CH2 – CH3 + H – H CH3 – CH2 – CH2 – CH2 – CH3
пентен-2 пентан
галогенирование
а) с изолированными связями
1 2 3 4 5 5 4 3 2 1
CH2=CH – CH2 – CH = CH2 + Br – Br CH2Br – CHBr – CH2 – CH = CH2
пентадиен-1,4 4.5-дибромпентен-1
5 4 3 2 1 5 4 3 2 1
CH2Br – CHBr – CH2 – CH = CH2 + Br – Br CH2Br – CHBr – CH2 – CHBr – CH2Br
4,5-дибромпентен-1 1,2,4,5-тетрабромпентан
б) с сопряженными связями
1 2 3 4 5 1 2 3 4 5
CH2 = CH – CH = CH – CH3 + Br – Br CH2 Br – CH = CH – CH Br – CH3
пентадиен-1,3 1.4-дибромпентен-2
1 2 3 4 5 1 2 3 4 5
CH2Br – CH = CH – CHBr – CH3 + Br – Br CH2Br – CH Br – CHBr – CH Br – CH3
1,4-дибромпентен-2 1,2,3,4-тетрабромпентан
гидрогалогенирование (по правилу Марковникова: при присоединении веществ с полярной ковалентной связью типа HX (где X – это -Hal, -OH и т.д.) к несимметричным непредельным углеводородам по месту разрыва π-связи атом водорода присоединяется к наиболее гидрированному атому углерода, а X – к наименее гидрированному атому углерода)
а) с изолированными связями
1 2 3 4 5 5 4 3 2 1
CH2=CH – CH2 – CH = CH2 + H – Br à CH3 – CHBr – CH2 – CH = CH2
пентадиен-1,4 4-бромпентен-1
5 4 3 2 1 5 4 3 2 1
CH3 – CHBr – CH2 – CH = CH2 + H – Br à CH3 – CHBr – CH2 – CHBr – CH3
4-бромпентен-1 2,4-дибромпентан
б) с сопряженными связями
1 2 3 4 5 1 2 3 4 5
CH2 = CH – CH = CH – CH3 + H – Br à CH3 – CH = CH – CHBr – CH3
пентадиен-1,3 4-бромпентен-2
1 2 3 4 5 5 4 3 2 1
CH3 – CH = CH – CHBr – CH3 + H – Br à CH3 – CH2 – CHBr – CHBr – CH3
4-бромпентен-2 2,3-дибромпентан
5 4 3 2 1
CH3 – CHBr – CH2 – CHBr – CH3
2,4-дибромпентан
ПУ: гидратация (по правилу Марковникова)
а) с изолированными связями
1 2 3 4 5 5 4 3 2 1
CH2=CH – CH2 – CH = CH2 + H – OH à CH3 – CH OH – CH2 – CH = CH2
пентадиен-1,4 пентен-1ол-4
5 4 3 2 1 5 4 3 2 1
CH3 – CH OH – CH2 – CH = CH2 + H – OH à CH3 – CH OH – CH2 – CH OH – CH3
пентен-1ол-4 пентандиол-2,4
б) с сопряженными связями
1 2 3 4 5 1 2 3 4 5
CH2 = CH – CH = CH – CH3 + H – OH à CH3 – CH = CH – CH OH – CH3
пентадиен-1,3 пентен-2ол-4
1 2 3 4 5 5 4 3 2 1
CH3 – CH = CH – CH OH – CH3 + H – OH à CH3 – CH2 – CH OH – CH OH – CH3
пентен-2ол-4 пентандиол-2,3
5 4 3 2 1
CH3 – CH OH – CH2 – CH OH – CH3
пентандиол-2,4
ПУ: диеновый синтез ( р. Дильса-Альдера)
Р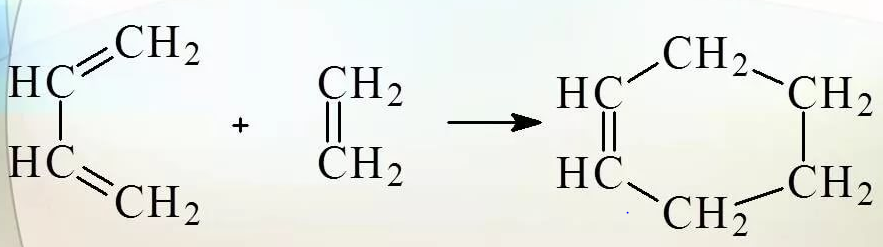
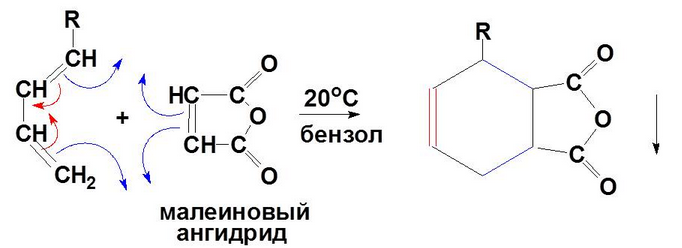 еакция характерна только для сопряженных диенов и соединений с двойными и тройными связями. Продуктами реакции являются шестичленные циклические соединения, обладающие высокой биологической активностью, поэтому используются как лекарственные препараты, средства защиты растений.
еакция характерна только для сопряженных диенов и соединений с двойными и тройными связями. Продуктами реакции являются шестичленные циклические соединения, обладающие высокой биологической активностью, поэтому используются как лекарственные препараты, средства защиты растений.
Реакция является качественной на сопряженные диены.
Реакции полимеризации.
t0, kt
n CH2 = CH – CH=CH2 ––––––– à (– CH2 – CH = CH – CH2 –)n
бутадиен-1,3 бутадиеновый каучук
H H H CH2 –
\ / \ /
C = C C = C
/ \ / \
– H2C CH2 – – H2C H
цис-конфигурация транс-конфигурация
Реакции окисления.
горение 2C4H6 + 11 O2 (избыток) à 8 CO2 + 6 H2O
ч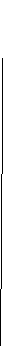 астичное окисление кислородом воздуха с образованием эпоксидов и диэпоксидов t0, Kt
астичное окисление кислородом воздуха с образованием эпоксидов и диэпоксидов t0, Kt
2 CH2=CH – CH = CH2 + O2 ––à CH2 – CH – CH = CH2 ()
\ /
O эпоксибутен-1 (или окись бутена-1)
t0, Kt
2 CH2 – CH – CH = CH2 + O2 à CH2 – CH – CH – CH2
\ / \ / \ /
O O O диэпоксибутан (или диокись бутана)
окисление KMnO4 или K2Cr2O7 в мягких условиях в нейтральной среде
4 3 2 1
CH2=CH – CH = CH2 + KMnO4 + H2О –––––––– CH2– CH – CH = CH2 +…
| |
OH OH (бутен-1диол-1,2)
4 3 2 1
CH2 –CH – CH = CH2 + KMnO4 + H2О –––––––– CH2– CH – CH – CH2 + …
| | | | | |
OH OH OH OH OH OH
(бутантетраол-1,2,3,4)
окисление KMnO4 или K2Cr2O7 в жестких условиях - в кислой среде , при ↑t:
Происходит разрыв двойных связей с образованием карбоновых кислот, кетонов и соединений с двумя функциональными группами.
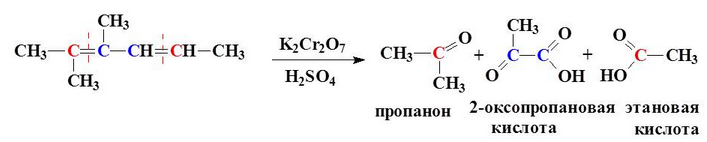
!!! Обесцвечивание раствора KMnO4 – это качественная реакция на непредельные углеводороды.
* Озонолиз. Образуются альдегиды и кетоны.
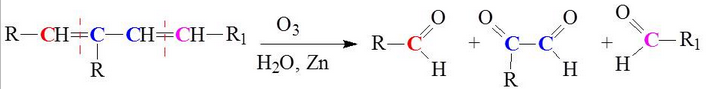
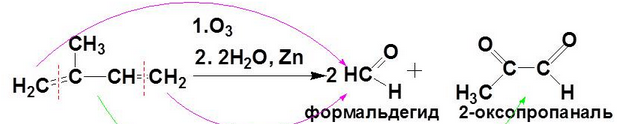
Получение.
I. Промышленные способы:
1. Метод Лебедева (1932г.) – дегидратация и дегидрирование
450oC, Al2O3, ZnO
2 CH3 – CH2 – OH ––––––––––––––––à CH2=CH – CH = CH2 + 2H2O + H2
этанол бутадиен-1,3
2. Способ дегидрирования
500-600⁰C, Kt
CH3– CH2 – CH2 – CH3 –––––––––––à CH2=CH – CH = CH2 + 2H2
н-бутан бутадиен-1,3
(проходит в две стадии)
500-600⁰C, Kt
CH3– CH – CH2 – CH3 –––––––––––à CH2=CH – CH = CH2 + 2H2
| |
CH3 CH3
2-метилбутан 2-метилбутадиен-1,3
(изопрен)
500-600⁰C, MgO, ZnO
CH2 = CH – CH2 – CH3 ––––––––––––––––à CH2=CH – CH = CH2 + H2
бутен-1 бутадиен-1,3
II. Лабораторный способ:
3. Способ дегидрогалогенирования дигалогенпроизводного алкана
Br Br
| | спирт, to
CH2 – CH2 – CH2 – CH2 + 2 KOH –––––––à CH3 = CH – CH = CH3 + 2 KBr + 2 H2O
1,4-дибромбутан бутадиен-1,3
Br Br
| | спирт, to
CH2 – CH2 – CH – CH3 + 2 KOH –––––––à CH3 = CH – CH = CH3 + 2 KBr + 2 H2O
1,3-дибромбутан бутадиен-1,3
(При использовании 2,3-дибромбутана или 2,2-дибромпропана – образуются соответствующие алкины)
Применение.
Диеновые углеводороды применяются в производстве синтетических каучуков, из которых в том числе делают и резину.
Задания по теме: «Алкадиены»
Из перечня формул, приведенного ниже, выберите формулы, которые могут соответствовать алкадиенам: С2Н6 , С8Н16, С9Н16, С7Н16, С4Н6 , С7Н12 , С5Н10, С4Н8
Составьте структурные формулы алкадиенов, состава С6Н10, так, чтобы среди них были изомеры с кумулированными, изолированными и сопряженными связями.
Дайте им названия. Какие виды изомерии характерны для алкадиенов?
Напишите графические формулы следующих алкадиенов:
А) 2,3-диметилбутадиен-1,3 В)3,4-диметилпентадиен-1,3
Б) 2,4-диметилгексадиен-2,4 Г) 2,3-диметилгексадиен-2,4
В чем особенность электронного строения алкадиенов с сопряженной двойной связью? Как это отражается на химических свойствах?
Напишите уравнения реакций:
А) гидрирования 2-метилбутадиена-1,3 (I стадия)
б) бромирования бутадиена-1,3 (I стадия)
В) гидробромирования бутадиена-1,3
г) полимеризации 2-метилбутадиена-1,3 (изопрена)
Составьте уравнения реакций, с помощью которых можно осуществить цепочки превращений веществ:
500-6000С, Сr2O3 kat, p
А) бутан ─→ А → В
Б) этан → этилен → бромэтан→ бутан → бутадиен-1,3 → 1,4-дибромбутен-2 →
→1,4-дибромбутан
В) СН4 →СН3Сl → C2H6 → C2H5Cl →C2H5OH → C4H6
+ Н2 +Сl2 +2 KOHспирт
Г) С2Н5ОН → бутадиен-1,3 → Х → 2,3-дихлорбутан → бутин-2
При сгорании органического вещества массой 17 г образовался углекислый газ объемом 28л и вода массой 18г. Плотность этого вещества по кислороду равна 2,125. Выведите молекулярную формулу органического вещества и составьте структурные формулы его изомеров. Дайте им названия.

 Получите свидетельство
Получите свидетельство Вход
Вход











 Конспект по теме "Алкадиены" (480.5 KB)
Конспект по теме "Алкадиены" (480.5 KB)
 0
0 3891
3891 52
52 Нравится
0
Нравится
0



