 4.
4.
Cr














Сабақ жоспары:
Тақырыбы: Хром және оның қосылыстары
Сабақтың мақсаты:
Білімділік:Оқушыларды хром және оның қосылыстарымен,химиялық қасиеттерімен таныстыру.
Дамытушылық: Оқушылар өз бетінше жауап беру біліктілігін қалыптастыру,негізгі ойды бөліп қорытындылап,салыстыра білуге үйрету.
Тәрбиелік:Уақытты бағалауға,өз бетінше жұмыс істеп,қорытындылай білуге үйрету
Сабақтың көрнекілігі: Периодтық кесте,слайдтар,сызбанұсқа, мультимедия
Сабақтың түрі: Жаңа сабақ
Сабақтың әдісі:сұрақ-жауап, ізденіс, өздік жұмыс, топпен жұмыс .
Пәнаралық байланыс: медицина, биология, тарих, география, математика, физика.
Күтілетін нәтиже: Оқушылардың хорм және оның қосылыстарының маңызын, химиялық және физикалық қасиеттерін меңгеріп, реакция теңдеулерін жазып және реакция типтерін ажырата білуі.
Сабақтың барысы:
І. Ұйымдастыру. (3 мин.)
ІІ. Үй тапсырмасын пысықтау. (сұрақ-жауап) (5 мин.)
ІІІ. Сабақтың мақсатымен таныстыру.
ІV.Жаңа сабақ түсіндіру (17)
а) Хром жайлы жалпы түсінік
б) Периодттық жүйедегі орны
в) Табиғатта таралуы.
г) Алынуы.
ғ) Физикалық қасиеттері.
д) Хром қосылыстары.
е) Хром қосылыстарын анықтау.
ж) Қолданылуы.
V.Жаңа сабақты қорытындылау (20 мин.)
а) Графикалық диктант. Т-кестесі (2 минут)
б) Бос орынға керекті сөзді жазыңыз: (3мин)
в) Адасқан формалар (2 мин)
г) Кластер әдісі (3мин)
ғ) Карточкамен жұмыс. Амалдарды жүзеге асыр (4мин)
д) Блум әдісі (2мин)
VІ.Үйге тапсырма беру. (2 мин.)
Х. Бағалау (2 мин.)
І. Ұйымдастыру.
а) оқушылармен сәлемдесу.
ә) оқушыларды түгендеу.
б) оқушылардың сабаққа дайындығын тексеру.
ІІ. Үй тапсырмасын пысықтау. (сұрақ-жауап)
ІІІ. Жаңа сабақ түсіндіру. Хром және оның қосылыстары:
Хром (Cr )— элементтердің периодтық жүйесінің VI Б тобындағы химиялық элемент, а. н. 24, а. м. 51,996. Тұрақты төрт изотобы бар. Хромды 1797 ж. француз химигі Л.Н. Воклен крокоит минералының құрамынан ашқан. Хром кең тараған элемент. Жер қыртысындағы салмақ мөлшері. 2*10–3%.%. Өнеркәсіптік маңызды минералы — хромит, оның бай кендері Солтүстік Оралда, Кавказ сыртында, Батыс Қазақстанда кездеседі.
Хром +1-ден +6-ға дейінгі тотығу дәрежелерін көрсетеді. Хромның +2, +3, +6 тотығу дәрежелері қосылыстары едәуір тұрақты.
Табиғатта таралуі. Жер қыртысында хромның жалпы мөлшері 0,03%-ті құрайды. Хром әр түрлі минералдардың құрамына кіреді. Хромит немесе хромның темір тас FeCr2O4 едәуір кең таралған, Еліміздегі хромның бай кен орны Ақтөбе облысында орналасқан. Бұл кен орындарындағы хромиттік кендер базасында Ақтөбе және Ақсу ферроқұйма зауыттары жұмыс істейді.
Табиғатта сонымен бірге хром (III) оксиді Сr2O3 және хормның кейбір басқа қосылыстары кездеседі.
Хром ғарышта, Күнде, жұлдыздарда және метеориттерде де бар екені анықталды.
Алынуы.Өнеркәсіпте хромды пирометаллургиялық және алюминтермиялық жолмен алады.
Хромды теміртасты көмірмен қатты қыздырғанда хром мен темірдің тотықсыздануы жүреді:
Fe+2O+Cr2+3O3+4C0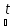 2Cr0+Fe0+4C+2O
2Cr0+Fe0+4C+2O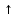
Бұл реакция нәтижесінде хромның темірмен құймасы-феррохром түзіледі.
Таза хромды алу үшін хром(III) оксидін алюминиймен тотықсыздандырады:
Cr2+3O3 +2Al0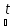 Al2+3O3+2Cr0
Al2+3O3+2Cr0
Физикалық қасиеттері. Хром-күмістей ақ, жылтыр металл. Металдардың ішіндегі ең қаттысы, шыныға жеңіл сызат түсіреді. Хром морт сынғыш, оның тығыздығы 7,2г/см3, балқу температурасы 18550С. Электр және жылу өткізгіштігі төмен.
Химиялық қасиеті. Хромның беті мөлдір оксид қабақшасымен қапталған. Ол өте жұқа (5*10-8), бірақ химиялық тұрақты, оны тіпті қышқылдық өзі қиындықпен бұзады. Осы қабақшаға байланысты хром жемірілуге тұрақты металдардың бірі болып табылады. Тіпті ылғал ауада да өзгермейді.
Жоғары температурада хром оттекте жанып, оксид Cr2O3 түзеді:
4Cr+ 3O3=2Cr2O3
Хром фтормен және хлормен шабытты әрекеттеседі. Қатты қыздыррылған хромнан хлорлы өткізгенде қоңыр қызыл түсті хром (III) хлориді алынады:
2Cr+ 3Cl3=2CrCl3
Қыздырылған хром су буымен әрекеттеседі:
2Cr+ 3H2O= Cr2O3+2H2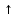
Хром қосылыстары. Хром +2-ден +6-ға дейін тотығу дәрежелерін көрсетіп, қасиеттері әр түрлі қосылыстар түзеді. Хром қосылыстары үшін басқа ауыспалы металдардың қосылыстары сияқты мынадай заңдылықтары тән: тотығу дәрежесі өскен сайын қосылыстарының негіздік және тотықсыздандырғыштық қасиеттері әлсірейді, ал қышқылдық және тотықтырғыштық қасиеттері күшейеді:
Cr
Тотықсыздандырғыш Тотықтырғыш




 Cr+2 Cr+3 Cr+6
Cr+2 Cr+3 Cr+6

CrO Cr2O3 CrO3
негіздік оксид екідайлы оксид қышқылдық оксид



Cr(OH)2 Cr(OH)3 H2CrO4 H2Cr2O7
негіз екідайлы гидроксид хром дихром
қышқылы қышқылы
Хром қосылыстарын анықтау.Барлық хром тұздарының ерітінділерінің түсі бар: Cr2+ -көгілдір түсті, Cr+3 -жасыл күлгін түсті, CrO42--сары түсті және Cr2O73-- қызыл сары түсті. Хромның қышқылдар мен негіздерден түзілген тұздары да ашық түсті, оларды түстері арқылы анықтауға болады.
Қолданылуы.Хромды антижемірілгіш және декоративті қаптамалар жасау үшін қолданады.
Хром тұздарының түсі әр түрлі: күлгін, көк, жасыл, қоңыр, қызыл, сары, қызыл және қара. Оларды пайдаланып, әр түрлі бояулар дайындайды.
Хроматтар мен дихроматтар тотықтырғыштар ретінде қолданады.Хром қосылыстарын тері илеуде пайдаланады. Осындан келіп "хром етік" атауы шыққан. Мұнда тері әдемі, жылтыр, мықты және кигенге ыңғайлы.
V.Жаңа сабақты қорытындылау
1.Графикалық диктант. Т-кестесі ( иә +, жоқ -) (3мин)
1. Хром жұмсақ метал (жоқ)
2. Cr+3-жасыл күлгін (иә)
3. Сутекпен әрекеттесуге бейім емес (иә)
4. Хромды тоқыма өнеркәсібінде мата ағартуға, дәрі-дәрмек, косметика жасауда қолданылады. (жоқ)
5. Хромды теміртасты көмірмен қатты қыздырып алады. (иә)
6. Хромның электр және жылу өткізгіштігі жоғары. (жоқ)
7. тотығу дәрежесі өскен сайын қосылыстарының негіздік және тотықсыздандырғыштық қасиеттері күшейеді, ал қышқылдық және тотықтырғыштық қасиеттері әлсірейді. (жоқ)
8. Хром +2-ден +6-ға дейін тотығу дәрежелер ін көрсетеді (иә)
2.Бос орынға керекті сөзді жазыңыз:
1. Хромды 1797 ж. француз химигі Л.Н. Воклен крокоит минералының құрамынан ашқан.
2. Хромның беті мөлдір оксид қабақшасымен қапталған.
3. Елімізднгі хромның бай кен орны Ақтөбе облысында орналасқан.
4. Металдардың ішіндегі ең қатты.
Керекті сөздер: мөлдір, крокоит минералының, Ақтөбе, қатты, француз.
3.Адасқан формалар
O2Fe(Cr)2 Cr2O7Na2 O3Cr2 Cl3Cr CrO7K2 CrH[Na3(O)6] BaO4Cr
Fe(CrO2)2; Na2Cr2O7; Cr2O3; CrCl3; K2CrO7; Na3[Cr(OH)6]; BaCrO4
5.Карточкамен жұмыс. Амалдарды жүзеге асыр
Cr2O7+OH.........
Fe(CrO2)2 +CFe+ ……
Na2Cr2O7+CCr2O3........
Cr2O3+NaOH+O2.......
| Білетін едім | Білдім | Білгім келеді |
|
|
|
|
VІ.Үйге тапсырма беру. (2 мин.)
§ 7. №4 жаттығу.
Тотығу-тотықсыздану процесіндегі хромның рөлін анықтаңдар:
CrO3+H2S Cr2(SO4)3+S+ H2O
Электрондық баланс әдісімен коэффициенттерін қойыңдар.
Х. Бағалау (2 мин.)
| Ерсінбек А
|
|
|
|
|
|
|
| Сапарова М
|
|
|
|
|
|
|
| Берікқызы А
|
|
|
|
|
|
|
| Зұлпыбекова Қ
|
|
|
|
|
|
|
| Қодарова А
|
|
|
|
|
|
|
| Қанағатова Н
|
|
|
|
|
|
|
| Нұрлыбек А
|
|
|
|
|
|
|
| Райымжанова А
|
|
|
|
|
|
|

 Получите свидетельство
Получите свидетельство Вход
Вход











 Хром және оның қосылыстары (36.55 KB)
Хром және оның қосылыстары (36.55 KB)
 0
0 3089
3089 19
19 Нравится
0
Нравится
0


