РЕЦЕНЗИЯ
на программу факультативного курса по химии в 11 классе
«Химия в промышленности»
Факультативный курс «Химия в промышленности» рекомендуется учащимся, которые проявляют интерес к инженерно-химическим вопросам, к химическому производству, желают получить более глубокие знания по химической технологии, чем те, которые предусмотрены программой по химии. Программа факультативного курса предназначена для учащихся 11 класса. Программа предусматривает 34 –часовой курс, включающий теоретический и практический материал.
В содержании факультативного курса выделены 2 раздела: собственно программа курса, список литературы. Собственно программа состоит из объяснительной записки, содержания указанного факультативного курса, тематического планирования.
В объяснительной записке автор программы формулирует основные цели и задачи курса, раскрывает содержание и обосновывает построение указанного факультатива. Описан основной критерий отслеживания результата работы.
Программное содержание изложено полно, соответствует поставленным целям и задачам. Шетихина О.С. приводит большое количество заданий, направленных на развитое таких познавательных процессов как зрительная и слуховая память, воображение, внимание, развитие мыслительных операций. Указывает основные виды содержательно-логических заданий.
Программа факультативного курса, разработанная Шетихиной О.С.интересна по содержанию, характеризуется самостоятельностью выполнения, научным подходом, обоснованностью положений.
Рекомендую программу Шетихиной О.С.для использования учителями химии школ.
Рецензент: учитель высшей
квалификационной категории Жумалиева К.Т.
Пояснительная записка
Факультативный курс «Химия в промышленности» рекомендуется учащимся, которые проявляют интерес к инженерно-химическим вопросам, к химическому производству, желают получить более глубокие знания по химической технологии, чем те, которые предусмотрены программой по химии. Программа факультативного курса предназначена для учащихся 11 класса. Программа предусматривает 34 –часовой курс, включающий теоретический и практический материал.
В школьном курсе рассматриваются не очень подробно химические производства металлов, неорганических соединений, мало внимания уделяется научным принципам химического производства, энергетике химической промышленности.
Программа предусматривает достаточно подробное практическое и теоретическое изучение не только основных химических производств, но и химические производства Республики Казахстан.
Принципы отбора материала курса.
Проблема определения содержания данного курса сложна, и не столько потому, что необходимо учитывать специфические особенности его проведения в средней общеобразовательной школе, сколько в связи с состоянием и перспективами развития химической технологии, с которыми знакомятся учащиеся в курсе.
В современном химическом производстве реализуются теоретические и тесно связанные с ними прикладные науки. Благодаря быстрым темпам развития науки в кратчайшие сроки меняется характер производства — непрерывно возникают новые технологические процессы, старые совершенствуются, а многие из них отмирают. Наряду со специализацией химических производств идет процесс их сближения на основе механизации и автоматизации, применения электроэнергии, общих принципов организации производства, контроля и планирования. Создается наука о закономерностях управления химическим производством — химическая кибернетика. Поэтому данный курс должен вооружать учащихся знанием общих закономерностей химической технологии и умением использовать эти знания для решения большого круга вопросов, и прежде всего для определения оптимальных условий управления производственными процессами. Необходимо отметить, что для изучения теоретических основ химической технологии требуются глубокие знания по физике и химии и владение более или менее сложным математическим аппаратом.
Учитывая подготовку учащихся по химии, физике и математике и сформулированную выше задачу курса — развитие инженерно-технического мышления учащихся, оказывается наиболее целесообразным раскрывать общие понятия и закономерности постепенно, на конкретных примерах. Эти примеры желательно отобрать таким образом, чтобы можно было наиболее ярко и в то же время доступно подвести учащихся к выводу общих закономерностей химической технологии. При этом изучение любого производства, как бы важно оно ни было для народного хозяйства, в свете задач, стоящих перед курсом, не является самоцелью.
Учащиеся должны получить представление о химической промышленности как важнейшей отрасли народного хозяйства. Она должна предстать перед ними во всем ее разнообразии, в связях с другими областями народного хозяйства.
В результате изучения курса у учащихся должно сформироваться представление о целях, методах, возможностях, своеобразии химической технологии, о месте этой науки среди других наук, об ее связях с фундаментальными теоретическими науками и прикладными. Знакомя с современным состоянием технологии, нельзя пренебрегать ее историей. Учащиеся должны увидеть производственную жизнь в движении, что особенно важно для понимания перспектив развития технологии.
Основной акцент при изучении вопросов курса должен быть направлен на активную работу учеников в классе в форме диалога учитель — ученик, активного обсуждения материала в форме ученик(и) — ученик(и), ученик — учитель.
Задачи курса: формирование умений и навыков комплексного мышления знаний в химии, помощь учащимся в подготовке к поступлению в вузы, удовлетворение интересов увлекающихся химией.
Реализация программы данного курса осуществляется на основе межпредметных связей с биологией, физикой, математикой и ставит своей целью
создание условий для развития у обучающихся интереса к изучению
химии;
развитие умений самостоятельно приобретать и применять знания, оценить свои склонности и интересы к данной области знаний, работать в группе;
формирование творческих способностей учащихся.
В работе с данным содержанием используется коммуникативно-
направленная групповая работа, проектно - исследовательская деятельность,
выделение проблемы, сбор информации, её обработка, обсуждение . Здесь высока роль самостоятельной работы ученика на практических занятиях.
Отследить динамику интереса к курсу, результативность помогут различные виды контроля: тематический, текущий, обобщающий, а также анкетирование.
В качестве конечных продуктов деятельности учащихся могут быть рефераты, доклады, презентации и др. Главной мотивацией работы остаётся познавательный интерес.
Требования к ЗУН учащихся:
Курс будет считаться успешно пройденным, если учащиеся в процессе обучения приобретают следующие конкретные
знания о:
Развитие химической промышленности в РК.
Научных принципах химического производства.
Производстве металлов: чугуна, стали, алюминия в промышленности.
Производстве основных неорганических продуктов: серной кислоты,
аммиака, азотной кислоты, стекла, цемента в промышленности.
Производстве важнейших нефтепродуктов.
В процессе обучения учащиеся приобретают следующие конкретные умения:
Экспериментально решать задачи с производственным содержанием.
Расширять знания о химических производствах, об особенностях химических и технологических процессов, научных принципах.
Планировать работу и поэтапно ее осуществлять, работать с дополнительной литературой; навыки публичного выступления, умение вести дискуссию, проводить презентацию своего проекта.
Формами отчетности учащихся за данный курс могут быть:
По желанию учащихся
1. Презентация проектной работы, защита рефератов.
2. Мини-сочинение «Чем мне был полезен и интересен данный курс».
Учебно –тематический план
курса «Химия в промышленности»
| № | № | Наименование тем | Кол. часов | дата |
|
|
| Введение. Общие научные принципы химического производства. (3 часа) |
|
|
| 1 | 1 | Общие научные принципы химического производства. | 1 |
|
| 2 | 2 | Понятие о химической и механической технологии. Содержание науки «Химическая технология». | 1 |
|
| 3 | 3 | Развитие химической промышленности в Республике Казахстан. Современное состояние химической промышленности в Республике Казахстан и её роль в народном хозяйстве. | 1 |
|
|
|
| Сырье. Энергия. Вода. (12 часов) |
|
|
| 4 | 1 | Полезные ископаемые как сырье для химической промышленности. | 1 |
|
| 5 | 2 | Понятие о сырье, промежуточном продукте (полупродукте), готовом продукте, отходах производства. Виды и классификация сырья: минеральное и органическое; твердое, жидкое и газообразное; природное и искусственное сырье. Запасы сырья. | 1 |
|
| 6 | 3 | Подготовка сырья к переработке: измельчение, обезвоживание, классификация и обогащение сырья; применяемые методы и аппаратура. Флотация твердого сырья. Флотореагенты: пенообразователи, собиратели, регуляторы. Механические и пневматические флотационные машины. Коллективная и селективная флотация. Обогащение жидкого и газообразного сырья. | 1 |
|
| 7 | 4 | Принципы рационального, экологичного использования сырья. Комплексное использование сырья. | 1 |
|
| 8 | 5 | Безотходная технология. Замена пищевого сырья синтетическим. | 1 |
|
| 9 | 6 | Энергетика химической промышленности. | 1 |
|
| 10 | 7 | Виды и источники энергии, применяемой в химических производствах. Энергоемкость химико-технологических процессов. | 1 |
|
| 11 | 8 | Вода и её использование в химической промышленности. Замкнутый водооборот в химическом производстве. | 1 |
|
| 12 | 9 | Временная и постоянная жёсткость воды. | 1 |
|
| 13 | 10 | Требования, предъявляемые к качеству промышленной воды. Подготовка промышленной (технологической) воды: отстаивание, фильтрация, коагуляция, умягчение, обессоливание. Химические и физико-химические методы умягчения воды. | 1 |
|
| 14 | 11 | Материалы в химической промышленности. | 1 |
|
| 15 | 12 | Итоговое занятие. | 1 |
|
|
|
| Основные химические производства Республики Казахстан. Охрана окружающей среды.(19 часов) |
|
|
| 16 | 1 | Понятие металлургии. | 1 |
|
| 17 | 2 | Производство металлов. Классификация металлов .Черные металлы.
| 1 | Презента-
|
| 18 | 3 | Производство чугуна. | 1 |
|
| 19 | 4 | Производство стали. | 1 |
|
| 20 | 5 | Охрана окружающей среды. | 1 |
|
| 21 | 6 | Электрохимические производства. Производства алюминия. | 1 |
|
| 22 | 7 | Силикатная промышленность. Производство стекла. | 1 |
|
| 23 | 8 | Производство цемента и других силикатных материалов. | 1 |
|
| 24 | 9 | Охрана окружающей среды при производстве силикатных материалов. | 1 |
|
| 25 | 10 | Производство минеральных удобрений Роль минеральных удобрений. Фосфорные, азотные, калийные удобрения. | 1 |
|
| 26 | 11 | Химическая переработка топлива. Виды топлива. | 1 |
|
| 27 | 12 | Переработка твердого топлива. | 1 |
|
| 28 | 13 | Переработка нефти и нефтепродуктов. | 1 |
|
| 29 | 14 | Переработка газообразного топлива | 1 |
|
| 30 | 15 | Охрана окружающей среды при химической переработке и добыче нефти и нефтепродуктов. | 1 |
|
| 31 | 16 | Производство аммиака. | 1 |
|
| 32 | 17 | Производство азотной кислоты. | 1 |
|
| 33 | 18 | Производство серной кислоты контактным способом. | 1 |
|
| 34 | 19 | Итоговое занятие. | 1 |
|
Список литературы для учителя:
Краузер Б., Фримантл М.Химия. Лабораторный практикум. – М.: Химия, 1995.
Фримантл М. Химия в действии. Ч.1,2.– М.: Мир, 1991.
Третьяков Ю.Д. Химия и современность. – М.: Просвещение, 1985.
Третьяков Ю.Д. Химия. Справочные материалы. – М.: Просвещение, 1988.
Алексинский В.Н. Занимательные опыты по химии.– М.: Просвещение, 1995.
Пиментел Д., Кунрод Дж Возможности химии сегодня и завтра. – М.: Мир, 1992.
7. Габриелян О.С. Настольная книга учителя химии. 8-11 кл. –
М.: Блик плюс, 2000.
8. Брокгауз Ф. А., Ефрон И. А. Энциклопедический
словарь.— С.-П., 2001.
Список литературы для учащихся:
1. Люцис К.Малая энциклопедия по химии..- М.,2001
2. Гржимек Б. Экологические очерки о природе и человеке.- М.:
Прогресс, 1988.
3. Третьяков Ю.Д.. Химия. Справочные материалы.–
М.: Просвещение, 1988.
4. Габриелян О.С. Химия. 9 кл.– М.: Дрофа, 2005.
5. Габриелян О.С., Остроумов И.Г., Карцова А.А. Химия. 10 кл.–
М.: Просвещение , 2003.
6. Ахметов С.Н. Неорганическая химия. 9 кл.– М. ,
Просвещение, 2000.
Н.Нурахметов, К.Бекишев, Н.Заграничная. Химия /естественно-математическое направление/. 10 класс. –А: Мектеп,2010.
Содержание курса
Общее количество часов – 17.
Тема 1. Введение. Развитие химической промышленности в России. Общие
научные принципы химического производства. (1ч)
Цели и задачи курса «Химия в промышленности». Темы проектных работ и презентаций.
Химизация народного хозяйства, масштаб и структура использования химических процессов. Понятие химической технологии, элементы химической технологии. Общие технологические принципы.
Тема 2. Сырье, энергетика, материалы в химической промышленности.(3ч)
Классификация сырья, его добыча и переработка, поиск новых резервов добычи сырья.
Источники энергии для осуществления химико -технологических процессов, понятие топлива и его классификация, принципы развития топливной энергетики в России.
Конструкционные материалы, классификация материалов по составу. Порошковая металлургия, авиационная и космическая промышленность.
Тема 3. Основные химические производства.(4ч)
Основные группы химико –технологических процессов.
Производство металлов( чугуна, стали, алюминия) : сырье, вспомогательные материалы, основной химический процесс, побочные процессы, особенности технологического процесса, основной продукт, свойства, применение, утилизация побочных продуктов.
Производство основных неорганических продуктов ( аммиака, азотной кислоты, стекла) : сырье, вспомогательные материалы, основной химический процесс, побочные процессы, особенности технологического процесса, основной продукт, свойства, применение.
Производство важнейших органических соединений (ацетилена, уксусной кислоты, метилового спирта, целлюлозы): сырье, вспомогательные материалы, основной химический процесс, особенности технологического процесса, основной продукт.
Производство высокомолекулярных соединений (полиэтилена, пластмасс, синтетического каучука и резины, химических волокон): сырье, вспомогательные материалы, основной химический процесс, особенности технологического процесса, основной продукт.
Тема 4. Основные химические производства Брянской области.(5ч)
Экскурсии на предприятия Брянской области:
Бежицкий камвольный комбинат,
Сталелитейный завод,
«Мальцовский портландцемент»,
Силикатный завод,
Дятьковский хрустальный завод.
Тема 5. Решение экспериментальных задач с производственным содержанием.(2ч)
Распознавание веществ: сырья, продуктов производства. Очистка сырья и продуктов химических производств и определение примесей в них. Получение веществ в промышленности и управление химическими реакциями.
Тема 6. Охрана окружающей среды. (1ч)
Понятие безотходной технологии, создание малоотходных и безотходных производств.
Обезвреживание газообразных отходов, сточных вод.
Тема 7. Заключительное занятие. (1ч)
Подведение итогов. По желанию учащихся :защита проектов, написание мини-сочинения «Чем мне был полезен и интересен данный курс», тест по содержанию курса, оформление дневника по теме:»Химические технологии Брянской области».
Урок 1.
Тема: Развитие химической промышленности в России. Общие научные принципы химического производства.
Цель: -изучить схему химизации народного хозяйства, масштаб и структуру использования химических процессов; понятие химической технологии, элементы химической технологии; общие технологические принципы;
- развивать логическое мышление, творческие способности у учащихся.
Ход урока:
1.Начало занятия. Сообщения задач
2.Предъявление нового материала.
Цели и задачи курса «Химия в промышленности».
Учащимся дается
1.задание по группам по теме «Основные химические производства.»; список используемой литературы (на уроки 3-6)
2.темы проектных работ и презентаций.
Химизация — это внедрение достижений химии в народное хозяйство с целью ускоренного развития производительных сил, повышения эффективности общественного производства и создания условий для удовлетворения материальных и культурных потребностей социалистического общества. Проблема химизации народного хозяйства - необходимость всемерно развивать химическую промышленность как условие успешного развития экономики. Химизация народного хозяйства имеет двоякое значение. Во-первых, она усовершенствует технологию производственных процессов, заменяя механические операции химическим воздействием. Во-вторых, химия вообще и химия полимеров и керамики в частности являются важнейшим источником дешевого сырья и новых материалов. Химизация народного хозяйства включает:
1) широкое использование химических процессов во всех отраслях материального производства;
2) использование в промышленности и строительстве синтетических материалов и пластмасс вместо цветных металлов, сплавов и природных материалов;
3) развитие производства минеральных удобрений и химических средств защиты растений;
4) замену природных материалов и пищевого сырья, расходуемых химической промышленностью на синтетические продукты;
5) развитие химических производств для нужд здравоохранения;
6) использование химических продуктов и синтетических материалов в производстве товаров широкого потребления.
В нашей стране принята «Комплексная программа химизации народного хозяйства», которая предусматривает:
— обеспечение потребностей народного хозяйства в химической продукции, соответствующей требованиям научно-технического прогресса ;
— ускоренное развитие отраслей химической индустрии;
— повышение эффективности использования химической продукции за счет комплексного применения, рационального сочетания с традиционными материалами и расширение сфер ее потребления в различных отраслях народного хозяйства;
— ускорение внедрения химических процессов и методов переработки природного, промышленного, сельскохозяйственного и вторичного сырья, утилизацию отходов для более полного извлечения полезных компонентов»
Основу химизации народного хозяйства составляет химическая промышленность. Поэтому темпы ее развития в нашей стране опережают темпы роста промышленного производства в целом.
ОБЩИЕ НАУЧНЫЕ ПРИНЦИПЫ ХИМИЧЕСКОГО ПРОИЗВОДСТВА
Научную основу химической промышленности составляет химическая технология.
В буквальном смысле слово «технология» означает учение о мастерстве. Однако многие, и не случайно, понимают под технологией последовательность производственных операций, позволяющих сырье превратить в целевой продукт. Некоторые вкладывают в термин «технология» еще более широкий смысл, отождествляя его с последовательностью (алгоритмом) действий в любой области.
Если же говорить о химической технологии, то наиболее емкое определение было дано Д. И. Менделеевым почти 100 лет назад: «Технология — учение о выгодных (т. е. поглощающих наименее труда людского и энергии природы) приемах переработки природных продуктов в продукты, потребные для применения в жизни людей… Дело, например, химии изучать получение железа из его руд, а дело технологии изучить выгоднейшие для этого способы, выбрать из возможностей наиболее приемлемую по выгодности — к данным условиям времени и места...» (Брокгауз Ф. А., Ефрон И. А. Энциклопедический словарь.— С.-П., 1901.— Т. 33.— С. 132).
Обратите внимание, что главным является не просто получение целевого продукта, чем мог бы довольствоваться химик-исследователь, а массовое получение продукта при минимальных затратах ресурсов труда, сырья, энергии, минимальных капитальных вложениях и минимальном ущербе для человека и окружающей природной среды.
В настоящее время под химической технологией мы понимаем важнейшую область знаний в практической - деятельности, которая охватывает вопросы управления процессами химической переработки сырья в целевые продукты, выбранными на основании фундаментальных физико-химических закономерностей с учетом экономических и социальных факторов, ресурсообеспечения и необходимой безопасности производства. Длительное время считали, что основу химической технологии составляют сырье, энергия и аппаратура. В настоящее время выделяют по меньшей мере 10 элементов химической технологии. К ним относятся:
1) физикохимия процесса и поиски оптимальных физико-химических условий его осуществления;
2) сырье, основные и побочные продукты, отходы производства;
3) энергетика процесса, условия максимального полезного действия энергии;
4) аппаратура, среди которой наиболее важны химические реакторы, аппараты для осуществления химико-технологических процессов;
5) материалы аппаратуры и средства их защиты от коррозии, создание новых материалов;
6) аналитический контроль и управление процессом (включая автоматизацию и управление ЭВМ);
7) организация и охрана труда;
8) защита окружающей среды и создание экотехнологии, т. е. технологии, при использовании которой химическое производство не наносит ущерба окружающей среде;
9) экономика производства, включая капиталовложения, производи-
тельность труда и себестоимость продукции;
10) развитие принципиально новых химико-технологических процессов, в том числе с использованием экстремальных воздействий (космическая технология, радиационные, плазмохимические, крио-химические процессы).
В современных химических производствах широко используются общие технологические принципы: непрерывность процесса, противоток, утилизация теплоты реакции (благодаря теплообмену), комплексное использование сырья и отходов производства.
Процессы бывают непрерывные, периодические и циркуляционные. В непрерывных процессах исходное сырье непрерывно подается в реакционный аппарат, а продукты химического взаимодействия отводятся из аппарата. Принцип непрерывности используется в производстве чугуна, при обжиге извести, в контактном способе производства серной кислоты, при синтезе аммиака и в производстве водяного газа.
В периодическом (прерывном) процессе стадии смешивания реагирующих веществ, химического взаимодействия и выделения продуктов реакции, составляющие цикл, следуют друг за другом и периодически повторяются через определенные промежутки времени. В каждом цикле условия протекания реакции непрерывно изменяются, так как с течением времени концентрация исходных веществ уменьшается, что ведет к снижению скорости реакции, изменению температуры и т. д. Вследствие этого периодические процессы менее производительны. Их используют в производстве стали, кокса, многих органических красителей, взрывчатых веществ, соляной кислоты и других химических продуктов.
В современной химической промышленности стремятся (там, где это возможно) перейти от периодических к непрерывным способам производства. Например, периодический способ получения анилина путем восстановления нитробензола чугунной стружкой с соляной кислотой в настоящее время заменен непрерывным методом — каталитическим гидрированием нитробензола водородом.
Некоторые процессы производства осуществляются полунепрерывным путем. Например, в коксохимическом производстве коксование — периодический процесс, а переработка коксового газа — непрерывный.
В циркуляционном (циклическом) процессе реакционная смесь, покидающая реактор, разделяется. Непрореагировавшие исходные смеси после обогащения реагентами снова направляют в аппарат. Применение циркуляционного принципа способствует более полному использованию сырья и позволяет значительно повысить производительность процесса.
В химической технологии осуществляются следующие принципы.
Принцип противотока. Противотоком называется противоположно направленное движение взаимодействующих веществ.
Движение веществ в одном и том же направлении носит название прямотока.. Противоток применяют для реализации оптимальных условий массо- и теплообмена (проведение химических реакций, поглощение газов, растворение твердых тел, охлаждение продуктов реакции, нагревание исходных веществ и т. д.).
Принцип кипящего слоя, или псевдоожижения. Для образования «кипящего слоя» или псевдоожижения, газообразные реагенты продувают через отверстия снизу аппарата, а находящиеся в нем твердые исходные вещества при этом как бы кипят, находясь все время во взвешенном состоянии. Этот принцип получил широкое распространение в химической промышленности для интенсификации гетерогенных процессов, т. е. химического или физического взаимодействия веществ, находящихся в разных агрегатных состояниях (обжиг пирита в производстве серной кислоты, каталитический крекинг нефтепродуктов, сушка влажных материалов, сорбция из газовых смесей и растворов и т. д.).
Принцип утилизации теплоты реакции. Утилизация теплоты реакции,
т. е. использование выделяющейся при химических взаимодействиях теплоты для подогрева исходного сырья или дальнейшей тепловой обработки образующихся продуктов, позволяет резко снижать производственные энергетические затраты. Например, в производстве чугуна в домну подают воздух, нагретый за счет теплоты происходящих реакций.
Принцип использования производственных отходов (комплексное использование сырья, безотходная технология). Превращение отходов в побочные продукты производства позволяет полнее использовать сырье, что в свою очередь снижает стоимость продукции и предотвращает загрязнение окружающей среды. Например, из полиметаллических сульфидных руд при комплексной переработке получают цветные металлы, серу, серную кислоту и оксид железа (III) для выплавки чугуна. Комплексное использование сырья служит основой комбинирования предприятий. При этом возникают новые производства, перерабатывающие отходы основного предприятия, что дает высокий экономический эффект и является важнейшим элементом химизации народного хозяйства.
Организация химического производства — процесс чрезвычайно трудоемкий. Необходимо решить много проблем, связанных с выбором сырья и способов его подготовки, определить оптимальные физико-химические параметры ведения химико-технологического процесса (температура, давление, применение катализатора и т. д.). Современное химическое предприятие характеризуется высокой степенью автоматизации.
3.Взаимоконтроль
Составить структуру отраслей народного хозяйства, указав долю химических производств в каждой из них.





1.Электролиз воды. 1.Легирование. 1.Стекло. 1.Кокс. 1.Лекарства
2.Плазмолиз воды. 2.Эпитаксия 2.Цемент. 2.Прямое 2.Антисептики
3.Газификация угля. 3.Материалы для кабелей 3.Лаки. восстановление Ме 3.Вата, бинты.
4.Энергия Солнца. и корпусов электроприб. 4. Краски. синтез - газом









1.Топливо. 1.Сиропы, эссенции
2
 .Конструкционные 2.Виноделие, напитки
.Конструкционные 2.Виноделие, напитки
материалы. 3. Шоколад, конфеты




1.Переработка ядерного 1.Минеральные удобрения. 1.Синтетические каучуки, 1.Топливо.
топлива. 2.Фунгициды и инсектициды волокна, ткани. 2.Масла и смазки.
2.Теплоносители. 3. Кормовой синтет. белок 2.Парфюмерия, красители, бумага. 3.Автом. камеры.
4. Итоги занятия
Д/з записи в тетрадях.
Урок 2.
Тема: Сырье в химической промышленности.
Цель: -изучить классификацию сырья, основные способы добычи и переработки сырья;
- развивать умение логически излагать свои мысли, сравнивать, анализировать и делать выводы по изученной теме.
Ход урока:
1. Начало занятия. Сообщения задач.
2.Предъявление нового материала.
Лекция- беседа
Любое химическое производство начинается с сырья, которое по происхождению может быть минеральным, растительным или животным. В химической промышленности чаще всего используется минеральное сырье, т. е. добываемые из земных недр природные минералы. Минеральное сырье делится на рудное, нерудное и горючее.
Рудное сырье, или руда, служит для получения металлов. Например, руды железа, марганца, титана состоят главным образом из сульфидов и оксидов соответствующих металлов.
Нерудное минеральное сырье — это горные породы или минералы, являющиеся источником получения неметаллических химических продуктов. К нему относят апатит, фосфорит, гипс, известняк, слюду, хлорид натрия и др.
Горючее минеральное сырье — ископаемые, которые могут служить в качестве топлива (каменные и бурые угли, нефть, природный газ и т. п.). Этот вид сырья иногда называют органическим, так как оно имеет органическое происхождение. В последние годы органическое сырье все чаще используют не в качестве топлива, а как сырье для химической промышленности.
В качестве основной особенности, характеризующей сырье, следует указать на огромные масштабы его добычи и переработки. В настоящее время в мире ежегодно извлекается и перерабатывается 10" т, т. е. 100 млрд. т горных пород, а ведь в качестве сырья, подвергаемого химическому переделу, используются не только горные породы. Чтобы представить себе масштаб этого рода человеческой деятельности, достаточно простейшего расчета: на каждого человека, включая младенцев и стариков, ежедневно приходится 100 кг извлеченных горных пород. Учитывая, что масштаб производств в последние десятилетия значительно возрос, а само производство как в нашей стране, так и за рубежом в целом развивалось по экстенсивной схеме, возникла серьезная проблема истощения естественных источников сырья. Как видно из цветного рисунка I, при сохранении нынешних темпов потребления нефть, газ, уран-235, легкие цветные металлы (исключая алюминий) могут быть исчерпаны к середине следующего столетия.
Проблема сырья существенно усугубляется тем обстоятельством, что сами природные ископаемые распределены в мире исключительно неравномерно. Почти 95% мировых угольных запасов сосредоточены в недрах стран Северного полушария, в том числе 63% — в Азии, 26% — в Северной Америке и около 6% — в Европе. Аналогичная или еще более контрастная неравномерность распределения в литосфере характерна месторождениям нефти и газа, фосфатов и бокситов и др. Значительная часть мировых запасов многих важнейших видов минерального сырья сосредоточена в недрах развивающихся стран. Их удельный вес в суммарных достоверных и вероятных запасах капиталистических и развивающихся стран составляет: нефть — почти 90%, природный газ — около 70%, бокситы — 74%, олово — 87%, кобальт — 90%, медь — более 65%, фосфориты — 75%, никель, сурьма и апатиты — 60%.
Экономика России почти полностью развивается на базе отечественного сырья. Наша страна занимает одно из первых мест в мире по запасам железа, марганца, хрома, свинца, платины, золота, меди, цинка, никеля, титана, кобальта и оказывает существенную помощь странам СЭВ, обеспечивая их каменным углем, природным газом, нефтью, железной рудой.
Однако минеральные богатства недр России также не безграничны. Как и во всех странах мира, условия эксплуатации месторождений минерального сырья с каждым десятилетием, даже с каждым годом становятся все более сложными и требуют непрерывно возрастающих затрат.
Итак, в условиях все возрастающего дефицита сырья необходим поиск новых резервов. К ним относятся:
1) разработка новых источников и методов извлечения сырья в литосфере, гидросфере и атмосфере;
2) разработка новых эффективных методов рециркуляции, т. е. многократного использования металлов и других видов сырья;
3) разработка новых технологий, способных работать на новом сырье или с меньшими затратами ресурсов;
4) использование альтернативных материалов.
Неиссякаемыми источниками сырья являются промышленные и бытовые отходы, так называемое вторичное сырье. Достаточно сказать, что в России и за рубежом в отвалах и хвостохранилищах размещается
1,6 х1012 м3 горных пород и отходов переработки полезных ископаемых, и на каждого человека в год образуется 400 кг бытовых отходов. Металлы в виде вторичного сырья (так называемого скрапа) используют уже сейчас довольно широко: около половины мирового производства стали базируется на скрапе. Он же покрывает от 20 до 60% потребности в важнейших металлах.
До поступления на химическое производство минеральное сырье, как правило, подвергается предварительной обработке, после которой его состав и свойства удовлетворяли бы требованиям данного технологического процесса. Такая обработка состоит из совокупности механических, химических и физико-химических операций: измельчение, укрупнение, обезвоживание, обогащение или флотация. Флотация основана на различной смачиваемости водой полезных компонентов и пустой породы минерального сырья. Например, флотацией полиметаллических сульфидных руд получают концентраты, отделяя при этом пустую породу.
3. Взаимоконтроль
Составить тест по изученной теме.
Примерный тест
1. Рудное сырье, или руда, служит для получения
неметаллов;
металлов;
металлов и неметаллов.
2.Нерудное минеральное сырье является источником получения
неметаллических химических продуктов;
металлических химических продуктов;
металлических и неметаллических продуктов.
3. Горючее минеральное сырье служить в качестве
получения электроэнергии;
конструктивных материалов;
топлива.
4. Неиссякаемыми источниками сырья является
вторичное сырье;
первичное сырье;
не то и не другое
5. До поступления на химическое производство минеральное сырье подвергается предварительной обработке. Она состоит из совокупности
механических;
химических;
физико-химических операций;
всех перечисленных выше операций.
4. Итоги занятия
Д/з записи в тетрадях
Урок 3.
Тема: Энергетика в химической промышленности.
Цель: изучить источники энергии для осуществления химико -технологических процессов; понятие топлива и его классификацию; принципы развития топливной энергетики в России;
- развивать умение логически излагать свои мысли, сравнивать, анализировать и делать выводы по изученной теме .
Ход урока:
1. Начало занятия. Сообщения задач
2.Предъявление нового материала.
Лекция- беседа
ЭНЕРГЕТИКА ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ
Химическая промышленность — самая энергоемкая отрасль народного хозяйства. В таблице 1 показано, какое количество энергии необходимо затратить на получение тонны продукта (алюминия, стали, цемента, нефти, бумаги).
Таблица1. Необходимые количества энергии для производства
1 т продукта. (в среднем в мире)
| Способ получения продукта
| Энергопотребление на 1 т, в ГДж и т условного топлива
|
| алюминия
| стали
| цемента
| нефти
| бумаги
|
| Действующая технология
| 211,0 7,2
| 28,49 0,97
| 9,50 0,32
| 4,75 0,16
| 42,20 1,4
|
| Реально возможная технология
| 179,36 6,1
| 17,94 0,6
| 4,00 0,14
| 3,69 0,126
| 26,38 0,9
|
| Теоретически рассчитанная технология
| 26,37 0,9
| 6,33 0,21
| 0,74 0,025
| 0,42 0,014
| 0,21 0,007
|
| 1 ГДж соответствует 109 Дж; 1 т условного топлива — 29,3 МДж/кг.
|
В России химическая промышленность выпускает 7% всей промышленной продукции, а потребляет 20% энергии. За рубежом это соотношение еще более контрастно.
Основным источником энергии для осуществления химико-технологического процесса является электрическая энергия и внутренняя энергия (получаемая при сгорания топлива).
Электрическая энергия используется:
1) для различных электрохимических процессов (электролиз растворов и расплавов солей);
2) для электротермических процессов (плавление, возгонка, получение элементного фосфора и т. д.);
3) в электромагнитных процессах (разделение продуктов);
4) в электростатических процессах (электрокрекинг углеводородов) .
Внутренняя энергия используется для разнообразных физических процессов (нагревание, плавление, сушка и т. д.) и для нагревания реагентов при химических превращениях.
Топливо — это материал, служащий источником энергии. Название топлива, как правило, отражает его природу или назначение (например, горючие вещества, ядерное топливо, ракетное топливо и т. д.). В горючих веществах основной составной частью является углерод. Эти вещества находят широкое применение для получения энергии или служат сырьем в химической промышленности. По происхождению топливо делится на природное (нефть, уголь, природный газ и пр.) и искусственное (кокс, моторные топлива и пр.), а по агрегатному состоянию — на твердое, жидкое и газообразное. Мировые запасы энергии различных источников приведены в таблице 2, а виды топлива — в таблице 3.
Таблица2. Мировые запасы энергии различных источников
Источники энергии
Запасы энергии, млрд. кВт-ч
480х103
5,8х106
30х106
700х103
80х103
223х103
200х103
150х106
150х103
70х106
23х103
Практически безграничны
Торф
Угли бурые
Угли каменные
Сланцы горючие
Газ природный
Нефть
Древесина (годовой прирост)
Энергия Солнца
Энергия ветра
Энергия приливов и отливов
Энергия рек
Энергия ядерного горючего
Таблица 3. Виды топлива
| Название топлива
| Содержание углерода, %
| Теплота сгорания, кДж/кг
|
| Антрацит
| 95
| 34000
|
| Каменный уголь
| 75—90
| 35000
|
| Бурый уголь | 65—70 | 28000 |
| Торф сухой | 55—60 | 23000 |
| Нефть
| 80—87
| 44000
|
| Природный газ
| До 95% метана
| 50000
|
В настоящее время основным источником получения внутренней энергии служит нефть. В топливно-энергетических балансах промышленно развитых стран доля нефти составляет 47%, газа — 17%, угля — 30%. Остальные 6% приходятся на все прочие источники энергии, включая гидроэлектростанции, атомные электростанции, геотермальные, ветровые, солнечные и другие установки. Тенденция увеличения расхода природного газа и нефти объясняется большей их экономичностью (относительная простота добычи, транспорта, хранения и использования). Однако природные ресурсы нефти и газа ограничены и невосполнимы
Очевидно, что и сегодня, и через 25 лет нефть сохранит свою лидирующую позицию. Вместе с тем ее вклад в энергоресурсы заметно сократится, и будет компенсироваться возросшим вкладом угля, газа, ядерного горючего, энергии Солнца и других видов возобновляемой энергии, включая биоэнергетику.
Основным принципом топливной энергетики нашей страны является максимальное и комплексное энерготехнологическое использование топливных ресурсов.
Из соображений экономии вытекает необходимость:
1) максимального использования теплоты;
2) вторичного использования теплоты;
3) регенерации и рекуперации теплоты;
4) уменьшения потерь теплоты в окружающую среду;
5) максимального использования местных топливных ресурсов и производственных отходов.
Теплота, выделяющаяся при химических превращениях в реакторе, используется для нагревания исходных продуктов . Горячие газы, проходя по трубам, отдают теплоту воде, находящейся в межтрубном пространстве, а образующийся пар применяется далее.
Бережное расходование энергетических ресурсов — хозяйственная политика нашей страны. Это — увеличение к.п.д. технологических процессов, снижение металлоемкости оборудования, снижение удельных расходов энергоресурсов, повышение эффективности процессов производства и передачи электроэнергии.
В будущем восполнение топливных ресурсов связывают с рациональной переработкой угля, который будут сжижать (запасы угля превышают 95% от запасов природных топлив).
Неисчерпаемые возможности таит ядерная энергетика. Расчеты показали, что при правильном использовании урана можно не бояться его истощения в ближайшие тысячелетия. В перспективе получение энергии управляемым термоядерным синтезом ядер дейтерия и трития.
В промышленности твердое топливо сжигают в печах непрерывного действия. Принцип непрерывности осуществляется при помощи подвижной колосниковой решетки (рис. 17) , на которую непрерывно подается твердое топливо. Жидкое топливо вводится в топку через форсунку при помощи водяного пара или сжатого воздуха. Еще лучше смешивается с воздухом и полнее сгорает газообразное топливо. Для сжигания газообразного топлива используются особые керамические печи, в которых горючий газ и требуемое количество воздуха подаются в мельчайшие каналы, где происходит сгорание.
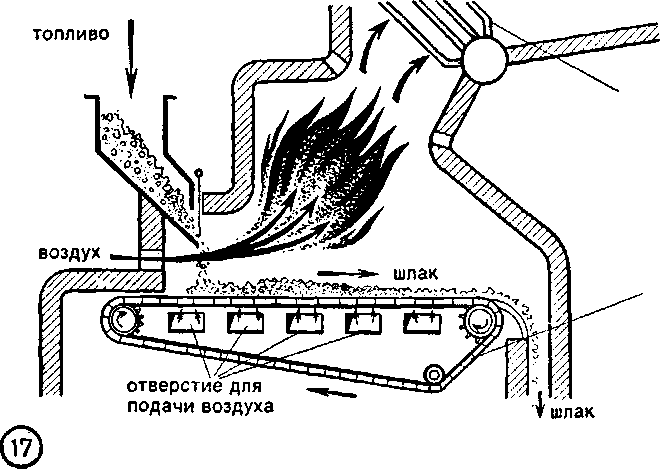
трубы с водой
колосники
Газообразное топливо имеет ряд преимуществ перед твердым топливом: 1) экономически более выгодна добыча и транспортировка;
2) упрощается устройство топок и облегчается труд человека при подаче топлива в печь;
3) упрощается управление процессом горения и облегчается соблюдение гигиены труда;
4) достигается более полное и рациональное сжигание топлива;
5) почти полностью устраняется засорение окружающей среды.
По этим причинам газообразное топливо находит себе все более широкое применение в промышленности, а также в качестве бытового топлива и в автотранспорте.
Природное газообразное топливо — природный газ содержит около 95% метана. Его добывают из газовых или нефтяных месторождений. Искусственное газообразное топливо получают переработкой угля. Это генераторные (воздушный, смешанный, водяной) и коксовый газы. Газообразное топливо является не только удобным видом топлива, но и ценнейшим сырьем в производстве основного органического синтеза (например, ацетилена, метанола, формальдегида и др.). .
Единственное жидкое природное топливо — нефть является сложной смесью циклопарафинов (нафтенов), предельных и ароматических углеводородов. Нефть как топливо непосредственно не применяется, а перерабатывается в товарные нефтепродукты методами фракционированной перегонки, термического и каталитического крекинга, каталитического риформинга и т. д.
Важнейшими группами нефтепродуктов являются топлива и смазочные масла. Нефтяные топлива разделяются на моторные, применяемые в двигателях, и котельные — для сжигания в топках паровых котлов и в промышленных печах.
Первые из них подразделяются в свою очередь на карбюраторные, дизельные и топлива для реактивных авиационных двигателей. Карбюраторным топливом для двигателей внутреннего сгорания с карбюраторами является бензин, важнейшей характеристикой которого является его стойкость к детонации. Детонация — это чрезмерно быстрое сгорание топливной смеси в цилиндре карбюраторного двигателя, нарушающее нормальную работу двигателя. Наиболее склонны к детонации предельные углеводороды нормального строения, тогда как предельные углеводороды с сильно разветвленной цепью детонируют слабо. Способность бензина к детонации оценивается октановым числом. В качестве стандарта принимается к-гептан и 2,2,4-триметилпентан (изооктан), октановые числа которых считают равными 0 и 100 соответственно. Если октановое число равно 80, то это значит, что данный вид топлива детонирует в смеси с воздухом как смесь, состоящая из 80% изооктана и 20% гептана (табл. 4).
Таблица 4. Октановые числа бензина
| Способ получения бензина
| Октановое число
|
| Прямая перегонка Термический крекинг Каталитический крекинг Каталитический риформинг
| 66—80 60—75 80 85—90
|
Сорта автомобильных бензинов обозначают буквой А и цифрой, указывающей его октановое число, например: бензин А-72, А-91, А-95. Сорта авиационного бензина обозначают буквой Б, например: Б-95, Б-100.
Промышленной переработкой каменных углей, называемой коксованием, занимаются коксохимические предприятия. Основными продуктами являются кокс, каменноугольная смола и коксовый газ. Дальнейшей переработкой каменноугольной смолы получают ценнейшие органические продукты: бензол, толуол, нафталин и др.
На первом этапе реализации Энергетической программы России первостепенное значение придается форсированному развитию газовой промышленности, имеющей достаточно надежную сырьевую базу, прежде всего в районах Западной Сибири.
Прирост производства электроэнергии будет происходить в основном за счет ядерного горючего, гидроэнергии и использования углей в восточных районах страны (Канско-Ачинский территориально-производственный комплекс). При этом предполагается, что атомная энергетика будет развиваться опережающими темпами, а использование традиционных топливно-энергетических ресурсов будет улучшено за счет сокращения потребления нефтепродуктов в качестве топлива.
Одним из основных направлений социально-экономического развития является увеличение масштабов использования возобновляемых источников энергии, включая энергию Солнца, ветра, воды, теплоту глубинных слоев Земли, особенно в отдаленных районах с дефицитом органических топливно-энергетических ресурсов.
3. Взаимоконтроль
С оставить тест по изученной теме
оставить тест по изученной теме
П римерный графический тест (да нет )
римерный графический тест (да нет )
1.Химическая промышленность — самая энергоемкая отрасль народного хозяйства.(да)
2.Основным источником энергии для осуществления химико-технологического процесса является электрическая энергия и внутренняя энергия. (да)
3.Внутренняя энергия используется для разнообразных электрохимических процессов. (нет)
4. Топливо — это материал, служащий источником энергии. (да)
5.В горючих веществах основной составной частью является фосфор. (нет)
6. Основным принципом топливной энергетики нашей страны является максимальное и комплексное энерготехнологическое использование топливных ресурсов. (да)
7. Теплота, выделяющаяся при химических превращениях в реакторе, используется для нагревания исходных продуктов. (да)
8. Природное газообразное топливо — природный газ содержит около 95% бутана. (нет)
9. Единственное жидкое природное топливо — нефть. (да)
10. Промышленной переработкой каменных углей, называемой коксованием. (да)
11. Одним из основных направлений социально-экономического развития является увеличение масштабов использования возобновляемых источников энергии. (да)










 1 2 3 4 5 6 7 8 9 10 11
1 2 3 4 5 6 7 8 9 10 11
4.Итоги занятия
Д/з записи в тетрадях
Урок 4.
Тема: Материалы в химической промышленности.
Цель: - изучить выбор конструкционных материалов, классификацию материалов по состав; что такое порошковая металлургия, авиационная и космическая промышленность;
- развивать умение логически излагать свои мысли, сравнивать, анализировать и делать выводы по изученной теме, творческие способности у учащихся.
Ход урока:
1. Начало занятия. Сообщения задач
2.Предъявление нового материала.
Лекция-беседа
Чтобы осуществить любой химико-технологический процесс, необходимо располагать соответствующей аппаратурой. Но тогда возникает вопрос: из каких материалов следует делать эту аппаратуру, чтобы она была способна противостоять разнообразным агрессивным воздействиям, в том числе химическим, механическим, термическим, электрическим, а в ряде случаев также радиационным и биологическим?
Выбор конструкционных материалов осложняется, когда перечисленные воздействия сопутствуют друг другу. Кроме того, в последнее время требования к материалам, используемым в химической технологии, повысились по двум причинам. Во-первых, значительно шире стали применять экстремальные воздействия, такие, как сверхвысокие и сверхнизкие температуры и давления, ударные и взрывные волны, ионизирующие излучения, биологические ферменты. Во-вторых, переход к аппаратам большой единичной мощности по производству основных химических продуктов создает исключительно сложные проблемы в изготовлении, транспортировке, монтаже и эксплуатации подобных установок. Например, на современном химическом предприятии можно видеть контактные аппараты для производства серной кислоты диаметром 5 м, содержащие до 5000 различных труб, реакторы синтеза аммиака и ректификационные колонны высотой более 60 м.
Конструкционные материалы классифицируют по различным признакам, например по составу, структуре, свойствам и областям применения. При классификации материалов по составу можно условно выделить три большие группы — металлические, неметаллические и композиционные материалы.
Металлические материалы обладают сочетанием механических свойств, таких, как прочность, вязкость, пластичность, упругость и твердость, с технологическими — возможностью использования приемов ковки, сварки, обработки режущими инструментами. Они являются незаменимыми не только для построения химических реакторов самой разнообразной формы и размеров, но и в различных областях промышленности. Так, за последние 20 лет мировое производство железа увеличилось примерно в 2,7 раза, меди — в 2,3, алюминия — в 4,7, никеля — в 4, цинка — в 2, титана — в 17 раз.
Чистые металлы сравнительно редко выступают в роли материалов. К их числу относятся алюминий (изготовление емкостей, теплообменников, мешалок), медь (днища и трубопроводы тепло-обменных химических аппаратов для жидких криогенных веществ), молибден (нагреватели и высокотемпературные печи), никель (емкости и колонны для работы в химически агрессивных средах), платиновые металлы (химическая посуда, аноды, катализаторы) и некоторые другие.
Значительно чаще применяют металлические сплавы на основе железа (сталь и чугун), алюминия, магния, меди (бронза и латунь), никеля, ниобия, титана, тантала, циркония и других металлов.
Среди металлических материалов исключительное положение занимают сплавы на основе железа. Сплавы железа с содержанием углерода до 2% принято называть сталью, а свыше 2% — чугуном. Используемые в настоящее время в промышленности стали обычно делят на углеродистые и легированные. Создание новых и интенсификация существующих промышленных процессов заставляет все больше использовать легированные стали, которые обладают повышенной коррозионной стойкостью. Массовая доля средне- и высоколегированных сталей в настоящее время составляет почти 20% от общего количества производимых промышленностью черных металлов. Для легирования используют такие металлы, как никель,хром, молибден, вольфрам, ванадий, кобальт, марганец, медь, титан, алюминий.
Для улучшения качества металлических материалов исключительно важное значение приобрела порошковая металлургия, включающая процессы производства металлических порошков и спеченных из них изделий.
В современной порошковой металлургии можно выделить два основных направления:
1) создание материалов и изделий с такими характеристиками (состав, структура, свойства, которые в настоящее время невозможно достичь известными методами плавки;
2) изготовление традиционных материалов и изделий при более выгодных технико-экономических показателях производства. Обработкой металлических порошков удается достичь важных для практических целей свойств материалов. Например, вольфрам, получаемый в инертной атмосфере в вольтовой дуге, хрупок. Прессованием порошка вольфрама и последующим спеканием изделий в атмосфере водорода изготавливают прочные металлические бруски, которые можно ковать, катать из них листы и штамповать.
Неметаллические материалы принято разделять на две группы — органические и неорганические.
Среди неметаллических органических материалов можно выделить природные и синтетические.
К важнейшим синтетическим полимерным материалам относят пластмассы, эластомеры, химические волокна и полимерные покрытия. В отличие от металлических материалов они имеют высокую устойчивость в агрессивных средах, низкую плотность, высокую стойкость к истиранию, хорошие диэлектрические и теплоизоляционные свойства. Из них несложно изготовить детали и аппараты сложной конструкции. Недостатком многих полимерных материалов является их склонность к старению и невысокая термическая стабильность (до 250 °С). Наиболее известны материалы на основе фенолформальдегидных смол , поливинилхлорида, полиэтиленов и фторопластов.
Среди других полимерных материалов следует отметить каучуки и различные материалы на их основе, такие, как бутил-каучук, силиконовые и фторкаучуки и т. д.
Неметаллические органические материалы составляют лишь небольшую долю используемых в современной технике и промышленности материалов. Их номенклатура насчитывает десятки тысяч названий и быстро увеличивается. Состав и технологические условия получения многих из них запатентованы и представляют большую ценность.
Группа неметаллических неорганических материалов включает керамику, фарфор, стекло, силикатные цементы и бетоны, графит и
многое другое. Их можно также разделить на две группы — природные и искусственные. К первым относятся различные горные породы — незаменимый конструкционный материал для изготовления крупногабаритных сооружений.
Искусственные материалы неорганического происхождения весьма разнообразны и широко используются благодаря кислотостойкости в виде самостоятельных конструкционных материалов или для футеровки различных аппаратов. Наиболее распространены различные виды искусственных силикатных материалов, получаемых плавлением: стекло (с. 189), кварц, ситаллы, эмали, цементы (с. 189).
Особое место среди неметаллических неорганических материалов занимает керамика. Керамическими материалами называют любые поликристаллические материалы, получаемые спеканием неметаллических порошков природного или искусственного происхождения. Перспективность керамики как материала будущего обусловлена его многофункциональностью, доступностью сырья, относительно низкими энергетическими затратами при получении, большой безопасностью и экологическими преимуществами керамического производства.
Композиционные материалы (композиты) состоят из пластичной основы (матрицы) и наполнителя — включений специальных компонентов. Они очень многообразны. Условно можно выделить керамика-металлические материалы (керметы), наполненные органические полимеры (норпласты), газонаполненные материалы (пены).
В качестве основы (матрицы) используются металлы и сплавы, полимеры, керамика. Они обеспечивают связь между составляющими компонентами, прочность и пластичность под действием нагрузок. Значительно разнообразнее применяемые наполнители, особенно для композитов на основе пластмасс, от которых зависит прочность и жесткость композитов. Из наполнителей следует выделить металлические и углеродные волокна, дисперсные тугоплавкие металлы с размером частиц от 0,01 до 0,06 мкм, нитевидные кристаллы карбида и нитрида кремния.
Композиты с полимерными матрицами получают более широкое распространение, чем на основе металлов или керамики.
Пока еще основными потребителями композитов являются авиационная и космическая промышленность. Их использование не только позволяет получать высокоэкономичные и надежные конструкции, но и дает возможность реализовать перспективные аэродинамические схемы, например истребитель с крылом обратной стреловидности. По многим главным физико-химическим свойствам — прочности, ударной вязкости, усталостной прочности и др.— композиты выигрывают у традиционных материалов в 5 раз, а иногда и более.
Потребности общества в новых материалах непрерывно растут, что обусловлено следующими причинами:
1) развитие новых научно-технических направлений (робототехники, информатики, гибких химических производств), требующих принципиально новых материалов со специфическими функциями;
2) повышение стоимости традиционного сырья (в том числе для производства энергии);
3) значительное усиление требований к охране окружающей среды, что привело к удорожанию традиционного химического передела и замене его в ряде случаев новыми технологическими процессами;
4) развитие технологических процессов с использованием экстремальных воздействий (плазмы, сверхвысоких и сверхнизких давлений и температур, облучений и др.).
Таким образом, новые материалы должны удовлетворять разнообразные потребности общества, а их технология обязана быть экономичной в условиях растущего дефицита сырья и стоимости энергии.
3. Взаимоконтроль
Фронтальный опрос по изученной теме в форме беседы
4.Итоги занятия Д/з записи в тетрадях, подготовить презентации, схемы, таблицы к уроку 5
Урок 5.
Тема: Производство металлов: чугуна, стали, алюминия в промышлен-ности.
Цель: - изучить виды сырья, вспомогательных материалов, основной химический процесс, побочные процессы, особенности технологического процесса, основной продукт, свойства, применение, утилизация побочных продуктов при производстве металлов;
- развивать умение логически излагать свои мысли, сравнивать, анализировать и делать выводы по изученной теме.
Ход урока:
1. Начало занятия. Сообщения задач
2..Предъявление нового материала.
1. Современная химическая промышленность выпускает десятки тысяч продуктов. Все многообразие химико-технологических процессов можно свести к пяти основным группам: механическим, гидродинамическим, тепловым, диффузионным (массообменным) и химическим.
Механические — это процессы дробления, измельчения, агломерации, транспортирования твердых материалов, гранулирования и т. п.
Гидродинамические — это процессы перемещения жидкостей и газов по трубопроводам, перемешивания, псевдоожижения, очистка газов от пыли и тумана и др.
Тепловые — это процессы нагревания, охлаждения, конденсации, выпаривания и т. д.
Диффузионные (массообменные) — это процессы сорбции, ректификации, растворения, кристаллизации, сушки и т. д.
Наиболее важна и многообразна группа химических процессов, связанных с изменением химического состава и свойств веществ.
К ним относятся:
процессы горения — сжигание топлива, серы, пирита и других веществ;
пирогенные процессы — коксование углей, крекинг нефти, сухая перегонка дерева;
электрохимические процессы — электролиз растворов и расплавов солей, электроосаждение металлов;
электротермические процессы — получение карбида кальция, электровозгонка фосфора, плавка стали;
процессы восстановления — получение железа и других металлов из руд и химических соединений;
термическая диссоциация — получение извести и глинозема;
обжиг, спекание — высокотемпературный синтез силикатов, получение цемента и керамики;
синтез неорганических соединений — получение кислот, щелочей, металлических сплавов и других неорганических веществ;
гидрирование — синтез аммиака, метанола, гидрогенизация жиров;
основной органический синтез веществ на основе оксида углерода (II), олефинов, ацетилена и других органических соединений;
полимеризация и поликонденсация — получение высокомолекулярных органических соединений и на их основе синтетических каучуков, резин, пластмасс и т. д.
Каждое химическое производство состоит из трех взаимосвязанных стадий:
1) подготовка сырья и подвод реагирующих компонентов в зону реакции;
2) химическое превращение;
3) отвод продуктов и непрореагировавших веществ из зоны реакции, выделение целевого продукта.
2. Практическая часть
Домашняя групповая работа учащихся с дополнительной литературой.
Учащиеся в группах дома составляют опорный конспект по производству чугуна, стали, алюминия в промышленности, используя дополнительную литературу.
Доводят до сведения своих товарищей в виде презентаций, схем, таблиц.
План работы:
сырье,
вспомогательные материалы,
основной химический процесс,
побочные процессы,
особенности технологического процесса,
основной продукт,
свойства,
применение,
утилизация побочных продуктов при производстве металлов.
3.Итоги занятия
Д/з записи в тетрадях, подготовить презентации, схемы, таблицы к уроку 6.
Урок 6.
Тема: Производство неорганических соединений: аммиака, азотной кислоты, стекла в промышленности.
Цель: -изучить виды сырья, вспомогательных материалов, основной химический процесс, побочные процессы, особенности технологического процесса, основной продукт, свойства, применение;
- развивать умение логически излагать свои мысли, анализировать и делать выводы по изученной теме, творческие способности у учащихся;
- формировать навыки работы с дополнительной литературой, компьютером.
Ход урока:
1. Начало занятия. Сообщения задач.
2.Предъявление нового материала.
Практическая часть
Групповая работа учащихся с дополнительной литературой.
Учащиеся составляют опорный конспект по производству аммиака, азотной кислоты, стекла в промышленности, используя дополнительную литературу, таблицы.
Доводят до сведения своих товарищей в виде презентаций, схем, таблиц.
План работы:
сырье,
вспомогательные материалы,
основной химический процесс,
побочные процессы,
особенности технологического процесса,
основной продукт,
свойства,
применение.
3.Итоги занятия
Д/з записи в тетрадях, подготовить презентации, схемы, таблицы к уроку 7.
Урок 7.
Тема: Производство органических соединений: ацетилена, уксусной кислоты, метилового и этилового спирта, целлюлозы в промышленности.
Цель: - изучить виды сырья, вспомогательных материалов, основной химический процесс, побочные процессы, особенности технологического процесса, основной продукт, свойства, применение;
-развивать умение логически излагать свои мысли, анализировать и делать выводы по изученной теме, творческие способности у учащихся;
- формировать навыки работы с дополнительной литературой, компьютером.
Ход урока:
1. Начало занятия. Сообщения задач
2.Предъявление нового материала.
Практическая часть
Групповая работа учащихся с дополнительной литературой.
Учащиеся составляют опорный конспект по производству ацетилена, уксусной кислоты, метилового спирта, целлюлозы в промышленности, используя дополнительную литературу, таблицы.
Доводят до сведения своих товарищей в виде презентаций, схем, таблиц.
План работы:
сырье,
вспомогательные материалы,
основной химический процесс,
побочные процессы,
особенности технологического процесса,
основной продукт,
свойства,
применение.
3.Итоги занятия
Д/з записи в тетрадях, подготовить презентации, схемы, таблицы к уроку 8.
Урок 8.
Тема: Производство высокомолекулярных соединений: полиэтилена, пластмасс, синтетического каучука и резины, химических волокон в промышленности.
Цель: - изучить виды сырья, вспомогательных материалов, основной химический процесс, побочные процессы, особенности технологического процесса, основной продукт, свойства, применение;
- развивать умение логически излагать свои мысли, анализировать и делать выводы по изученной теме, творческие способности у учащихся;
- формировать навыки работы с дополнительной литературой, компьютером.
Ход урока:
1. Начало занятия. Сообщения задач
2.Предъявление нового материала.
Практическая часть
Групповая работа учащихся с дополнительной литературой.
Учащиеся разбиваются на 5 групп и составляют опорный конспект по производству полиэтилена, пластмасс, синтетического каучука и резины, химических волокон в промышленности, используя дополнительную литературу, таблицы.
Доводят до сведения своих товарищей в виде презентаций, схем, таблиц.
План работы:
сырье,
вспомогательные материалы,
основной химический процесс,
побочные процессы,
особенности технологического процесса,
основной продукт,
свойства,
применение.
3.Итоги занятия
Д/з записи в тетрадях, начать работу над проектом (по желанию учащихся)
Уроки 9-13.
Тема: Основные химические производства Брянской области.
Цель:- изучить на практике особенности технологических процессов производства стали, цемента, силикатного кирпича, стекла, шерстяных и лавсановых тканей;
- развивать умение логически излагать свои мысли, анализировать и делать выводы по изученной теме, творческие способности у учащихся.
Ход урока:
1. Начало занятия. Сообщения задач
2.Предъявление нового материала.
Организация экскурсий для учащихся на предприятия Брянской области.
3. Итоги занятий
Д/з Учащиеся оформляют дневник по химической технологии по теме: «Основные химические производства Брянской области». (см. Приложение №1)
Приложение №1.
Дятьковский хрустальный завод
Основан в 1790г Мальцевым.
Состав простого стекла: песок, поташ, сода, сульфаты, мышьк, мел, натриевая селитра, азотнокислый барий.
Состав хрусталя: песок, сода, сурик свинцовый, мышьяк, поташ, калиевая селитра, борная кислота, окись цинка.
Красители: окись кобальта, селена, хрома. Кадмий сернистый и т.д.
Варка стекла:
Это процесс расплавления шихты до однородной смеси.
При варке стекла происходят сложные физико – химические процессы.
При нагревании шихты MgCO3+Na2CO3=MgNa 2(CO3)2 (t=2500C)
CaCO3+ Na2CO3= CaNa 2(CO3)2 (t=4000C)
Они вступают в реакцию: MgNa 2(CO3)2+2SiO2= MgSiO3+ Na2SiO3+2CO2
CaNa 2(CO3)2+2SiO2= CaSiO3+ Na2SiO3+2CO2
При температуре 750 -9000С возникает жидкая фаза и поэтому реакция образования силикатов ускоряется. Небольшая добавка к шихте плавикового шпата СaF2 ускоряет процесс варки стекла.
При дальнейшем нагревании стекломассы до 15000С вязкость ее уменьшается, вследствие диффузии выравнивания состава (гомогенизация) и удаление пузырьков газа (осветление).
Варят стекло в ванных печах непрерывного действия. Печи регенеративные, шихту засыпают периодически в зону варки (температура 14000С). Стекломасса самотеком идет в зону осветления. Для увеличения вязкости попадает в зону с температурой 12000С, оттуда ее забирают для выработки изделий.
Выдувание изделий производится ручным способом, затем обрабатываются края изделия, наносится гравировка (алмазная грань), может применяться роспись
Бежицкий камвольный комбинат
Построен в 1953г., в 1979г стал объединением, сейчас АО «Брянсктекстиль». Выпускает шерстяные, полушерстяные, лавсановые ткани.
Имеет несколько цехов:
Сырьевой или подготовительный
Сырье – белая овечья шерсть вылеживается 1 неделю в тюках, затем идет на тряпально – рыхлительную машину, где происходит разрыхление и замасливание эмульсией, чтобы снять статистическое напряжение.
Затем сырье идет на тряпальные машины, содержащие вертикальные и горизонтальные решетки (разрыхлители). Затем – на чесальную машину, где шерсть расчесывают и формируют в ленту и клубок. Первый рабочий орган чесальной машины покрыт пальчатой фурнитурой, а второй – игольчатой.
Чесальная машина – сырье загружают в самовес, расчесанная шерсть идет на съемный гребень, с помощью вьюнка наматывается в бабины.
На комбинате производят ватин из отходов производства.
Гребнечесальная машина – вычесывает из ленты короткие волокна, а длинные – формируются в таз.
Ленточные машины –происходит чесание, смешивание шерсти и полушерсти.
Окрашивание волокна
Красят три вида волокон – шерсть, полушерсть и лавсан.Волокно находится в Бабине. Для шерсти и полушерсти характерны химические процессы крашения, для лавсана – механические.
Для окрашивания шерсти используют следующие виды красителей: кислотные, хромовые и активные.
Шерсть загружают в аппараты для окрашивания. В аппарате имеется бак, в который заранее загружают краситель( температура составляет 400С, каждый краситель имеет свою среду и особые вещества – выравниватели, замедлители). Затее производят перекачивание красителя в камеру окрашивания.
При окрашивании лавсана используют температуру 1300С, р=300 атм.
Окрашенную шерсть помещают в гладильно –сушильную машину, затем – в промывательный бак. Сушат, чешут с замасливанием и потом формируют в ленту.
3. Ровничный цех
Функция ровничных машин: вытягивание лент в горизонтальные.
4. Прядильный цех
В этом цеху нити делают ровными. Ленточный аппарат перекручивает нить из початков на бабину, а с бабин на катушку и далее поставляют на тканевый цех.
5.Тканевый цех
583 станка. Путем переплетения основной нити (вдоль) и уточной нити (поперек) получают ткань.
6.Товарно – браковочный цех
Имеется три поточные машины, всю полученную ткань сшивают, проверяют на брак. Если на ткани есть пятно, то ее направляют на замывочный стол.
Цех отделочного производства
Грубой ткани придают товарный вид. Для этого промывают в растворе сода + мыло + щелочь + вода при температуре 1000С, потом ткань сушат. Ткань поступает на мерительные машины, где ее отмеряют, пришивают этикетку с названием, артикулом.
Бежицкий сталелитейный завод
Построен в 1935г. Первая плавка стали – в 1936г. В 1946г. Завод восстановили после войны и расширили производство. Имеются цеха крупного и среднего литья.
Вспомогательные цеха
Автотранспортный
Модельный
Железнодорожный
На заводе производят низкопородистую и легированную сталь (содержание С до 0,3%).
Сталь получают 2 способами:
В мартеновских печах.
В электропечах.
Сырье: металлолом со всей территории России, ферросплавы ( марганец, хром, стронций).
Мартеновский способ
Имеет 2 печи в рабочем состоянии.
Печь – чаша, выложенная огнеупорным кирпичом, отапливается мазутом, который распыляется при помощи форсунок под р=5 атм.Температура в печи 1600-17000С. Размеры печи: длина равна 10м, ширина равна 3,5 м.
Печь может вместить 60т.
Технологический процесс: в шихту загружают металлолом + добавки, которые помещают в печь, плавка составляет 7-8 часов при повышенной температуре. Вредные элементы фосфор и сера переходят в шлак, всплывают на поверхности и помещают в специальные емкости, стоящие около печи. Плавку разливают на два ковша по 30т, которые заранее нагревают природным газом. Шихта должна быть хорошо прокалена, так как может произойти взрыв.
Благодаря выделению пузырьков СО, металл как бы кипит.
Электропечи
Имеется 7 электропечей. Печь – чаша, выложенная огнеупорным кирпичом, а свод – из хромо – магнезитного кирпича. Загрузка сырья осуществляется сверху. Имеется три электрода диаметром 20 см, а между ними и шихтой возникает электродная дуга (температура составляет более 40000С) Это позволяет более чисто удалить фосфор и серу и выплавлять тугоплавкие ферросплавы за короткий срок (3 ч.) Емкость печи составляет 3 т. Из этой стали изготавливают более мелкие детали.
Литейный цех
Сталь разливают в формы, которые изготавливают в формовочном цехе
Технологический процесс: формовка – заливка – выбивка – разделки – термообработка – обрезка – формализация ( 9300С выдержки) – охлаждают на воздухе – закалка – обрезка металла об металл.
При заливке делают пробные бруски, по ним определяют химический состав, механические свойства стали.
Перспективы развития
Разрабатываются схемы измельчения гранул шлака, которые продаются для строительства дорог.
Разрабатываются схемы полного удаления металла из шлака.
Более широкая автоматизация производства и механизация труда сталеваров.
Мальцовский портландцемент
Цементный завод построен в 1899г. Завод выпускает 3 млн. т. цемента в год.Цемент покупают многие города России.
Сырье: мел и глина. Сырье добывают в карьерах, ме6л на глубине 13м, т.к. на глубине 7м. –пустая порода.
Цементный завод имеет следующие цеха:
С начало добывают мел экскаватором, потом он поступает в сырьевой цех на переработку. В 1 отделе получают глиняный шлак, во 2 отделе – глиняно – меловой шлак, в 3 отделе – тонко мелят смесь.
Вначале были построены вращающиеся и шахтные печи.
Применяют мокрый способ производства. Сырье имеет большую влажность.
Технология производства цемента
Глина – экскаватор – дунканы – грузовой цех – приемное устройство – транспортер – мельница (сюда добавляют воду) – глиняный шлам – гидротранспортер –
глиняно-меловой шлам (сюда уже добавляют мел) – бассейн (механическое и воздушное перемешивание) – бассейн готового шлама с крановыми мешалками – вращающаяся печь на обжиг.
Вращающаяся печь
В подготовительной зоне происходит удаление воды на 40%.
В зоне дегидратации происходит удаление воды из криталлогидратов.
В зоне кальцинирования происходит разложение карбоната кальция.
Зона экзотермической реакции.
Зона смешения (получается 4-х компонентный клинкер).
Аллит 3 CaO x SiO2 (основной)
Белит 2CaO x SiO2 (основной)
3-х кальцинированный алюминат 3 CaO x Al2O3
4-х кальцинированный алюмоферрит 4 CaO x Al2O3х Fe2O3
Используется 200кг топлива за смену, температура 15000С.
6. Зона охлаждения до температуры 10000С
7. Холодильник
8. Транспортер
9. На склад
10. В цементную мельницу
При помощи клинкера обязательно добавляют гипс для замедления сроков схватывания. Количество добавок (гранул, доменного шлака ) зависит от вида цемента.
Виды цемента:
Вращающиеся печи работают по принципу противотока. Используются электрофильтры, пыльные камеры, циклоны, рукавные фильтры.
Силикатный завод
Основное сырье и его запасы:
Добыча его производится в пойме о. Орлик.
Технологическая схема процесса:
Добыча песка.
Отстаивание песка.
Просеивание и поступление на хранение в бункеры.
Совместный помол песка и извести в мельницах.
Дозировка.
первичное перемешивание в мешалках.
Вторичное перемешивание и увлажнение.
Доувлажнение.
Гашение и прессование.
Стадии производства:
Песок после его добычи отстаивают два месяца.
Шагающим экскаватором загружают в бункера и он поступает на пескосвал.
На пескосвале имеется решетка для удаления крупных примесей (песок поступает на сито, где происходит просеивание песка).
Песок и известь по бетонной галерее поступает в 3 бункера.
Совместный помол песка и извести происходит в 2-х камерных мельницах. Данная смесь идет в 3-й вяжущий бункер.
Поступают в мешалки, где происходит премешивание по сухому способу.
Поступают в мешалки второго перемешивания, где происходит увлажнение смеси известковым молочком.
Поступают в силоса и на доувлажнение.
Прессование.
Устройство и принцип работы 2-х камерных мельниц:
В камерах находятся шары диаметром 130мм. Смесь проходит через мельницы 20 минут.
Основные технолого – экономические показатели
Производительность завода -13т в час.
Вес кирпича - 5,2 кг.
Завод выпускает полнотелый утолщенный рядовой кирпич.
Уроки 14-15.
Тема: Решение экспериментальных задач с производственным содержанием.
Цель: формировать навыки решения задач по химии с производственным содержанием на распознавание веществ: сырья, продуктов производств; очистку сырья и продуктов химических производств и определение примесей в них; получение веществ в промышленности и управление химическими реакциями.
Ход урока:
1. Начало занятия. Сообщения задач
2.Решение задач
Примерные экспериментальные задачи с производственным содержанием
-- Один из промышленных способов получения хлорида меди (II) заключается в проведении реакции между хлоридом бария и медным купоросом. Покажите на опыте, можно ли заменить хлорид бария более дешевой поваренной солью. Объясните.
-- Покажите на опыте, можно ли хранить на воздухе штукатурный раствор. Объясните наблюдаемые явления.
-- Сода является важнейшим химическим продуктом. В промышленности ее получают аммиачным способом. Получите соду аммиачным способом. Какие вещества, получающиеся в результате этих реакций как побочные продукты, можно использовать в качестве исходных для получения соды по этому же способу.
-- В двух ящиках находятся удобрения: в одном – каинит, в другом – хлорид калия. Определить эти вещества.
-- Определить, содержит ли известняк примесь песка.
3.Итоги занятий Д/з
-- решить задачу в тетради
В ряде химических производств в качестве побочного продукта образуется сероводород, который используется для получения серной кислоты. Напишите уравнения реакций получения серной кислоты из сероводорода и составьте задачу на нахождения выхода серной кислоты от теоретически возможного из сероводорода.
-- подготовить сообщения по темам
Создание малоотходных и безотходных производств.
Способы обезвреживания газообразных отходов.
Способы обезвреживания сточных вод
Урок 16.
Тема: Охрана окружающей среды.
Цель: - изучить понятие безотходной технологии, создание малоотходных и безотходных производств, способы обезвреживания газообразных отходов, сточных вод;
- развивать умение логически излагать свои мысли, анализировать и делать выводы по изученной теме, творческие способности у учащихся;
- формировать навыки работы с дополнительной литературой.
Ход урока:
1. Начало занятия. Сообщения задач.
2.Предъявление нового материала
Научно-техническая революция и связанный с нею интенсивный рост химического производства вызвали различные негативные изменения в окружающей среде: отравление и загрязнение пресных вод, загрязнение Мирового океана, загрязнение земной атмосферы, нарушение земного покрова Земли, опустошение недр, уничтожение плодородного слоя Земли, называемого почвой, истребление животных и птиц вплоть до полного исчезновения многих биологических видов.
Охрана природы в России является важной государственной задачей, возведенной в закон. По мере роста населения земного шара, расширения промышленности все более возрастает загрязнение окружающей среды. Рост промышленного производства неизбежно ведет к увеличению количества его отходов, которые, к сожалению, просто выбрасываются в окружающую среду, загрязняя водоемы, почву, воздух. Ухудшение качества атмосферного воздуха безусловно связано и с возрастанием потребления нефти и угля. Вода, почва и воздух сейчас настолько загрязнены, что дальнейшее бездействие может обернуться настоящей катастрофой для всего человечества. Поэтому зашита окружающей среды в настоящее время —- одна из актуальных, всеобщих проблем. Решение ее тесным образом связано со следующими главными задачами. Во-первых, с разработкой и внедрением новых, совершенных технологий. Во-вторых, с созданием программ комплексного использования сырьевых ресурсов, включая и безотходные производства. В-третьих, с грамотным и своевременным решением вопроса утилизации вредных отходов и обезвреживания ядовитых веществ, включая радиоактивные отходы.
Комплексное решение этих проблем позволит предотвратить уменьшение содержания кислорода в атмосфере, разрешение озоносферы Земли, загрязнение воздуха, воды и почвы, ухудшение климата нашей планеты.
3.Сообщения учащихся по темам:
Создание малоотходных и безотходных производств.
Способы обезвреживания газообразных отходов.
Способы обезвреживания сточных вод. (см. Приложение №2)
4.Итоги занятия
Д/з подготовиться к заключительному заняти
Приложение №2.
Сообщение по теме:
«Сущность и направления охраны окружающей среды.»
Сложившееся мнение, что основной вред окружающей среде наносят химические производства, статистика отвергает. Например, ежегодно в атмосферу выбрасывается 100 млн. т оксида серы (IV). Более половины этого количества приходится на долю теплоэлектростанций, четвертая часть — на долю цветной металлургии и лишь несколько процентов — на долю черной металлургии и основной химической промышленности. То же самое можно сказать о выбросах оксидов азота и оксида углерода (IV), твердых пылеобразных выбросах и канцерогенных твердых микроэлементах. Химическая промышленность наряду с нефтехимией в действительности ответственна за появление в атмосфере аммиака, сероводорода, хлоридов и фторидов, формальдегида, нафталина, стирола, толуола, метанола, азотной, фосфорной, уксусной и синильной кислот.
Разумеется, говоря о вреде химической промышленности для окружающей среды, следует иметь в виду не только функционирующее химическое производство, но и целевые химические продукты. Например, синтетические полимеры в отличие от природных не разлагаются ферментами, и в этом смысле они биологически неуничтожаемы. То же самое можно сказать о любых синтетических материалах, которые после употребления сжигают, тем самым увеличивая загрязнение воздуха. Учитывая, что доля полимеров быстро растет в ассортименте химической промышленности, проблема их утилизации после использования в виде конкретных изделий становится все более актуальной.
Как же используются отходы химической промышленности? В настоящее время из 780 видов отходов, образующихся в химической промышленности, полностью или частично применяются только 250, а стоимость сырья, теряемого в виде неиспользуемых отходов, оценивается астрономической цифрой — 100 млрд. руб. в год.
Действительный и потенциальный вред, наносимый окружающей среде и человеку быстро развивающимися производствами, которые используют химический передел, вызвал серьезные опасения.
Основные мероприятия по охране окружающей среды:
1) комплексное использование сырья и разработку безотходной технологии;
2) создание систем оборотного и повторного использования воды, включая внедрение на промышленных предприятиях бессточных систем водоиспользования;
3) конструирование высокоэффективных очистных сооружений.
Сообщение по теме:
«Создание малоотходных и безотходных производств.»
Под безотходной технологией понимается такой способ производства, при котором рационально используются все компоненты сырья и энергии в цикле:
|
|

| 
| Потребление
| 
| г
|
|
|

|
|
|
|

|
| Сырьевые ресурсы
| Производство
| Отходы
| Вторичные ресурсы
|
Малоотходная технология является промежуточной при организации безотходного производства.
Под малоотходным производством понимают такое производство (или совокупность производств), в результате функционирования которого вредное воздействие на окружающую среду не превышает санитарного уровня.
Рассмотрим направления создания малоотходных и безотходных производств на примере крупнотоннажного производства аммиака.
При синтезе аммиака бывают следующие выбросы:
1. Жидкие стоки, состоящие из конденсата, продуктов продувки системы охлаждения и промывки растворов.
2. Газовые выбросы, содержащие аммиак, углекислый газ и др.
3. Невосполнимые потери энергии в системах воздушного и водяного охлаждения, которые сами по' себе не оказывают заметного влияния на окружающую среду, но увеличивают тепловые потери.
В замкнутых системах производства аммиака промышленные выбросы уменьшаются. Ранее на стадии синтеза аммиака для предотвращения накопления инертных газов прибегали к продувке и частичному сбросу в атмосферу циркуляционного газа. В настоящее время этот газ после отделения аммиака используют как сырье или топливо на стадиях производства водородсодержащего газа.
Наиболее благоприятные возможности для организации малоотходных и безотходных химических производств существуют в территориально-производственных комплексах.
Как уже отмечалось ранее, отходы химических производств, являющиеся источником загрязнения окружающей среды, значительно уступают в этом смысле энергетике, черной и цветной металлургии, горнодобывающей промышленности и транспорту.
Поэтому перед химией стоит проблема изыскать эффективные методы обезвреживания и использования не только отходов собственно химической промышленности, но и многих промышленных и бытовых отходов. И эта актуальная задача уже решается для всех сфер окружающей среды, включая атмосферу, природные воды и почву.
Характеристикой качества газообразных отходов и промышленных сточных вод является предельно допустимая концентрация (ПДК), определяющая содержание загрязняющих примесей в миллиграммах на 1 м3 воздуха или на 1 л воды, которое не вызывает заболеваний или отклонений в состоянии здоровья работающих на химических предприятиях или живущих в близлежащей местности.
ПДК различают по длительности воздействия на окружающих:
восьмичасовое воздействие на работающих в течение всего рабочего стажа — ПДК рабочей зоны (ПДК ),
среднесуточное и максимально разовое воздействия на окружающих (ПДК и ПДК ) и др.
Капитальные затраты на очистные сооружения в зависимости от природы и концентрации загрязнений составляют от 2 до 60% всех затрат на сооружение объекта.
Методы обезвреживания газовых выбросов и сточных вод чрезвычайно многообразны, и их выбор определяется степенью загрязненности.
Сообщение по теме:
«Способы обезвреживания газообразных отходов.»
| Обезвреживаемый продукт
| Предельно допустимая концентрация (ПДК), мг/м9
| Способ очистки
| Степень очистки, %
|
|
| ПДКр.з | ПДКм.р.
| ПДКс.с. |
|
|
| Азота (IV) оксид
| 9
| 0,035
| 0,085
| Абсорбция 75 — 90%-ной серной кислотой в пенных аппаратах. Каталитическое окисление Адсорбция на угле |
80 95 99
|
| Азотная кислота
| 2
| 0,4
| 0,15
| Центрифугирование
| 90
|
| Апатит
| 6 | -- | -- | Абсорбция в пенных аппаратах | 98,5
|
| Ацетон
| 200
| 0,35
| 0,35
| Каталитическое окис- ление на медно-хромо- вом катализаторе
| 80—100
|
| Бензол
| 5
| 1,5
| 0,1
| Каталитическое окисление | 85—100
|
| Метиловый спирт
| 5
| 1
| 0,5
| Каталитическое окисление
| 100
|
| Серная кислота
| 1
| 0,3
| 0,1
| Центрифугирование
| 95
|
| Сероводород
| 10
| 0,008
| 0,008
| Абсорбция раствором моноэтаноламина
| 99,5
|
| Серы (IV) оксид
| 10
| 5
| 0,05
| Адсорбция гидроксида- ми щелочных металлов
| 80
|
| Углерода (IV) оксид
| 9000
| —
| —
| Абсорбция водой в скрубберах
| 99
|
| Углерода (II) оксид
| 20
| 5
| 3
| Абсорбция медно-аммиачным ацетон-карбонатным раствором Отмывка жидким азотом (вымораживание)
| 99,9
99,9
|
| Сажа
| 3,5
| 0,15
| 0,05
| Фильтрование через бу- мажный фильтр
| 96
|
| Фенол
| 0,3
| 0,01
| 0,003
| Каталитическое окисление
| 100
|
| Формальдегид
| 0,5
| 0,035
| 0,012
| Абсорбция 30%-ным раствором уротропина
| 70
|
| Цемент
| 6
| 0,3
| 0,1
| Улавливание в инерционном пылеуловителе
| 90
|
Сообщение по теме:
«Способы обезвреживания сточных вод.»
| Обезвреживаемый продукт
| Предельно допусти- мая концентра- ция (ПДК), мг/л
| Способ очистки
| Степень очистки, %
|
| Ароматические органи- ческие соединения
|
—
| Адсорбция на угольных фильтрах
|
|
| Ацетон
| 0,1
| Биохимическое окисление
|
|
| Грубодисперсные примеси
| 10—15
| Отстаивание
| 70
|
| Железа (III) гидроксид
| 10
| Фильтрование через слой вспомогательных материалов
|
99
|
| Железа (II) соли
| 0,5
| Хлорирование
| 99
|
| Марганца (II) соли
| 1
| Хлорирование
| 99,9
|
| Масла
| 0,3
| Отстаивание
| 65—95
|
| Минеральные соли (NаС1, К2SО4 и др.)
| 1000
| Сорбция на анионитах
| 99,9
|
| Нефть
| 0?1 | Фильтрование через песок Улавливание в нефтеловушках Биохимическое окисление
| 50—90 99,9
53
|
| Сероводород
|
| Отдувка воздухом из воды
| 80
|
| Фенол
| 0,001
| Экстракция Озонирование Биохимическое окисление
|
|
| Формальдегид
| 0,5
| Экстракция Озонирование Биохимическое окисление
| 100
|
Урок 17.
Тема: Заключительное занятие.
Цель: подвести итоги, обобщить знания учащихся по данному элективному курсу в виде защиты проектов, мини-сочинений «Чем мне был полезен и интересен данный курс», выполнения теста по содержанию курса, оформить дневники по химическим технологиям Брянской области.
Ход урока:
1. Начало занятия. Сообщения задач
2.Обобщение и систематизация знаний учащихся
1.Оформление дневника по химической технологии
2.
Защита реферата.
Защита проектов.
План работы над проектом:
Определение темы.
Подбор материала по теме.
Обработка материала, оформление работы.
Отчет о работе в форме презентации.
Темы проектов:
Использование отходов производства.
Использование веществ на основании их свойств в сельском хозяйстве, промышленности.
Природоохранная деятельность предприятий (на местном материале).
Составление экспериментальных задач на материале экскурсий на химические предприятия.
Список литературы для учителя:
Краузер Б., Фримантл М.Химия. Лабораторный практикум. – М.: Химия, 1995.
Фримантл М. Химия в действии. Ч.1,2.– М.: Мир, 1991.
Третьяков Ю.Д. Химия и современность. – М.: Просвещение, 1985.
Третьяков Ю.Д. Химия. Справочные материалы. – М.: Просвещение, 1988.
Алексинский В.Н. Занимательные опыты по химии.– М.: Просвещение, 1995.
Пиментел Д., Кунрод Дж Возможности химии сегодня и завтра. – М.: Мир, 1992.
7. Габриелян О.С. Настольная книга учителя химии. 8-11 кл. –
М.: Блик плюс, 2000.
8. Брокгауз Ф. А., Ефрон И. А. Энциклопедический
словарь.— С.-П., 2001.
Список литературы для учащихся:
1. Люцис К.Малая энциклопедия по химии..- М.,2001
2. Гржимек Б. Экологические очерки о природе и человеке.- М.:
Прогресс, 1988.
3. Третьяков Ю.Д.. Химия. Справочные материалы.–
М.: Просвещение, 1988.
4. Габриелян О.С. Химия. 9 кл.– М.: Дрофа, 2005.
5. Габриелян О.С., Остроумов И.Г., Карцова А.А. Химия. 10 кл.–
М.: Просвещение , 2003.
6. Ахметов С.Н. Неорганическая химия. 9 кл.– М. ,
Просвещение, 2000.

 Получите свидетельство
Получите свидетельство Вход
Вход

















 .Конструкционные 2.Виноделие, напитки
.Конструкционные 2.Виноделие, напитки





 оставить тест по изученной теме
оставить тест по изученной теме








 Химия в промышленности (0.46 MB)
Химия в промышленности (0.46 MB)
 0
0 1847
1847 135
135 Нравится
0
Нравится
0







