Холодный утренний туман, столб дыма над костром, взвешенные частицы в воде рек и озёр – это дисперсные системы. Они состоят из вещества в мелкораздробленном состоянии – дисперсной фазы и среды, в которой эта фаза распределена и называется дисперсионной средой.
Дисперсные системы бывают газовыми, жидкими и твёрдыми.
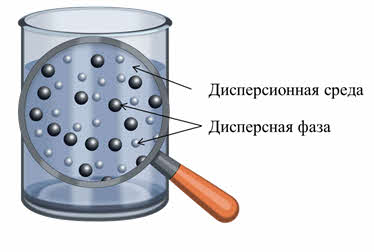
При смешивании одних веществ с водой образуются однородные, или гомогенные системы, а при смешивании других – неоднородные, или гетэрогенные.
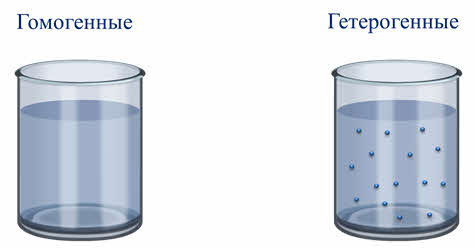
По степени дисперсности, то есть по величине частиц, распределённых в дисперсионной среде, различают грубодисперсные системы, как суспензии и эмульсии и тонкодисперсные системы.
Измеряется размер частиц в нанометрах. Один нанометр равен десять в минус девятой степени метру.
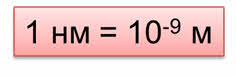
Так частицы в грубодисперсных системах хорошо видны в микроскоп, их средний размер более десяти в шестой степени метра. Например, грубодисперсной системой является молоко.

Оно представляет собой эмульсию капелек жира в жидкости. Грубодисперсные системы неустойчивы и со временем дисперсная фаза отделяется от дисперсионной среды.
В тонко или высокодисперсных системах, которые ещё называют коллоидными системами размер частиц от одного микрометра до одного нанометра.

Классификация дисперсных систем.
Суспензии или взвеси представляют собой находящиеся в жидкой среде мелкие частицы твёрдого вещества. Примером может служить смесь глины с водой. Мутные частицы здесь видны невооружённым глазом. Они легко осаждаются, задерживаются любыми фильтрами, размер этих твёрдых частиц около ста нанометров. То есть в суспензиях дисперсной фазой являются твёрдые вещества.

Какао – также пример суспензии, эта смесь кажется гомогенной, но в конце концов она разделяется. То есть в суспензиях частицы находятся во взвешенном состоянии, и со временем распределяются вниз или вверх, в зависимости от самих частиц. Примером суспензий являются также цементный раствор, бетон и другие.

Эмульсии – это смесь в жидкой среде мелких капелек другой жидкости. Например, смесь масла с водой. В эмульсии мутные отдельные частицы видны невооружённым глазом, они также легко осаждаются, задерживаются обычными фильтрами, размер частиц также около ста нанометров.

Таким образом, эмульсии – это системы, состоящие из двух несмешивающихся жидкостей. Они широко распространены в природе: сырая нефть, млечный сок растений.
Облака, туманы и дым представляют собой аэрозоли. Аэрозоли нашли широкое применение – это топливо в двигателях внутреннего сгорания.
Туман образуется при выпускании в воздух содержимого аэрозольных баллончиков. Дым образуется не только при горении топлива, но и при химических реакциях. Например, при взаимодействии хлороводорода с аммиаком.
Если дисперсионная среда – жидкость, а дисперсная фаза – газ, то образуется система, называемая пеной. Устойчивость пен зависит от прочности плёнок, разделённых пузырьками газа.

Жидкие пены – это мыльная, пивная, квасная пены. При затвердевании плёнок образуются устойчивые твёрдые пены – пемза, вулканический туф. К твёрдым пенам относится также пенопласт, поролон, микропористая резина. Банная губка является дисперсной системой с двумя взаимопроникающими дисперсионными средами. В виде дисперсных систем с жидкой дисперсной фазой и твёрдой дисперсионной средой выпускают некоторые лекарственные средства. Устойчивость пены применяется и при тушении пожаров.
По размерам частиц промежуточное положение между взвесями и истинными растворами занимают коллоидные растворы – золи.

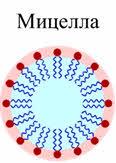
Коллоидные частицы очень малы, но могут состоять из сотен и тысяч молекул. Коллоидные частицы называются мицэллами.
Так, коллоидный раствор йодида серебра можно получить при взаимодействии разбавленных растворов нитрата серебра и йодида калия.
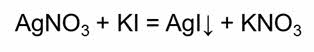

Нерастворимые молекулы йодида серебра образуют ядро коллоидной частицы.
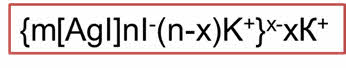
Само вещество ядра нерастворимо в дисперсионной среде и состоит из нейтральных молекул или атомов. В нашем примере ядро коллоидной системы – микрокристаллик йодида серебра, который состоит из множества молекул. Это ядро адсорбирует на своей поверхности ионы, которые находятся в растворе (это ионы серебра и ионы йода). Ядро с таким адсорбционным слоем называется гранулой. Оставшаяся часть ионов образует диффузный слой ионов. Ядро с адсорбционным и диффузным слоями представляет собой мицэллу.
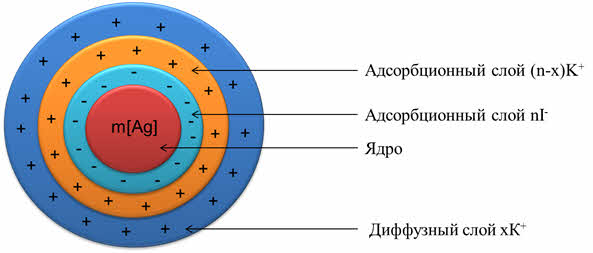
Коллоидные растворы – это смеси, в которых прозрачные отдельные частицы обнаруживаются только при помощи ультрамикроскопа. Эти частицы с трудом осаждаются в течение продолжительного времени и задерживаются только ультрафильтрами. Размер этих частиц приблизительно от одного до ста нанометров.
То есть, коллоиды – разновидность гомогенных систем. В этих смесях частицы настолько малы, что находятся во взвешенном состоянии. Примерами коллоидов является яичный белок, плазма крови.

Укрупнение коллоидных частиц называется коагуляцией. Некоторые коллоидные растворы при коагуляции образуют гели, или студни. Примерами студней являются желе, мармелад, мясной студень, простокваша.
Истинные растворы – это смеси, где прозрачные отдельные частицы нельзя обнаружить даже при помощи ультрамикроскопа, они не осаждаются и фильтрами не задерживаются. Размер этих частиц меньше одного нанометра.
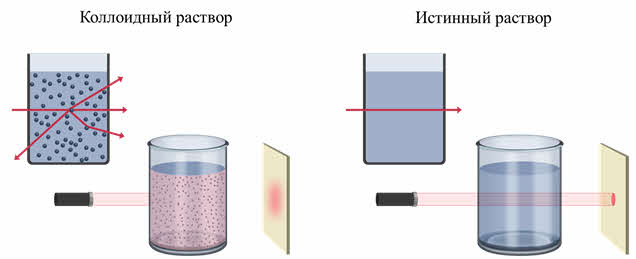
Сходство коллоидов и истинных растворов заключается в их прозрачности. При этом, пропущенный луч света через коллоид даёт светящийся конус, а истинный раствор не даёт. То есть, если на осветлённый коллоидный раствор посмотреть сбоку, то путь луча будет виден, как светлая дорожка, которая образуется в результате рассеивания света частицами. А в истинном растворе луч света не виден, так как молекулы слишком малы и не рассеивают свет.
Вещества в коллоидном состоянии являются основой жизни на земле. Это протоплазма любой живой клетки, представляющая собой сложную коллоидную систему. Мышечная ткань, хрящи, клетки тканей растений, эритроциты – разновидности студней. Коллоиды почвы играют значительную роль в корневом питании растений.
Вещества в коллоидном состоянии принимают участие в образовании многих минералов: агата, малахита, мрамора.

Некоторые драгоценные камни – жемчуг – представляют собой коллоидную систему, где дисперсионной средой является твёрдый карбонат кальция, а дисперсной фазой – капельки воды. Окраска драгоценных камней: рубина, изумруда, сапфира зависит от содержания в них небольших золей металлов.

Ещё в глубокой древности человек использовал коллоидные процессы: египтяне забивали в щели скал деревянные клинья, поливали их водой, древесина набухала, создавалось огромное давление, которое приводило к разрушению твёрдой породы.
Процессы коагуляции коллоидов применяют для очистки природной воды. Так, в бассейн-отстойник добавляют электролит, и коллоиды осаждаются в виде хлопьев, а они задерживаются песчаными фильтрами.
Мели и наносы в устьях образуются под действием воды, которая приводит к коагуляции частиц, находящихся в реке.
С коллоидными процессами связаны важнейшие отрасли промышленности: производство искусственных волокон, различных клеящих веществ, синтетического каучука. Коллоидные растворы используются в мыловарении, бумажной промышленности, в фармацевтическом производстве.
Адсорбционные свойства коллоидных частиц положены в основу процесса обогащения руд. Важнейшие пищевые продукты: простокваша, кефир, творог, желе, джем – это коллоидные системы – студни. Студни обладают некоторыми свойствами твёрдого тела: они легко режутся, сохраняют первоначальную форму.
Бумага, сплавы металлов, цветные стёкла, пластмассы, натуральные и искусственные ткани содержат вещества в коллоидном состоянии.

 Получите свидетельство
Получите свидетельство Вход
Вход




 11165
11165

