
МОУ«Средняя общеобразовательная школа № 36»
Тема : Алюминий и его соединения
(урок изучения нового материала)
9, 11 кл.
.
«Этому металлу – принадлежит великое будущее»
(Н.Г.Чернышевский)

Цель урока
- Повторить и систематизировать знания учащихся о металлах III группы главной подгруппы.
- Уметь давать характеристику металлам III группы главной подгруппы исходя из положения в периодической системе и строение атома.
- Уметь доказывать химические свойства алюминия и его соединениям. Записывать уравнения реакций в молекулярном, ионном, окислительно-восстановительном виде.
- Уметь пользоваться приемами сравнения, обобщения, делать выводы.

Оборудование к уроку
Образцы металла алюминия, природных соединений и сплавов, стеклянная посуда (чашка Петри, колба), вода, соли алюминия, коллекция веществ из алюминия, мультимедийный проектор, экран, компьютер, учебник.

План урока
- Положение металла в периодической системе Д.И.Менделеева.
- Строение атома металла.
- Физические свойства металла.
- Химические свойства металла.
- Получение металла.
- Применение металла и его соединений.

Ход урока
1.Организационный момент (психологический настрой) - 2 мин .
2. Проверка домашнего задания - 5 мин.
3. Вступительное слово учителя - 1 мин.
4. Повторение и обобщение темы - 32 мин.
6. Подведение итогов урока - 2 мин.
7. Задание на дом (дифференцированное ) - 3 мин.

Бор первый в группе третьей,
Но алюминию букеты все несут.
Он плод труда эпохи многолетней
Его теперь и режут и куют.

Из истории открытия Al
Открыт в 1825 г. Хансом Кристаном Эрстедом (Копенгаген, Дания).От лат. alumen – квасцы.
В период открытия алюминия - металл был дороже золота. Англичане хотели почтить богатым подарком великого русского химика Д.И Менделеева, подарили ему химические весы, в которых одна чашка была изготовлена из золота, другая - из алюминия. Чашка из алюминия стала дороже золотой. Полученное «серебро из глины» заинтересовало не только учёных, но и промышленников и даже императора Франции.

Строение атомов Ме III группы главной подгруппы
+5 B )) … 2 s 2 2 p 1
2 3
+13 Al )) )… 3 s 2 3 p 1
2 8 3
+ 31 Ga )) ))… 4 s 2 4 p 1
2 8 8 3
+ 49 In ))))) … 5 s 2 5 p 1
2 8 18 8 3
+ 81 Tl )))))) … 6 s 2 6 p 1
2 8 18 18 8 3
… ns 2 np 1
Al - амфотерный элемент
Изменение свойств металлов.
Учитель : Как и почему изменяется химическая активность металлов с возрастанием порядкового номера?
Примерные ответы учащихся :
- Радиус атома увеличивается.
- Увеличиваются восстановительные свойства (способность отдавать электроны).

Нахождение в природе Al
Al занимает 3-е место по распространению в земной коре после кислорода и кремния. Al самый распространенный Ме в природе. Соединения Al были известны очень рано: история глин начинается
с доисторических времен. Al входит в состав силикатов(шпаты, слюда), а также глин. Из соединений Al наибольшее значение имеет минерал Al 2 O 3 -(глинозем) корунд, синий - сапфир, фиолетовый - аметист, красный - рубин, непрозрачный- наждак. Ортоклаз, нефелин, боксит, криолит.

Нахождение в природе Al

Нахождение в природе Al 2 O 3
Сапфир
(с прим. Ti и Fe )
Аметист
Рубины ( c прим. Cr )
Топаз
Бирюза
Корунд
Физические свойства Al
Al серебристо – белый легкий металл. Высокие качества Al : электропроводность и теплопроводность, пластичность, легкость, стойкость по отношению к химическим веществам – одни эти качества обеспечивали бы Al широкую будущность, но «Металлом будущего » он становится главным образом благодаря способности давать сплавы. Al - как проводник электрического тока и тепла занимает 4 - е место после Cu , Ag и Au . С этим связано его применение для изготовления электрических проводов. Особо чистый Al хорошо отражает световые лучи. Им покрыто основное зеркало самого большого в мире советского 6 -ти метрового оптического телескопа.
Д/задание 1) исследуйте, горит ли Al на воздухе и как
легко плавится. Для этого отрежьте полоску фольги,
закрепите пинцетом один конец, а к другому поднесите
зажженную спичку. Опишите, что произойдет?
(вопрос: что мешает Al , после того как он расплавится,
стечь с нагретой полоски в виде капель?)
2 ) поместите по кусочку фольги в воду, в нашатырный спирт, в столовый уксус. Опишите, что произойдет через несколько суток. Опыт закончите, когда в одном
из растворов кусочек фольги превратится в тончайшее «кружево».Сохраните его.
Фильм № 1

Химические свойства Al
Фильм № 2
1. Металл взаимодействуют с простыми веществами: ( при t )
+ Г 2 = МеГ 3 (галогениды) - 7 группа , но 2Al + 3I 2 = 2AlI 3
( кат. H 2 O)
+ O 2 = Ме 2 О 3 ( оксид) - 6 группа
+ S = Ме 2 S 3 (сульфид) - 6 группа
Al + N 2 = Ме N (нитрид) - 5 группа
+ P = МеР ( фосфид ) - 5 группа
+ С = Ме 4 С 3 ( карбид ) - 4 группа
+ Si = Me 4 Si 3 ( силицид ) - 4 группа
+ H 2 = не реагирует
Самостоятельная робота по рядам
Задание: Составьте уравнения химических реакций и расставьте коэффициенты с помощью электронного баланса
1-й ряд 2-й ряд 3-й ряд
Al + Cl 2 = ? Al + O 2 = ? Al + C = ?
Фильм № 3

Проверка самостоятельной работы
Задание: Составьте уравнения химических реакций и расставьте коэффициенты с помощью электронного баланса ( одного на выбор).
1-й ряд 2-й ряд 3-й ряд
Al + Cl 2 = ? Al + O 2 = ? Al + C = ?
2Al 0 + 3Cl 2 0 = 2Al +3 Cl 3 -1 4Al 0 + 3O 2 0 = 2Al 2 +3 O 3 -2 4Al 0 +3C 0 = Al 4 +3 C 3 - 4
2 Al 0 - 3 е =Al +3 (восс.) 4 Al 0 - 3 е =Al +3 (восс.) 4 Al 0 - 3 е =Al +3 (восс.)
3 Cl 2 0 + 2 е=2 Cl -1 (окисл.) 3 O 2 0 + 4е =2O -2 (окисл.) 3 C 0 + 4е =C - 4 (окисл.)

Al + Br 2 = ?
Химические свойства Al
Опыт 1.
Алюминий взаимодействует с бромом
Фильм № 4

Фильм № 5
Опыт 2 . « Зажигание водой » Ложечку порошка I 2 смешали с порошком Al . Смесь пересыпали на асбестовою сетку. Собрали кучкой и прибавили несколько капель H 2 O . В присутствии H 2 O Al энергично соединяется с I 2 . Реакция сопровождается выделением большого количества теплоты, смесь воспламеняется. Выделяются пары I 2 , не успевшего вступить в реакцию. Al + I 2 = ? ( Какую роль здесь выполняет H 2 O )

Химические свойства Al
2. Металл взаимодействует со сложными веществами:
а) с Н 2 О:
у Al необходимо снять оксидную пленку, чтобы произошла реакция с водой 2 Ме + 6H 2 O = 2Me(OH) 3 + 3H 2 ( гидроксид)
б) с кислотами : 2 Ме + 6HCl = 2 Ме Cl 3 + 3H 2
При определенных условиях химические реакции с кислотами окислителями протекают следующим образом:
Ме + HNO 3 (разб.) = соль + NO + H 2 O
(или NH 4 NO 3 )
Ме + HNO 3 (конц.) = соль + N 2 O + H 2 O ( при t)
Ме + H 2 SO 4 (конц.) = соль + SO 2 + H 2 O ( при t)
( или S , H 2 S )
Запомним!
Что Al пассивирует при обычных условиях в конц. HNO 3 и H 2 SO 4 .

Задание «Соколиный глаз »
Данное задание позволит определить у кого острый глаз и пытливый ум. Из уравнений химических реакций вам следует выбрать практически осуществимые и прокомментировать их.
1) 2 Na + 2HCl = 2NaCl + H 2
2) 2Al + 6HCl = 2AlCl 3 + 3H 2
3) Mg + 2HNO 3 = Mg ( NO 3 ) 2 + H 2
4) 4Mg + 10HNO 3 ( конц. ) = 4Mg(NO 3 ) 2 + N 2 O + 5H 2 O
5) 2Al + 6H 2 SO 4 = Al 2 (SO 4 ) 3 + 3SO 2 + 6H 2 O
6) Ca + 2CH 3 COOH = (CH 3 COO) 2 Ca + H 2
![Химические свойства Al в ) амфотерный металл Al взаимодействует со щелочами: 2 Al + 2NaOH+ 6H 2 O = 2Na[ Al (OH) 4 ] + 3H 2 ( NaOH в недостатке ) (тетрагидроксоалюминат натрия) 2 Al + 6NaOH + 6H 2 O = 2Na 3 [ Al ( OH ) 6 ] + 3H 2 (NaOH в избытке ) (гексагидроксоалюминат натрия ) г ) в заимодействие Al с солями: Более активный металл вытесняет менее активный, например: Al + С uCl 2 = Al Cl 3 + Cu Расставьте коэффициенты и напишите полные и сокращенные ионные уравнения](https://fsd.videouroki.net/html/2021/04/19/v_607d58be62386/img18.jpg)
Химические свойства Al
в ) амфотерный металл Al взаимодействует со щелочами:
2 Al + 2NaOH+ 6H 2 O = 2Na[ Al (OH) 4 ] + 3H 2 ( NaOH в недостатке ) (тетрагидроксоалюминат натрия) 2 Al + 6NaOH + 6H 2 O = 2Na 3 [ Al ( OH ) 6 ] + 3H 2 (NaOH в избытке ) (гексагидроксоалюминат натрия )
г ) в заимодействие Al с солями: Более активный металл вытесняет менее активный, например: Al + С uCl 2 = Al Cl 3 + Cu Расставьте коэффициенты и напишите полные и сокращенные ионные уравнения

Проверка самостоятельной работы
Расставьте коэффициенты и напишите полные и сокращенные ионные уравнения: 2 Al + 3С uCl 2 = 2 AlCl 3 + 3 Cu
2 Al 0 + 3 С u 2+ + 6Cl - = 2Al 3+ + 6Cl - + 3Cu 0
2 Al 0 + 3 С u 2+ = 2Al 3+ + 3Cu 0

Химические свойства Al
д ) Взаимодействие Al с оксидами : (алюминотермия)
Вследствие высокой химической активности Al используют в качестве восстановителя в металлургии.
Расставьте коэффициенты с помощью электронного баланса для данного уравнения .
Al + Fe 2 O 3 = Al 2 O 3 + Fe + Q
Фильм № 6

Проверка самостоятельной работы
C оставьте электронный баланс для данного уравнения .
2 Al 0 + Fe 2 +3 O 3 -2 = Al 2 +3 O 3 -2 + 2 Fe 0
Al 0 - 3е = Al +3 1 ( Восстановитель, пр. окисления )
Fe +3 + 3е =Fe 0 1 ( Окислитель, пр. восстановления )

Качественная реакция на ион Al 3 +
Задание 1. Самостоятельно допишите и составьте для данных уравнений реакций полные и сокращенные ионные уравнения .
- Задание 1. Самостоятельно допишите и составьте для данных уравнений реакций полные и сокращенные ионные уравнения .
1. AlCl 3 + ? = Al(OH) 3 + ?
Al(OH) 3 - Белый студенистый осадок, который в
- 1. AlCl 3 + ? = Al(OH) 3 + ? Al(OH) 3 - Белый студенистый осадок, который в
кислотах растворяется.
- кислотах растворяется.
Al(OH) 3 + HCl = ?+?
Al(OH) 3 + KOH= ?+?
- Al(OH) 3 + HCl = ?+? Al(OH) 3 + KOH= ?+?
Al(OH) 3 входит в состав адсорбирующего и обволакивающего средства, применяется при язве желудка, гастритах. Некоторые соли Al 3+ применяются при кожных заболеваниях.
- Al(OH) 3 входит в состав адсорбирующего и обволакивающего средства, применяется при язве желудка, гастритах. Некоторые соли Al 3+ применяются при кожных заболеваниях.
Фильм № 7
![Проверка самостоятельной работы 1. AlCl 3 + 3NaOH = Al(OH) 3 + 3NaCl Al 3 + + 3 Cl - + 3Na + + 3 OH - = Al(OH) 3 + 3Na + + 3 Cl - Al 3+ + 3OH - = Al(OH) 3 Белый студенистый осадок 2. Al(OH) 3 + 3HCl = AlCl 3 + 3H 2 O Al(OH) 3 + 3H + + 3 Cl - = Al 3 + + 3 Cl - + 3H 2 O Al(OH) 3 + 3H + = Al 3 + + 3H 2 O Белый студенистый осадок в кислотах растворяется. 3. Al(OH) 3 + 3 KOH = K 3 [ Al ( OH ) 6 ] Al(OH) 3 + 3K + + 3 OH - = 3K + + [ Al ( OH ) 6 ] - Al(OH) 3 + 3 OH - = [ Al ( OH ) 6 ] - Белый студенистый осадок в щелочах растворяется. Al 3 + + 3 Cl - + 3Na + + 3 OH - = Al(OH) 3 + 3Na + + 3 Cl - Al 3+ + 3OH - = Al(OH) 3 Белый студенистый осадок 2. Al(OH) 3 + 3HCl = AlCl 3 + 3H 2 O Al(OH) 3 + 3H + + 3 Cl - = Al 3 + + 3 Cl - + 3H 2 O Al(OH) 3 + 3H + = Al 3 + + 3H 2 O Белый студенистый осадок в кислотах растворяется. 3. Al(OH) 3 + 3 KOH = K 3 [ Al ( OH ) 6 ] Al(OH) 3 + 3K + + 3 OH - = 3K + + [ Al ( OH ) 6 ] - Al(OH) 3 + 3 OH - = [ Al ( OH ) 6 ] - Белый студенистый осадок в щелочах растворяется.](https://fsd.videouroki.net/html/2021/04/19/v_607d58be62386/img23.jpg)
Проверка самостоятельной работы
1. AlCl 3 + 3NaOH = Al(OH) 3 + 3NaCl
Al 3 + + 3 Cl - + 3Na + + 3 OH - = Al(OH) 3 + 3Na + + 3 Cl -
Al 3+ + 3OH - = Al(OH) 3 Белый студенистый осадок
2. Al(OH) 3 + 3HCl = AlCl 3 + 3H 2 O
Al(OH) 3 + 3H + + 3 Cl - = Al 3 + + 3 Cl - + 3H 2 O
Al(OH) 3 + 3H + = Al 3 + + 3H 2 O Белый студенистый осадок в кислотах растворяется.
3. Al(OH) 3 + 3 KOH = K 3 [ Al ( OH ) 6 ]
Al(OH) 3 + 3K + + 3 OH - = 3K + + [ Al ( OH ) 6 ] -
Al(OH) 3 + 3 OH - = [ Al ( OH ) 6 ] - Белый студенистый осадок в щелочах растворяется.
- Al 3 + + 3 Cl - + 3Na + + 3 OH - = Al(OH) 3 + 3Na + + 3 Cl - Al 3+ + 3OH - = Al(OH) 3 Белый студенистый осадок 2. Al(OH) 3 + 3HCl = AlCl 3 + 3H 2 O Al(OH) 3 + 3H + + 3 Cl - = Al 3 + + 3 Cl - + 3H 2 O Al(OH) 3 + 3H + = Al 3 + + 3H 2 O Белый студенистый осадок в кислотах растворяется. 3. Al(OH) 3 + 3 KOH = K 3 [ Al ( OH ) 6 ] Al(OH) 3 + 3K + + 3 OH - = 3K + + [ Al ( OH ) 6 ] - Al(OH) 3 + 3 OH - = [ Al ( OH ) 6 ] - Белый студенистый осадок в щелочах растворяется.

Получение алюминия
А.Сент-Клер Девиль. Впервые получил алюминий промышленным способом (1855г.).
Немецкий учёный Ф. Велер (1827 г.) получил алюминий при нагревании хлорида алюминия со щелочными металлами калий и натрий.
Al получают электролизом его оксида в расплаве криолита .
Задание. C оставьте электронный баланс для данного уравнения .
Электролиз расплава «глинозема - Al 2 O 3 »:
2Al 2 O 3 = 4Al+3O 2

Проверка самостоятельной работы
Задание. C оставьте электронный баланс для данного уравнения.
А ) Электролиз расплава «глинозема - Al 2 O 3 »: 2Al 2 O 3 = 4Al + 3O 2
2Al 2 +3 O 3 - 2 = 4Al 0 +3O 2 0
( -К:) Al +3 +3е = Al 0 4 ( пр. восстановления)
( + A : ) 2 O - 2 - 4е = O 2 0 3 ( пр.окисления)

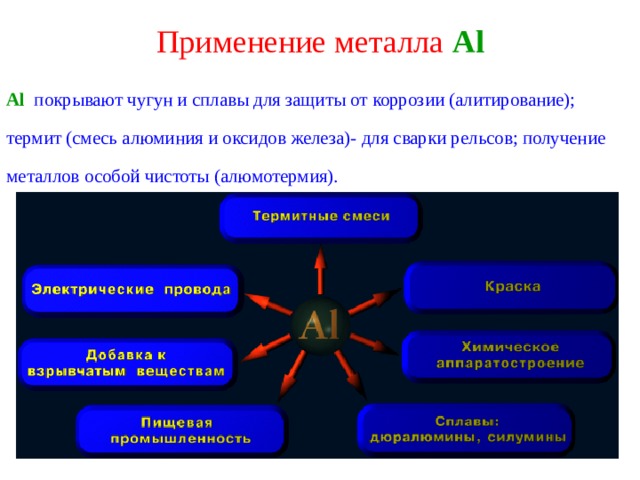
Применение металла Al
Al покрывают чугун и сплавы для защиты от коррозии (алитирование); термит (смесь алюминия и оксидов железа)- для сварки рельсов; получение металлов особой чистоты (алюмотермия).

Применение металла Al и его соединений
Сплавы но основе Al применяются в ракетной технике, в авиа-, авто-, судо- и вагоностроении. В строительстве (алюминиевые кровли, оконные переплеты.)В электротехнике для изготовления кабелей и проводов. В пищевой промышленности и в быту: фольга, посуда. Al «серебряная» краска. В производстве различных предметов воинского снаряжения (котелки, фляги). Al 2 O 3 - в часовых механизмов, ювелирные изделия. KAl(SO 4 ) 2 - в медицине как кровоостанавливающее средство, при дубление кожи. Al 2 (SO 4 ) 3 - очистка водопроводной воды.

Применение алюминия и его соединений

Биологическая роль Al
Несмотря на наличие громадных количеств Al в почвах, растения как правило, содержит мало этого элемента. Еще значительно меньше его содержится в животных организмах. У человека оно составляет лишь десятичные доли процента по массе. Накапливается в организме с ежедневным приемом пищи. Играет роль в развитии болезни Альц – Мейера. Токсическая доза 5 г. Не безобиден Al - он обладает нейротоксическим действием: нарушает двигательную активность, вызывает судороги, снижение памяти, некоторые психические реакции подобие слабоумия. Имеются данные о его мутагенной активности.
![Закрепление темы 1 . Почему Al посуда не разрушается кипяченой водой? 1- й ряд. 2. Целесообразно ли хранить раствор стиральной соды Na 2 CO 3 ,а также продукты молочнокислого брожения в Al посуде? Ответ подтвердите уравнениями реакций. 2-й ряд. 3. При хранении в алюминиевой посуде кислые щи приобретают неприятный «металлический» привкус . С каким химическим процессом это связано? 3-й ряд. Д/задание. Составьте уравнения реакций следующих превращений: Al 2 O 3 AlCl 3 Al(OH) 3 К [Al(OH) 4 ] Al(OH) 3 Al 2 O 3 NaAlO 2 .](https://fsd.videouroki.net/html/2021/04/19/v_607d58be62386/img31.jpg)
Закрепление темы
1 . Почему Al посуда не разрушается кипяченой водой? 1- й ряд.
2. Целесообразно ли хранить раствор стиральной соды Na 2 CO 3 ,а также продукты молочнокислого брожения в Al посуде? Ответ подтвердите уравнениями реакций.
2-й ряд.
3. При хранении в алюминиевой посуде кислые щи приобретают неприятный «металлический» привкус . С каким химическим процессом это связано? 3-й ряд.
Д/задание. Составьте уравнения реакций следующих превращений:
Al 2 O 3 AlCl 3 Al(OH) 3 К [Al(OH) 4 ] Al(OH) 3 Al 2 O 3 NaAlO 2 .
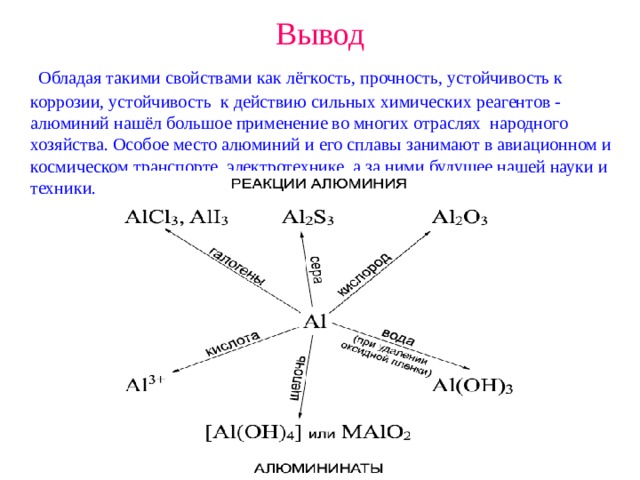
Вывод
Обладая такими свойствами как лёгкость, прочность, устойчивость к коррозии, устойчивость к действию сильных химических реагентов - алюминий нашёл большое применение во многих отраслях народного хозяйства. Особое место алюминий и его сплавы занимают в авиационном и космическом транспорте, электротехнике, а за ними будущее нашей науки и техники.

 Получите свидетельство
Получите свидетельство Вход
Вход












 Тема: «Алюминий, его соединения и применение» (2.11 MB)
Тема: «Алюминий, его соединения и применение» (2.11 MB)
 0
0 178
178 6
6 Нравится
0
Нравится
0


