Лабораторная работа №2
Тема: Методика определения свободной углекислоты
Биохимические процессы разложения органических веществ в природе являются основными поставщиками углекислоты в воду (содержание СО2 в воздухе не велико – всего – 0,03%). Растворяясь в воде СО2 реагирует с водой, образуя гидратированную форму Н2СО3.
При анализе воды определяется суммарная концентрация обеих форм углекислоты.
Этим методом углекислота может быть определена в водах, содержащих её в концентрациях, превышающих 3 мг/дм3. Максимально возможна ошибка определения 0,5 мг/ дм3 СО2.
Свободная углекислота может быть оттитрованна щелочью до бикарбоната:
CO2 + NaOH = NaHCO3
В качестве индикатора используется фенолфталеин.
Средства измерений, вспомогательные устройства, реактивы
Едкий натр, фиксанал;
Едкий натр;
Фенолфталеин;
Спирт этиловый;
Вода дистиллированная или конденсат турбин;
Коническая колба 500 см3;
Мерная колба на 100, 1000 см3;
Бюретка для титрования 25 см 3;
Хлоркальциевая трубка;
Резиновая пробка;
Зажим.
Требования безопасности
К работе в лаборатории допускается персонал, который прошел инструктаж по ТБ, теоретическую подготовку по новой профессии с обучением на рабочем месте 1 месяц, проверке знаний действующих правил техники безопасности и специальных инструкций.
Требования к обслуживающему персоналу
К выполнению анализа допускаются персонал, имеющий среднее, среднетехническое или высшее образование. При отсутствии специального химического образования необходимо пройти теоретическую подготовку по новой профессии с обучением на рабочем месте в течение месяца, изучить правила эксплуатации электрических станций, сдать экзамен и пройти дублирование в течение 2-х недель на рабочем месте. Проверка знаний у инженерно-технических работников производится 1 раз в 3 года, а у лаборантов – ежегодно с записью результатов по проверке знаний в удостоверении.
Подготовка к выполнению измерений
При отборе проб необходимо избежать контакта исследуемой воды с воздухом во избежание попадания СО2 из воздуха.
Температура исследуемой воды – не более 40 оС. Распад воды при отборе пробы – 20-30 л/ч.
1. Титрованный раствор едкого натра 0,1 н концентрации готовят из соответствующего фиксанала; раствор 0,01 н концентрации готовят разбавлением точно в 10 раз 0,1 н раствора.
2. спиртовой 1%-ный раствор фенолфталеина, растворяют 1г индикатора в 100 см3 спирта-ректификата и нейтрализуют приготовленный раствор 0,1 н щёлочью до появления устойчивой розовой окраски.
3. Концентрированный 30%-ный раствор NaOH. Растворяют 30 г NaOH в 70 г дистиллированной воды.
4. Приготовление эталона:
в коническую колбу такого же размера как и на приборе вводят 200 см3 анализируемой воды, добавляют к ней 0,2 см3 0,01%-ного раствора фенолфталеина и 1 см3 30%-ного раствора щелочи, окраски полученного эталона стремится достичь при титровании.
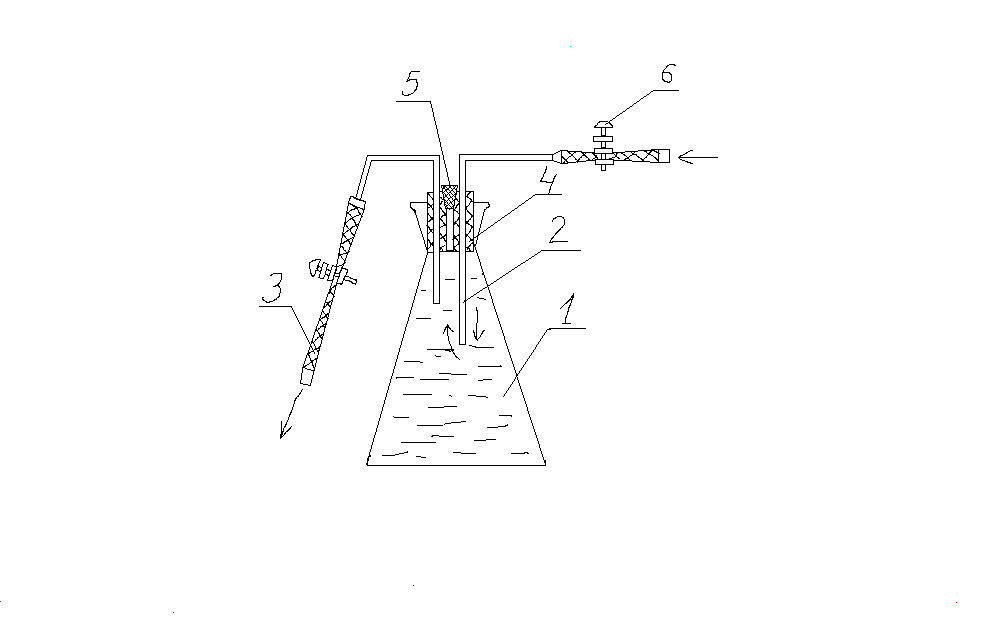
Рисунок 2.1 – Прибор для отбора пробы воды и определения в ней свободной углекислоты:
колба объёмом 300-500 см3;
вход воды;
отвод воды;
большая пробка;
малая пробка;
зажим винтовой.
Выполнение измерений
Собирают прибор по рисунку 2.1.
Присоединив прибор каучуковой трубкой 2 к отборной точке, заполняют колбу 1 анализируемой водой, давая ей выливаться через трубку 3, пока через прибор не пройдет 6-7 объёмов воды. После этого зажимают резиновую трубку 2 зажимом, заменяя её хлоркальциевой трубкой, содержащей известь. Зажим на трубке 2 ослабляют и дают воде из колбы вытекать пока уровень жидкости в ней установится на отметке 200см3. Зажимают вновь трубку 2 и через бюретку вводят 0,2 см3 1%-ного раствора фенолфталеина. Теперь титруют жидкость 0,1 н или 0,01 н раствором щелочи до установления окраски сравнивая цвет жидкости с эталоном.
Вычисление измерений
а х N х K х 1000
(СО2)=____________________________=220 х а x N x K
200
где СО2 – содержание свободной углекислоты в анализируемой воде, мг/ дм3;
а – расход раствора щёлочи на титрование 200 см3 анализируемой воды, см3;
N – нормальность примененного для титрования раствора щелочи;
К – поправочный коэффициент к номинальной нормальности.
При определении содержания углекислоты в Н-катионированной воде из величины «а» вычитают расход раствора щелочи на титрование такого же объема воды с метилоранжем, т. е. вычитают содержание минеральных кислот.

 Получите свидетельство
Получите свидетельство Вход
Вход












 Методика определения свободной углекислоты (51.5 KB)
Методика определения свободной углекислоты (51.5 KB)
 0
0 1243
1243 5
5 Нравится
0
Нравится
0


