Домашние задания.
Использование в учебном процессе подобных домашних заданий по отдельным разделам курса «Физика-10» и «Физика-11» способствует развитию навыков самостоятельной работы, углубленному пониманию сущности физических явлений и процессов, более прочному закреплению пройденного материала и развитию навыков решения расчетных и графических задач. При этом предусматривается работа учащихся с учебником и собственным конспектом (тетрадью) по физике.
Эту систему я уже несколько лет практикую в нашей школе. Задание выдаётся в начале каждого полугодия, а в предметном учебном графике (контрольные работы, рубежный контроль, зачеты) указывается срок (неделя) сдачи.
Все домашние задания выполняются в специальной тетради, которая активно используется при подготовке к экзамену. Качество выполнения позволяет учителю определить степень усвоения учащимися данной темы. После проверки домашнего задания предусматривается его защита учащимися в форме обсуждения полученных результатов и ответов на вопросы. Ответы учащихся учитываются также при выставлении общей оценки по данной теме.
ДОМАШНЕЕ ЗАДАНИЕ №1
«Газовые законы и процессы идеального газа»
Провести анализ отдельных газовых процессов, представленных на диаграммах состояний (в вариантах заданий) участками: 1-2, 2-3 и так далее, то есть:
- дать общую характеристику каждого процесса;
- указать закон, которому подчиняются параметры идеального газа в данном процессе;
-описать изменения основных параметров газа (давление, температура, объем) в ходе процесса;
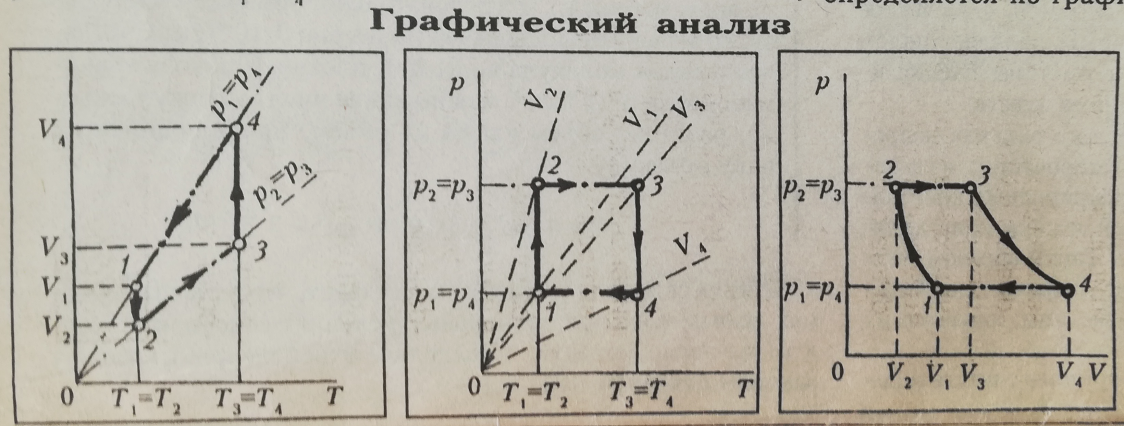
Изобразить процессы в координатах: давление-объем, давление-температура, объем-температура (p – V, p - T, V - T).
Направление процесса на графике указано стрелкой. Кривые на графике в координатах p - Vявляются отрезками гипербол.
Рекомендация: при изображении процессов использовать разные цвета или различный вид линий. Например:
Изотермы – красный цвет (сплошная линия);
Изохоры – зеленый цвет (пунктирная линия);
Изобары – синий цвет (штрих – пунктирная линия).
Примечание.
В вариантах N, N+10, N+20, где N=1-10, представлены одинаковые газовые процессы в разных координатах. (Соотношения выдержаны не везде). Например, вариант 6,16,26.
Пример выполнения домашнего задания.
Вариант 30
Участок 1 – 2
Изометрическое сжатие газа, T = const, T2=T1.
Линия 1 – 2 – изотерма.
Закон Бойля-Мариотта: pV = const.
Объем газа уменьшается: V2V1.
В соответствии с законом Бойля-Мариотта давление газа увеличивается: p2p1.
Участок 2 – 3.
Изобарное нагревание газа: p = const, p3=p2.
Линия 2 – 3 – изобара.
Закон Гей-Люссака: V/T = const.
Температура газа возрастает T3T2.
В соответствии с законом Гей-Люссака, объем газа так же увеличивается: V3V2.
Участок 3 – 4.
Изотермическое расширение газа, T=const, T4=T3.
Линия 3 – 4 – изотерма.
Закон Бойля-Мариотта: pV= const.
Объем газа увеличивается: V4 V3.
В соответствии с законом Бойля-Мариотта давление газа уменьшается: p4p3.
Участок 4 – 1.
Изобарное охлаждение газа, p = const, p1 = p4.
Линия 4 – 1 – изобара.
Закон Гей-Люссака: V/T = const.
Температура газа понижается: T1T4.
В соответствии с законом Гей-Люссака объем газа уменьшается: V1V4.
Примерные вопросы при защите задания.
1. Определить по графикам, во сколько раз объём V3 больше объёма V2 и во сколько раз температура T3 больше температуры T2 . Соответствует ли такое изменение V и T закону процесса перехода 2-3?
2. С помощью какой диаграммы и как графически определить работу газа в цикле 1-2-3-4-1?
З. Записать уравнение 1-го начала термодинамики для процессов 1-2 и 3-4. Чем отличаются процессы с точки зрения 1-го начала термодинамики?
4. Какие из процессов, входящих в состав данного цикла, протекают с поглощением теплоты и какие сопровождаются теплоотдачей?
Ответы.
1.С помощью линейки измеряем на диаграмме V, T отрезки OV3 , OV2 , OT3 , OT2 , находим их средние значения, которые в соответствующем масштабе (![]() и
и ![]() ) определяют значения объёмов V3 и V2 и температур T3 и T2 . Находим отношения:
) определяют значения объёмов V3 и V2 и температур T3 и T2 . Находим отношения: ![]() ≈ 2,5 и
≈ 2,5 и ![]() ≈ 2,5, откуда получаем
≈ 2,5, откуда получаем ![]() , что соответствует постоянству отношения объёма к температуре – закону Гей-Люссака:
, что соответствует постоянству отношения объёма к температуре – закону Гей-Люссака: ![]() .
.
2. Работа газа в цикле 1-2-3-4-1 графически определяется по графикам в координатах p, V следующим образом: элементарная работа газа подсчитывается по формуле ![]() , полная работа газа А=
, полная работа газа А=![]() и определяется площадью, ограниченную двумя изохорами, нулевой изобарой и кривой процесса. На участке 1-2 работа газа при его сжатии отрицательна (А’
и определяется площадью, ограниченную двумя изохорами, нулевой изобарой и кривой процесса. На участке 1-2 работа газа при его сжатии отрицательна (А’
На участке 2 – 3 работа газа при его расширении положительна (А` 0) и пропорциональна площади фигуры V223V3.
На участках 3 – 4 и 4 – 1 работа газа соответственно положительна и отрицательна и определяется площадями фигур V334V4 и V441V1.
Суммарная работа (с учётом знака составляющих) пропорциональна площади фигуры 1 2 3 4 1 (см. рис.):
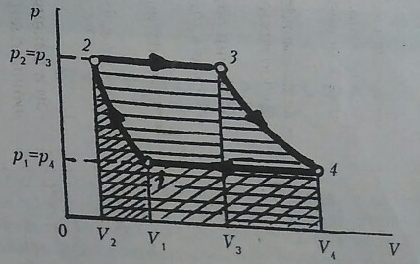
3. Первое начало термодинамики записывается в виде: ![]() U = A + Q, где A – работа внешних сил над газом, а A = –A ` (см. ответ на вопрос 2). Для изотермических процессов 1 – 2 и 3 – 4 первое начало термодинамики имеет вид Q = –A (при T = const U = const для идеального газа, и
U = A + Q, где A – работа внешних сил над газом, а A = –A ` (см. ответ на вопрос 2). Для изотермических процессов 1 – 2 и 3 – 4 первое начало термодинамики имеет вид Q = –A (при T = const U = const для идеального газа, и ![]() U = 0).
U = 0).
Для процесса изотермического сжатия газа 1 – 2 A 0 (A` 0) и Q
Для процесса изотермического расширения газа 3 – 4 A 0) и Q 0 – тепло к газу подводится.
4. На участках изобарного нагревания газа 2 – 3 и изотермического расширения 3 – 4 к газу тепло подводится, т.е. эти процессы сопровождаются поглощением газом теплоты извне; участки изобарного охлаждения 4 – 1 и изотермического сжатия 1 – 2 соответствуют теплоотдаче.

 Получите свидетельство
Получите свидетельство Вход
Вход












 Индивидуальные домашние задания по физике:"Графики изопроцессов" (1.14 MB)
Индивидуальные домашние задания по физике:"Графики изопроцессов" (1.14 MB)
 0
0 1090
1090 31
31 Нравится
0
Нравится
0


