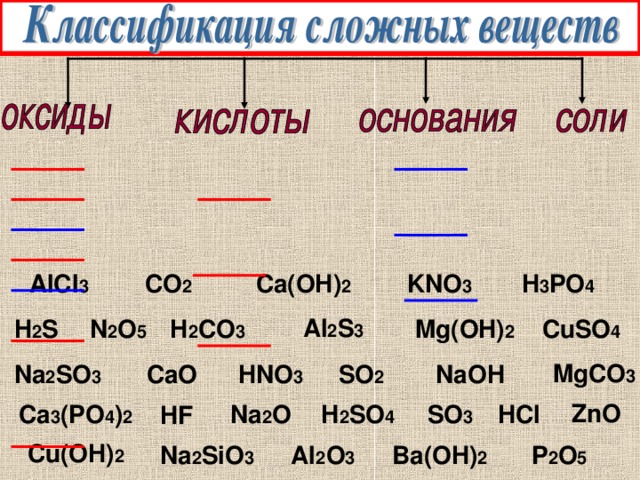
AlCl 3
H 3 PO 4
Ca(OH) 2
CO 2
KNO 3
Al 2 S 3
H 2 S
N 2 O 5
H 2 CO 3
Mg(OH) 2
CuSO 4
MgCO 3
SO 2
Na 2 SO 3
CaO
HNO 3
NaOH
ZnO
SO 3
Ca 3 (PO 4 ) 2
HCl
Na 2 O
H 2 SO 4
HF
Cu(OH) 2
P 2 O 5
Ba(OH) 2
Al 2 O 3
Na 2 SiO 3
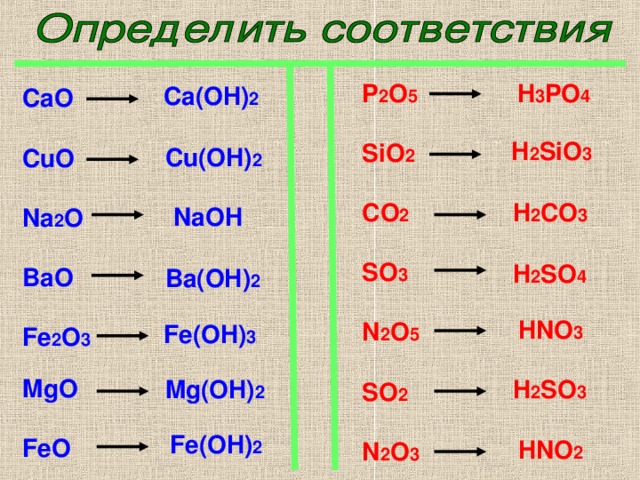
P 2 O 5
SiO 2
CO 2
SO 3
N 2 O 5
SO 2
N 2 O 3
H 3 PO 4
Ca(OH) 2
CaO
CuO
Na 2 O
BaO
Fe 2 O 3
MgO
FeO
H 2 SiO 3
Cu(OH) 2
H 2 CO 3
NaOH
H 2 SO 4
Ba(OH) 2
HNO 3
Fe(OH) 3
H 2 SO 3
Mg(OH) 2
Fe(OH) 2
HNO 2
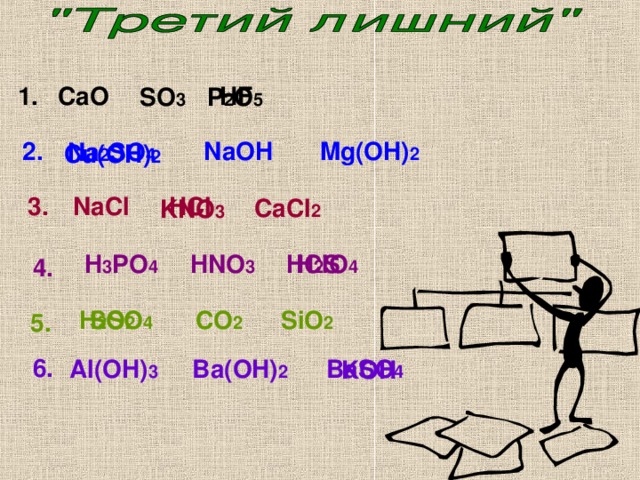
CaO
HF
1.
SO 3
P 2 O 5
Mg(OH) 2
2.
NaOH
Na 2 SO 4
Cu(OH) 2
3.
NaCl
HCl
CaCl 2
KNO 3
HClO 4
H 2 S
HNO 3
H 3 PO 4
4.
SiO 2
CO 2
SO 2
H 2 SO 4
5.
6.
Ba(OH) 2
BaSO 4
Al(OH) 3
KOH

Эти сложные вещества в при-
роде встречаются в жидком,
твёрдом и газообразном
состоянии.
КИСЛОТЫ
СОЛИ
ОСНОВАНИЯ
ОКСИДЫ
а
Эти соединения образуются в
результате р-ции нейтрализа-
ции, но не вода.
о
у
Эти вещества окрашивают лакмус в красный цвет.
ь
Эти вещ-ва окрашивают фенолфталеин в малиновый цвет.
л
Хлорид натрия – хорошо растворимая в воде … .
г
Эти вещества бывают одно-, двух- и трёхосновными.
Вещества, состоящие их двух элементов, одним из которых является кислород, называются …
я
н
В состав этих соединений входит гидроксильная группа.
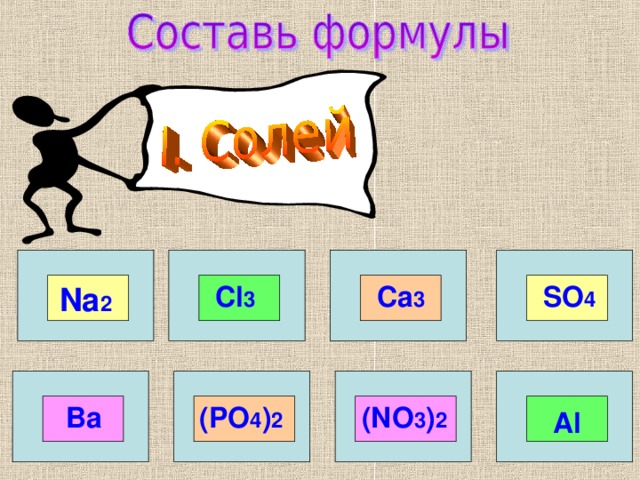
SO 4
Cl 3
Ca 3
Na 2
(NO 3 ) 2
(PO 4 ) 2
Ba
Al
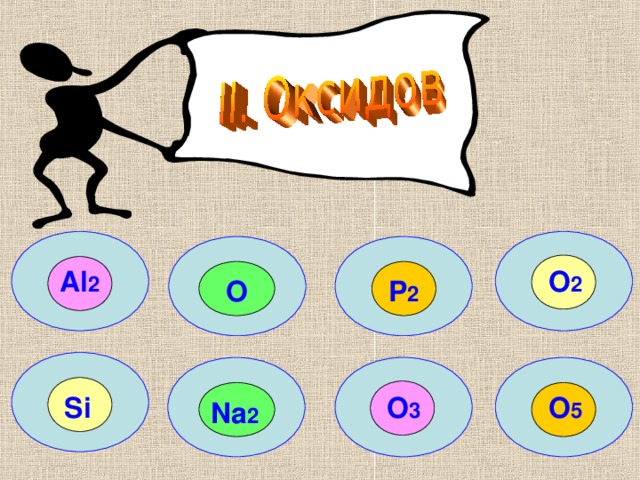
Al 2
O 2
O
P 2
O 5
Si
O 3
Na 2
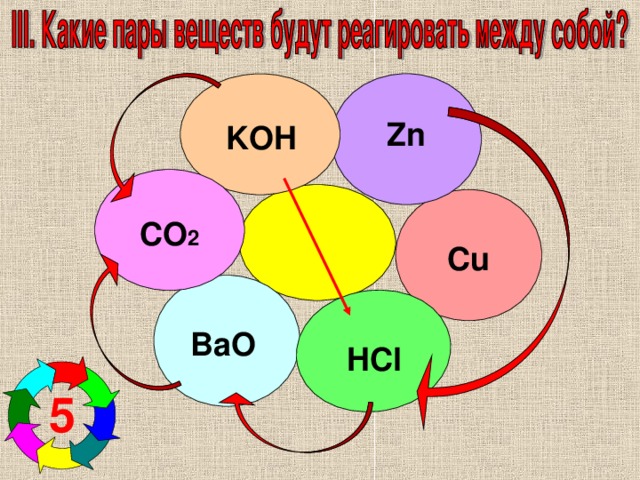
Zn
KOH
CO 2
Cu
BaO
HCl
5
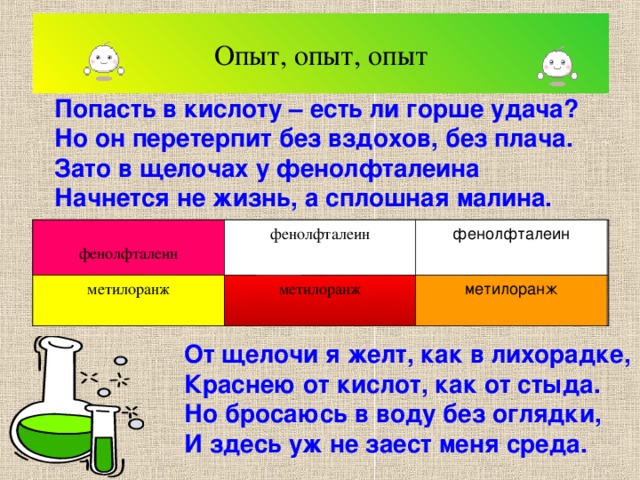
Опыт, опыт, опыт
Попасть в кислоту – есть ли горше удача? Но он перетерпит без вздохов, без плача. Зато в щелочах у фенолфталеина Начнется не жизнь, а сплошная малина.
фенолфталеин
фенолфталеин
фенолфталеин
NaOH
HCl
Н 2 О
метилоранж
метилоранж
метилоранж
От щелочи я желт, как в лихорадке, Краснею от кислот, как от стыда. Но бросаюсь в воду без оглядки, И здесь уж не заест меня среда.
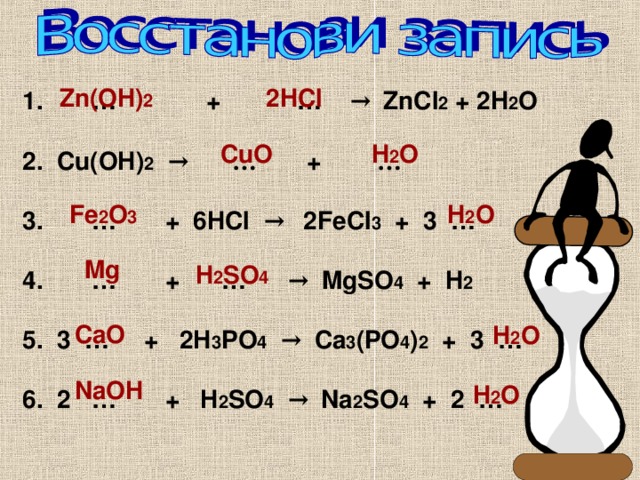
Zn(OH) 2
2HCl
1. … + … → ZnCl 2 + 2H 2 O
2. Cu(OH) 2 → … + …
3. … + 6HCl → 2FeCl 3 + 3 …
4. … + … → MgSO 4 + H 2
5. 3 … + 2H 3 PO 4 → Ca 3 (PO 4 ) 2 + 3 …
6. 2 … + H 2 SO 4 → Na 2 SO 4 + 2 …
H 2 O
CuO
Fe 2 O 3
H 2 O
Mg
H 2 SO 4
CaO
H 2 O
NaOH
H 2 O
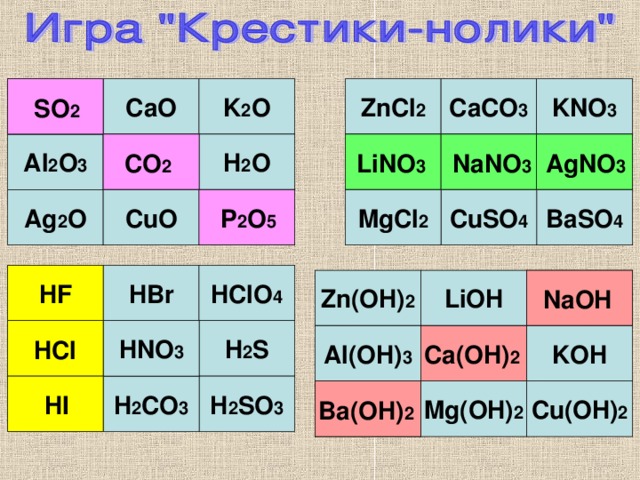
KNO 3
CaO
K 2 O
ZnCl 2
CaCO 3
SO 2
H 2 O
Al 2 O 3
AgNO 3
CO 2
LiNO 3
NaNO 3
CuO
BaSO 4
CuSO 4
MgCl 2
Ag 2 O
P 2 O 5
HClO 4
HBr
LiOH
Zn(OH) 2
HF
NaOH
HNO 3
H 2 S
KOH
Al(OH) 3
HCl
Ca(OH) 2
H 2 CO 3
H 2 SO 3
Mg(OH) 2
Cu(OH) 2
HI
Ba(OH) 2
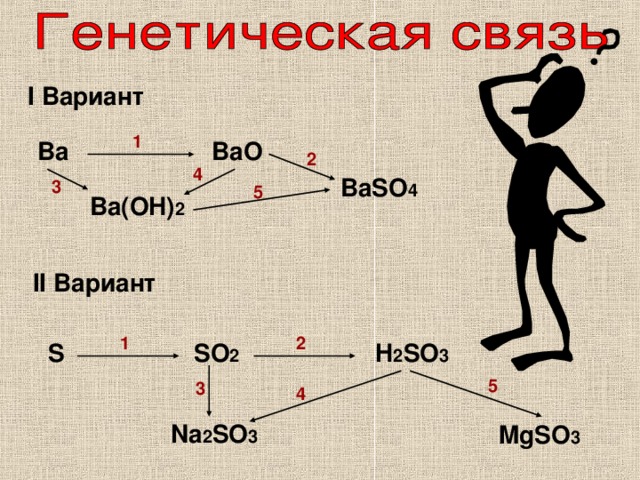
I Вариант
1
BaO
Ba
2
4
BaSO 4
3
5
Ba(OH) 2
II Вариант
1
2
H 2 SO 3
SO 2
S
5
3
4
Na 2 SO 3
MgSO 3
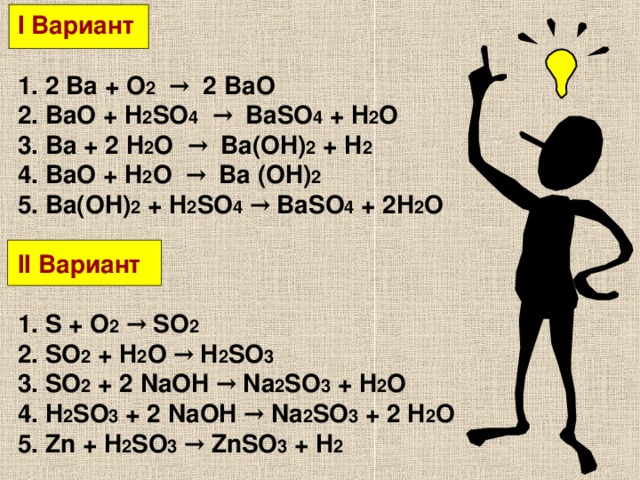
I Вариант
1. 2 Ba + O 2 → 2 BaO
2. BaO + H 2 SO 4 → BaSO 4 + H 2 O
3. Ba + 2 H 2 O → Ba(OH) 2 + H 2
4. BaO + H 2 O → Ba (OH) 2
5. Ba(OH) 2 + H 2 SO 4 → BaSO 4 + 2H 2 O
II Вариант
1. S + O 2 → SO 2
2. SO 2 + H 2 O → H 2 SO 3
3. SO 2 + 2 NaOH → Na 2 SO 3 + H 2 O
4. H 2 SO 3 + 2 NaOH → Na 2 SO 3 + 2 H 2 O
5. Zn + H 2 SO 3 → ZnSO 3 + H 2
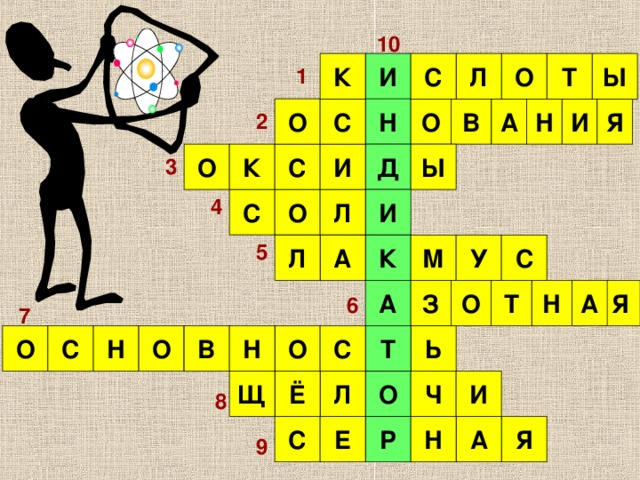
10
И
С
К
Т
О
Л
Ы
1
А
Н
О
С
О
В
Н
И
Я
2
Д
Ы
И
С
К
О
3
И
4
Л
О
С
5
С
У
М
Л
А
К
А
Я
Т
Н
О
З
А
6
7
С
Т
Ь
О
Н
В
Н
О
О
С
Ч
Ё
И
О
Л
Щ
8
С
Р
Е
Я
А
Н
9

 Получите свидетельство
Получите свидетельство Вход
Вход

























 Презентация по химии "Обобщение сведений об основных классах неорганических соединений" (0.3 MB)
Презентация по химии "Обобщение сведений об основных классах неорганических соединений" (0.3 MB)
 0
0 886
886 152
152 Нравится
0
Нравится
0


