
Тема: НЕМЕТАЛЛЫ.

НЕМЕТАЛЛЫ
ОБЩАЯ ХАРАКТЕРИСТИКА И СВОЙСТВА НЕМЕТАЛЛОВ.

НЕМЕТАЛЛЫ В ПРИРОДЕ
- В природе встречаются самородные неметаллы N 2 и O 2 (в воздухе), сера (в земной коре), но чаще неметаллы в природе находятся в химически связанном виде. В первую очередь это вода и растворённые в ней соли, затем минералы и горные породы (например различные силикаты, алюмосиликаты, фосфаты, бораты, сульфаты и карбонаты).
- По распространенности в земной коре неметаллы занимают самые различные места: от трех самых распространенных элементов (O, Si, H) до весьма редких (As, Se, I, Te).
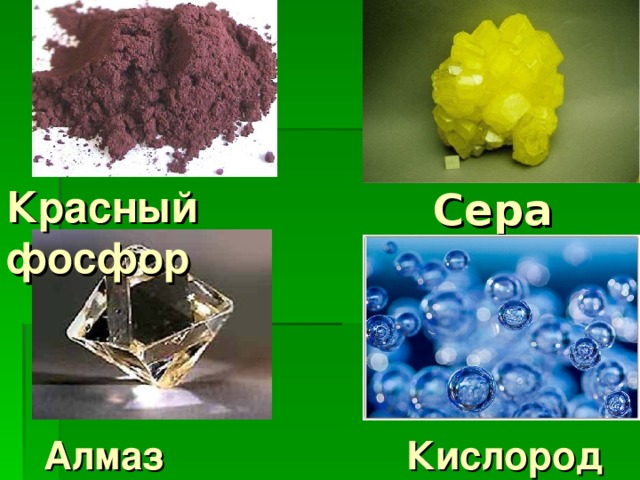
Красный фосфор
Сера
Алмаз
Кислород


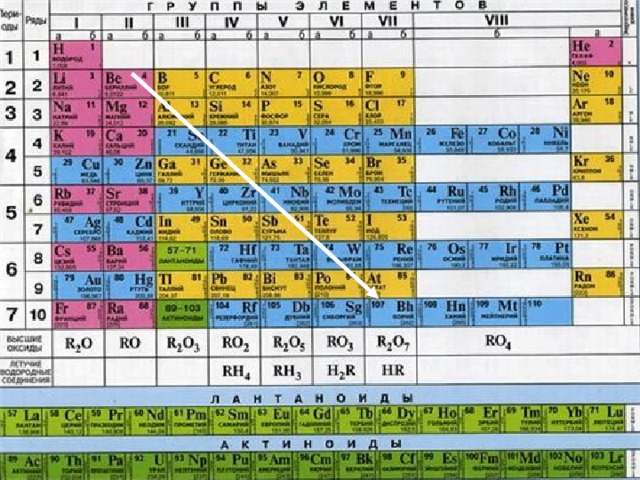
Положение металлов в Периодической системе химических элементов
- Если провести воображаемую диагональ от бериллия Be к астату At, то неметаллы расположатся в главных подгруппах выше диагонали (т. е. в верхнем правом углу). К неметаллам относятся также водород Н и инертные газы.

Физические свойста неметаллов.
Признаки сравнения
Характерные физические свойства
металлов
Агрегатное состояние
Цвет
Блеск
Прозрачность
Ковкость
Теплопроводность
Электропроводность
Плотность
Температура кипения и плавления
неметаллов
2.Типичный серебрист ы й
3 . Есть
4 .Непрозрач н ы
1.Твёрдое (фосфор, сера), жидкое (бром), газообразное (кислород, хлор)
2. Разнообразный (сера – жёлтый, фосфор – белый и красный)
3. Отсутствует
4. Газы водород, кислород, азот бесцветны
5. Отсутствует
6. Слабая
7. Слабая
8. Низкая
9. Низкие
5 . Хорошая
6 . Хорошая
7 . Хорошая
8 .Сравнительно высокая
9 . Высокие
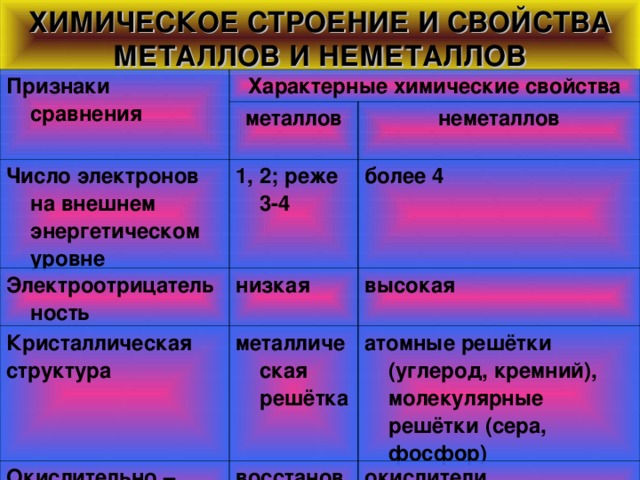
ХИМИЧЕСКОЕ СТРОЕНИЕ И СВОЙСТВА МЕТАЛЛОВ И НЕМЕТАЛЛОВ
Признаки сравнения
Характерные химические свойства
металлов
Число электронов на внешнем энергетическом уровне
неметаллов
1, 2; реже 3-4
Электроотрицательность
Кристаллическая
структура
низкая
более 4
высокая
металлическая решётка
Окислительно – восстановительные свойства
атомные решётки (углерод, кремний), молекулярные решётки (сера, фосфор)
восстановители
окислители

АЛЛОТРОПИЯ
- Аллотро́пия (от др-греч. αλλος — «другой», τροπος — «поворот, свойство») — существование одного и того же химического элемента в виде двух и более простых веществ, различных по строению и свойствам: так называемых аллотропических модификаций или аллотропических форм.


Аллотропия углерода


 Получите свидетельство
Получите свидетельство Вход
Вход
























 Презентация по химии "Общая характеристика и свойства неметаллов" (1.77 MB)
Презентация по химии "Общая характеристика и свойства неметаллов" (1.77 MB)
 0
0 2682
2682 418
418 Нравится
0
Нравится
0


