ДЕПАРТАМЕНТ ОБРАЗОВАНИЯ ГОРОДА МОСКВЫ
ГОУ СПО Колледжа связи № 54
МЕТОДИЧЕСКАЯ РАЗРАБОТКА
по теме
«БЕЛКИ – БИОЛОГИЧЕСКИЕ ПОЛИМЕРЫ»
Преподавателя химии
высшей категории
к.х.н. Аракелян Г.Г.
Москва 2009
БЕЛКИ - биологические полимеры
Тип урока. Изучение нового материала
Цели урока. Обучающие – изучение характеристики белков как высшей формы развития вещества на уровне понимания и применения полученных знаний на практике. Развитие внутренней мотивации учащихся к химии на примере творческой деятельности русских и советских ученых-химиков и писателей фантастов.
Развивающие – развитие познавательных умений учащихся, выделение существенных признаков и свойств в химических соединениях, устанавливание причинно-следственных связей, Приобретение знаний о строении, свойствах и получении питательных веществ, в употребляемых продуктах, умение анализировать, выполнять опыты, оформлять наблюдения в виде таблицы.
Методы обучения. Методы организации учебно-познавательной деятельности – словесные (эвристические беседы), наглядные (рисунки, таблицы, портретная галерея ученых–химиков и писателя А.Р.Беляева, опыты, ТСО), практические (лабораторная работа).
Методы стимулирования интереса к учению – привлечение художественной литературы (произведение А.Р.Беляева «Вечный хлеб»), учебные дискуссии.
Методы контроля. Устный контроль, экспериментальный контроль.
Оборудование и реактивы. Компьютер, видеокамера, телевизор, книга А.Р. Беляева «Вечный хлеб». На столах учащихся – конспекты, поддон для реактивов, штатив с пробирками, тигельные щипцы, раствор белка, растворы : глицерина, NaOH, CuSO4, HNO3, перо птицы, шерстяная нить, нить из искусственной шерсти, спички.
ХОД УРОКА
Организационный момент.
Отметить отсутствующих, объяснить цели урока и познакомить учащихся с его планом.
ПЛАН УРОКА
Повторить предыдущий материал: строение и свойства аминокислот. (Устный опрос)
Какие функциональные группы содержатся в аминокислотах?
Почему аминокислоты называют органическими амфотерными соединениями?
Какие аминокислоты относятся к -аминокислотам?
Могут ли аминокислоты взаимодействовать друг с другом?
Какой группой атомов соединены остатки -аминокислот?
Как называется реакция получения полипептидов?
Значение белков. Белки как пищевая составляющая в рационе человека
Функции белков в организме человека
Строение белков – их свойства
Выполнение лабораторной работы
Подведение итогов урока, определение домашнего задания
Итог урока: фронтальный опрос
БЕСЕДА ПО ТЕМЕ
«Белок как пищевая составляющая в рационе человека»
-Преподаватель. Вспомните, где в повседневной жизни вы могли встретить информацию о белке.
-Учащиеся. Информация о содержании белка на упаковках продуктов питания.
-Преподаватель. Какие известные вам сырьевые ресурсы природы с высоким содержанием белка?
-Учащиеся. Животные, бобовые растения (соя, горох, фасоль).
-Преподаватель. Достаточно ли продуктов питания с высоким содержанием белка в рационе человека?
-Учащиеся. Нет, так как существует разрыв между потребностью человечества в животном белке и низкими темпами развития животноводства.
-Преподаватель. Ежегодный разрыв между необходимым количеством пищевых продуктов и потребляемым населением Земли (в белке) составляет более 6 млн. тонн и год от года возрастает.
Однако, на земле имеются значительные ресурсы белка, которые уже широко используются для производства пищевых продуктов. Появились СПП (синтетические пищевые продукты) и ИПП (искусственные пищевые продукты).
Идеи о получении СПП из отдельных химических элементов и ИПП из низших организмов высказывал ещё в конце 19 в. Д.И.Менделеев.
На экране телевизора портрет Д.И.Менделеев
Писатель – фантаст А.Р. Беляев в своем произведении «Вечный хлеб» (1928г.) развил идею о создании искусственной пище для человека достаточно реалистично, описывая возможности науки химии и ее роль в осуществлении этой идеи.
На экране телевизора портрет А.Р. Беляев
Зачитывается отрывок из книги А.Р. Беляев «Вечный хлеб»:
- «Химия – великая наука и великая сила, но каждая наука имеет свои пределы. Если бы даже химикам удалось, скажем получить белок химическим путем, а рано или поздно это, конечно, будет достигнуто, то проблема питания ещё не будет разрешена.»
- «Создать химически все необходимое для питания организма – разрешимая, но чрезвычайно трудная задача при современном состоянии наших знаний».
-Преподаватель. Как вы думаете, в каком году была написана книга А.Р. Беляев «Вечный хлеб»?
-Учащиеся. Высказывают свои предположения.
-Преподаватель. Это произведение было написано в 1928 году.
Писатели - фантасты в своем творчестве всегда опережали время, научный прогресс. И нередко, их творческая мысль со временем воплощалась в жизнь в виде научных открытий и изысканий ученых.
СССР во второй половине ХХ века внес особый научный и технологический вклад в развитие новой отрасли пищевой промышленности- искусственные пищевые продукты.
Ученые решили создать, сконструировать, искусственные продукты питания, внешне не отличающиеся от привычных для нас традиционных продуктов, на базе использования имеющихся ресурсов белка.
Конструирование пищи заключается в выделении белка из сырья различной природы и превращении его машинным способом в аналог пищевого продукта с заданным составом и свойствами.
В СССР широкое исследование по проблеме белковых ИПП начались в 60-х г. по инициативе академика А.Н.Несмеянова.
На экране телевизора портрет А.Н.Несмеянова
В 1961 году А.Н. Несмеянов впервые сформулировал проблему получения пищи нетрадиционными методами. Так, был разработан и освоен промышленностью метод приготовления белковой зернистой икры, подобной икре осетровых, на основе белков молока. Другое направление – выращивание дрожжей на углеводородах нефти и получение из них пищевого белка. В результате возникла новая отрасль промышленности – микробиологическая. И еще один путь, чисто химический, – синтез аминокислот, составляющих основу белков. Эти работы проводили в ИНЭОСе (Элементоорганических соединений институт РАН им. А.Н.Несмеянова. Москва, ул.Вавилова, 28) и в некоторых институтах Ленинграда (ныне Санкт-Петербург).
В результате были получены ИПП: зернистая икра, мясоподобные продукты и другие изделия. Был создан аналог готового колбасного фарша по вкусу, запаху, внешнему виду, структуре совершенно не отличается от натурального продукта.
Интерес Несмеянова к синтезу пищи не случаен. Главная задача, которую он хотел решить, – получать пищевой белок, не убивая животных. Татьяна Николаевна, его сестра, вспоминает: "В девять лет Шура отказался есть мясо, а в двенадцать лет стал полным вегетарианцем, отказавшись и от рыбы. В основу легло твердое убеждение, что нельзя убивать животных. Это не было никем внушено, и всю свою жизнь он не изменял данному себе однажды в детстве слову".
Производство аналогов пищевых продуктов—область сравнительно молодая, но уже обеспечивающая миллиарды потребителей во всем мире, включая и Россию.
В настоящее время в мире организовано широкомасштабное производство искусственных пищевых продуктов.
Вам, наверное, будет интересно узнать, что кроме искусственных мясопродуктов изготовляют искусственные молоко и молочные продукты, крупы, макаронные изделия, "картофельные" чипсы, "ягодные" и "фруктовые" продукты, "ореховые" пасты для кондитерских изделий, подобия устриц. (В частности, на банках с искусственным сгущенным "молоком" пишут название не "Сгущённое молоко", а "Сгущёнка" - будьте внимательны при выборе.)
Белок интересен не только как составляющая нашего пищевого рациона, но и как важная компонента жизни.
Рассмотрим роль белка и его функции в живых организмах.
Строительная Из белка состоят кости мышцы и другие ткани живых организмов, они входят в состав клеточных мембран принимают участие в строительстве всего организма.
Энергетическая Белок, как любой пищевой продукт обеспечивает организм энергией и важными микроэлементами. При окислении 1 г белка выделяется 17,6 кДж энергии.
Каталитическая Все катализаторы в живых организмах - белки. Они спопобствуют ускорению химических процессов в клетках в сотни тысяч раз.
Двигательная Сокращаясь белки, создают в клетках и во всем организме двигательные реакции
Транспортная С помощью гемоглобина (белок-крови) транспортируется кислород от легких к клеткам организма, а из клеток выносит углекислый газ.
Сигнальная Белки принимают участие в передаче нервных возбуждений.
Защитная Белки способны разрушать бактерии, вирусы - антитела. Они составляют защитную систему организма, то есть иммунную систему.
Регуляторная Белки дозируют и регулируют обменные процессы в клетках. Инсулин(белок)-регулирует обмен глюкозы.
По каждому из восьми пунктов, с учащимися ведётся дискуссия.
На наглядных примерах разбирается роль и участие белковых молекул в жизнедеятельности организмов.
Белки, в организме, могут превращаться в жиры и углеводы. Обратное превращение невозможно.
По разнообразию своих функций с белками не может сравниться ни одно из веществ организма.
Недостаток белка в рационе человека может привести к тяжелым заболеваниям (истощение, быстрая утомляемость и др.)
Белки обеспечивают процессы жизнедеятельности всех животных и растительных организмов.
ВЫВОД: «ЖИЗНЬ – ЕСТЬ ФОРМА СУЩЕСТВОВАНИЯ БЕЛКОВЫХ ТЕЛ».
Состав и строение белка
Белки–биополимеры, то есть они являются природными высокомолекулярными соединениями. Их относительная малекулярная масса имеет более 10 000 а.е.м. и достигает значений сотни миллионов.
При гидролизе любого белка получается смесь около 20 разновидностей -аминокислот.
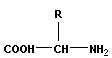
Строение аминокислот, составляющих белки, можно выразить общей структурной формулой R-CH(NH2)-COOH.
На экране телевизора общая структура -аминокислот
или 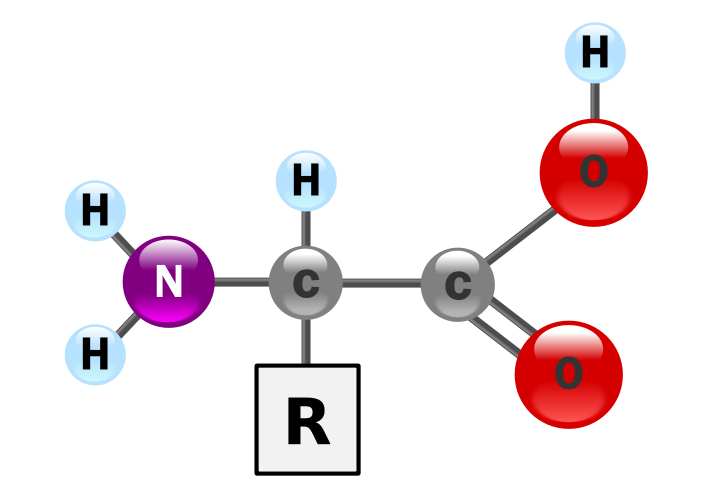
В состав заместителя R могут входить открытые цепи, циклы и различные функциональные группы.
По элементному составу – это углерод 50~%, водород ~7%, кислород ~22%, азот ~19%, сера ~2% . Наиболее часто в составе белков встречается:
глицин NH2–CH2-COOH
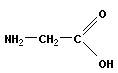
глицин (Gly)
аланин CH3–CH(NH2)-COOH
цистеин HS-CH2-CH(NH2)-COOH
серин HO-CH2-CH(NH2)-COOH и т.д.
Десять из них не синтезируются живым организмом. Это так называемые незаменимые аминокислоты (табл.1).
На экране телевизора Таблица 1. «Незаменимые аминокислоты»
Как же аминокисоты образуют белковую молекулу?
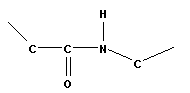
Ещё в 80-х г. 19-го столетия русский биохимик А.Я.Данилевский изучая различные белки указал на наличие в них пептидных групп (-CONH-).
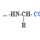
На экране телевизора пептидная группа
В начале 20-го столетия немецкий ученый Э.Фишер предположил, что белки представляют собой длинные цепи аминокислот, соединенные пептид ными (амидными ) связями.
В процессе реакции поликонденсации между аминокислотами при взаимодействии карбоксильных групп одних молекул и аминогрупп других молекул отщепляются молекулы воды и образуются пептидные группы.
На экране телевизора «Схема реакции поликонденсации между аминокислотами»
Схема реакции поликонденсации между аминокислотами
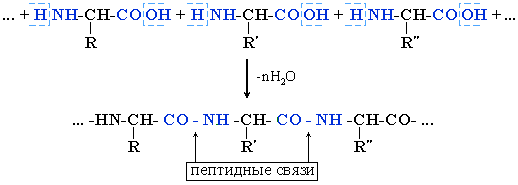
Э.Фишеру и другим исследователям удалось синтезировать соединения, в молекулу которых входило 18 остатков различных -аминокислот, соединенных такими связями. Эти полипептиды по некоторым свойствам напоминали белки.
Природные белки являются высокомолекулярными соединениями и в их полипептидных цепочках аминокислотные остатки повторяются многократно.
Из набора двадцати разновидностей -аминокислот может быть образовано практически безграничное количество различных белковых молекул.
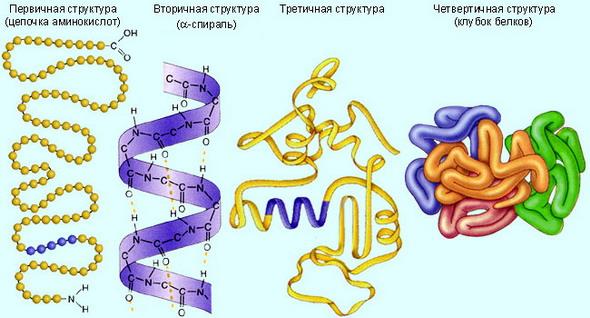
Различные свойства белковых молекул определяется их строением:
Первичная структура – последовательность чередования различных аминокислотных звеньев в полипептидной цепи;
Вторичная структура – спирализация белковой молекулы за счёт образования многочисленных водородных связей между группами
–CO- и -NH-, впервые найденная Л. Полингом и Р.Б.Кори.
Третичная структура – расположение спирализованной молекулы в пространтве. Она поддерживается взаимодействием различных функциональных групп полипептидной цепи и возникновением водородных связей.
Четвертичная структура – соединение нескольких белковых молекул друг с другом в крупные агрегатные сообщества.
На экране телевизора плакат «Структуры белка»
Денатурация белка
С изменением структуры белковых молекул изменяется свойство белка.
К этому приводят следующие воздействия, оказываемые на белок:
Соли тяжелых металлов (Cu, Hg, Pb и.т.п.)
Радиация
Высокие температуры (при т-ре до 1000 большинство белков свертываются, т.е. живое гибнет)
Агрессивные среды (кислоты, щелочи)
Этиловый спирт
Гидролиз белков (процесс пищеварения в организме)
Экспериментальная работа. Исследование растворов на содержание белка. Преподаватель проводит опыт 1.
Цветные реакции белка (качественные реакции на белок)
А. (Ксантопротеиновая реакция)
Белок (раствор) + HNO3 (конц.) → жёлтое окрашивание
Б. (Биуретовая реакция)
Белок (раствор) + CuSO4 → фиолетовое окрашивание
В. Белок (раствор) + C2H5OH → белое окрашивание
Г. Белок (раствор) + (CH3COO)2Pb → черное окрашивание
Опыт 2.
Преподаватель проводит эксперимент, демонстрируя горение белка (появление специфического запаха – качественное определение серы) на примере шёлка, пера птицы, шерсти, кожи.
Далее учащимся предлагается выполнить исследовательскую экспериментальную работу:
Определить растворы белка и глицерина в пронумерованных пробирках реактивом Cu(OH)2 .
Определить искусственную и натуральную шерсть ( пряжа) в выданных пакетиках.
ВОПРОСЫ ПО ПРОЙДЕННОЙ ТЕМЕ
Какие химические соединения используются в организме для синтеза белков?
Перечислите важнейшие химические свойства белка. Какие из них являются качественными?
Какие цветные реакции доказывают наличие белка?
Какими биологическими функциями обладают белки?
Какова роль белков для жизнедеятельности живого организма?
Каким путем решается проблема удовлетворения человека белками?
В результате гидролиза белка какие соединения получатся?
Как можно распознать натуральный шелк и натуральную шерсть?
Домашнеее задание:
§17 БЕЛКИ
Габриелян О.С. Химия. 10 класс. Базовый уровень. М.: Дрофа, 2009.-191с.
ЛАБОРАТОРНАЯ РАБОТА
ИНСТРУКЦИЯ К ЭКСПЕРИМЕНТУ
«Исследование свойств белка:
распознавание в белковой молекуле пептидной группы»
СТРОГО ВЫПОЛНЯЙТЕ ПРАВИЛА ТЕХНИКИ БЕЗОПАСНОСТИ ПРИ ВЫПОЛНЕНИИ ПРАКТИЧЕСКИХ РАБОТ!
Исследование растворов в пробирках на содержание белка и многоатомного спирта-глицерина.
Вопросы для повторения:
1.Каким реактивом можно определить многоатомный спирт?
1. С помощью какого реактива можно распознать растворы белка и глицерина?
АЛГОРИТМ
К растворам в пробирках добавить:
NaOH (гидроксид натрия) – 1 мл
CuSO4 (сульфат меди (11)) – 0,5 мл
Пробирки встряхнуть.
Наблюдать изменение цвета.
Занести в таблицу полученные результаты.
Исследование волокна. Отличить натуральную шерсть от искусственной по характерному запаху при горении.
АЛГОРИТМ
Взять волокна щипцами и поджечь.
По запаху определить наличие шерсти в исследуемых образцах пряжи.
Занести в таблицу полученные результаты.
| Исследование растворов | Исследование волокон |
| Белок | № пробирки | Натуральная шерсть | Цвет пряжи № пакета |
| Глицерин | № пробирки | Искусственная шерсть | Цвет пряжи № пакета |
Оформленную работу в лабораторных тетрадях сдать преподавателю.

ДМИТРИЙ ИВАНОВИЧ МЕНДЕЛЕЕВ
( 8.02.1834 – 2.02.1907 )

АЛЕКСАНДР РОМАНОВИЧ БЕЛЯЕВ
( 1884-1942 )

АЛЕКСАНДР НИКОЛАЕВИЧ НЕСМЕЯНОВ
( 1899 – 1980 )
Таблица 1
Незаменимые аминокислоты
| Название | Сокращенное
обозначение | R | | Валин, α-аминоизовалериановая кислота | Val | 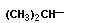
| | Лейцин, α-аминоизокапроновая кислота | Leu | 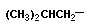
| | Изолейцин, α-амино-β-метилвалериановая кислота | Ile | 
| | Фенилаланин, α-амино-β-фенилпропионовая кислота | Phe | 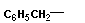
| | Метионин, α-амино-γ-метилтиомасляная кислота | Met | 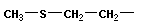
| | Триптофан, α-амино-β-имидолилпропионовая кислота | Try | 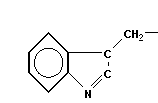
| | Треонин, α-амино-β-гидроксимасляная кислота | Thr | 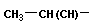
| | Гистидин, α-амино-β-имидазолилпропионовая кислота | His | 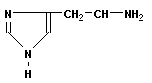
| | Лизин, α, ε-диаминокапроновая кислота | Lys | 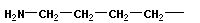
| | Аргинин, α-амино-δ-гуанидинвалериановая кислота | Arg | 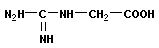
|
|
СТРУКТУРЫ БЕЛКОВЫХ
МОЛЕКУЛ
Литература
Ю.М.Ерохин Химия. - М.: Мастерство, 2002. – 384 с.
О.С.Габриелян, И.Г.Остроумов. Химия: учеб. для студ. сред. проф. учеб. заведений – М.: «Академия», 2008.
Захаров В.Б. «Общая биология» 10-11 кл. М.: «Дрофа», 2002.
Новошинский И.И., Новошинская Н.С. Органическая химия. 11 класс. М.: ООО «ТИД «Русское слово – РС», 2008.
Габриелян О.С. Химия. 10 класс. Базовый уровень. М.: Дрофа, 2009.
Волков В.А., Вонский Е.В., Кузнецов Г.И. Выдающиеся химики мира:
Биографический справочник. – М.: Высшая школа, 1999.
Добротин Р.Б., Карпило Н.Г., Керова Л.С., Трифонов Д.Н. Летопись жизни и деятельности Д.И.Менделеева. – Л.: Наука, 1984.
А.Р.Беляев «Вечный хлеб». Собрание сочинений в пяти томах.-Л.: Изд.»Детская литература», 1983.
Интернет ресурсы :
Статья. Доктор химических наук Э.Г.Перевалова «На стыке наук».
Статья. Ответственный редактор А.В.Сторонкин «Летопись жизни и деятельности Д.И.Менделеева»
Статья. П.А.Чугаев «Дмитрий Иванович Менделеев. Биография русского гения». Экология и жизнь, №1, 2009.
Краткий биографический словарь. «Русские писатели и поэты» М., 2000.
«Современные технологии в пищевой промышленности»
Искусственная пища. Информационный сайт для населения Immunologia.ru.
Википедия: Биография писателя А.Р.Беляева
Таблица 1
Незаменимые аминокислоты
| Название | Сокращенное
обозначение | R |
| Валин, α-аминоизовалериановая кислота | Val | 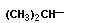
|
| Лейцин, α-аминоизокапроновая кислота | Leu | 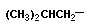
|
| Изолейцин, α-амино-β-метилвалериановая кислота | Ile | 
|
| Фенилаланин, α-амино-β-фенилпропионовая кислота | Phe | 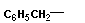
|
| Метионин, α-амино-γ-метилтиомасляная кислота | Met | 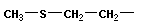
|
| Триптофан, α-амино-β-имидолилпропионовая кислота | Try | 
|
| Треонин, α-амино-β-гидроксимасляная кислота | Thr | 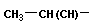
|
| Гистидин, α-амино-β-имидазолилпропионовая кислота | His | 
|
| Лизин, α, ε-диаминокапроновая кислота | Lys | 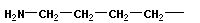
|
| Аргинин, α-амино-δ-гуанидинвалериановая кислота | Arg | 
|
19


 Получите свидетельство
Получите свидетельство Вход
Вход






















 Белки-биополимеры (0.36 MB)
Белки-биополимеры (0.36 MB)
 1
1 493
493 35
35


Смотрите код внизу любого письма рассылки сайта на зеленом фоне.